
- •Получение кремниевых подложек. Маркировка подложек.
- •Основы химической теории травления кремния
- •Факторы, влияющие на скорость химического травления кремния
- •Достоинства пхт
- •Анизотропия и селективность при пхт
- •Факторы, влияющие на скорость пхт
- •Понятие о рит (реактивно-ионное травление)
- •Механизм образования естественного окисла на поверхности кремния
- •Термическое окисление. Уравнение Дила-Гроува
- •Факторы, влияющие на скорость термического окисления
- •Практические методы термического окисления
- •Структура двуокиси кремния
- •Маскирующие и пассивирующие свойства окисла кремния
- •Зарядовые свойства окисла кремния
-
Термическое окисление. Уравнение Дила-Гроува
Особенности процесса термического окисления кремния во многом определяются структурой и свойствами образующейся стеклообразной пленки двуокиси кремния (700-1150 С). Окисел обладает открытой пространственно-полимерной структурой с прочными связями Si-O-Si и, с одной стороны, имеет высокую проницаемость, с другой стороны, является одним из лучших диэлектриков с очень высоким сопротивлением, вплоть до температур, близких к температуре плавления. Поэтому процесс окисления кремния не может быть аналогичен процессам окисления металлов, где рост окисла предполагается за счет отрыва металлических ионов и их диффузии в растущем окисле.
Рост окисла кремния SiO2 происходит на границе раздела кремний - окисел в атмосфере сухого кислорода или паров воды согласно реакциям
Si + O2 = SiO2;
Si + H2O = SiO2 + 2H2.
При этом граница двух фаз Si - SiO2 движется в глубь полупроводника, часть кремния поглощается окислом.
Толщина пленки SiO2, равная x, поглощает слой кремния толщиной 0,44 x. Таким образом, можно считать, что толщина окисла примерно в два раза больше толщины поглощенного им кремния.
Высокотемпературный процесс окисления кремния рассматривается обычно состоящим из двух этапов: диффузии окисляющих частиц через растущий окисел и их химического взаимодействия с кремнием на границе раздела двух фаз Si - SiO2.
Диффундирующими частицами в случае окисления в сухом кислороде считаются либо молекулы кислорода O2, либо атомы кислорода.
При окислении в парах воды окисляющими частицами могут быть молекулы воды H2О, а также ионные пары H3O+ и OH–.
Уравнение Дила-Гроува
-Доставка кислорода к поверхности. F1 = h(C* – C0),
-Его диффузия через
слой уже сформировавшегося окисла к
границе с подложкой.
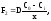
-Химическая реакция с материалом подложки. F3 = kCi
h - коэффициент переноса окисляющих частиц через внешнюю границу окисла; C* и С0 - концентрации окисляющих частиц вне окисла и вблизи поверхности внутри окисла в любой момент времени окисления t
D - коэффициент диффузии окисляющих частиц; Ci - концентрация окислителя на границе SiO2 – Si
-
Факторы, влияющие на скорость термического окисления
-
Температура процесса
-
Давление окислителя
-
Кристаллографическое ориентирование подложки
-
Степень легирования подложки
-
Время
-
Практические методы термического окисления
Окисление в сухом кислороде с добавлением галогенов. Некоторые соединения галогенов (газообразные Cl2, НСl и СНСl3 (трихлорэтилен)) вводят в поток сухого кислорода для улучшения свойств оксида и расположенного под ним кремния.
Окисление в парах воды. При окислении в парах воды источником окислителя служит вода высокой чистоты (10 - 20 МОм см), которая нагревается до температуры, достаточной для образования потока водяных паров.
Окисление во влажном кислороде. Процесс окисления во влажном кислороде представляет собой комбинацию двух ранее рассмотренных процессов окисления: в парах вода и в сухом кислороде. Установка для окисления во влажном кислороде представляет собой систему, в которой сухой кислород пропускается через водяную баню (барботер), вода в которой нагрета до 95 °С.
Пирогенное окисление. Окисление во влажном кислороде может проводиться пирогенным методом, при котором образование паров воды происходит за счет реакции Н2 и 02 . Водород Н2 сжижается и образуется водяной пар под давлением (5 - 10) 105 Па. Пирогенный метод гарантирует получение паров воды высокой чистоты, что связано с высокой чистотой используемых газов.
Окисление при повышенном давлении. Повышение давления водяных паров приводит к дополнительному увеличению скорости роста.
