
- •Тесты к модулю №1 (для итогового рубежного контроля)
- •1) Термодинамика. Химическое равновесие.
- •4) Для нахождения реакции, следует воспользоваться формулой…
- •5) Для нахождения реакции, следует воспользоваться формулой …
- •6) Если энтальпия образования so2 равна -297 кДж/моль, то количество теплоты, выделяемое при сгорании 16г серы, равно . . . КДж
- •7) В реакции, протекающей в соответствии с термохимическим уравнением
- •12. В результате реакции, описываемой термохимическим уравнением
- •15. В результате реакции, термохимическое уравнение которой
- •23. В реакции, протекающей в соответствии с термохимическим уравнением
- •33) Будет ли влиять давление на смещение равновесия данной реакции
- •15) Сумма коэффициентов в уравнении реакции, соответствующая схеме , составляет …
- •39) В системе, состоящей из луженого (покрытого оловом) железа при нарушении целостности покрытия в морской воде самопроизвольно протекает…
- •61) Гидроксид хрома (|||) Сr(oh)3 может проявлять в окислительно – восстановительных реакциях свойства:
- •1. Молярная масса неэлектролита, раствор 11,6 г которого в 200 г воды замерзает при -1,86°с (), равна _____ г/моль.
- •2. Массовая доля метанола в растворе, содержащем 60 г спирта и 40 г воды равна…
- •11. Молярная концентрация раствора, в 2 л которого содержится 4,25 г хлорида лития, равна ______ моль/л.
23. В реакции, протекающей в соответствии с термохимическим уравнением
3H2 + N2 = 2 NH3 + 92 кДж
выделилось 23 кДж теплоты. Объём полученного (при н.у.) аммиака
2) 11,2л
24) По термохимическому уравнению С2Н4+Н2О↔С2Н5ОН+46 кДж
вычислите объём взятого этилена (н.у.), если известно, что выделившаяся в этом процессе теплота составила 138 кДж.
3) 67,2л
25) В реакцию, протекающую в соответствии с термохимическим уравнением 2Al + 3S = Al2S3 +509 кДж вступило 108 г алюминия. Количество выделившейся теплоты равно
3) 1018 кДж
26) В результате реакции, термохимическое уравнение которой 2Al +Fe2O3 = Al2O3 + 2 Fe +848 кДж, выделилось 169,6 кДж теплоты. Масса образовавшегося железа равна:
2) 22,4 г
27) По термохимическому уравнению реакции горения ацетилена 2С2Н4 + 5О2 = 4СО2 + 2Н2О +2610 кДж рассчитайте, сколько выделится теплоты, если в реакцию вступило 67, 2 л ацетилена (н.у.)
2) 3915 кДж
28) Уравнение константы равновесия гетерогенной химической реакции 2H2S(г) + SO2(г) ↔ 2S(к) + 2Н2O (г)…
1)
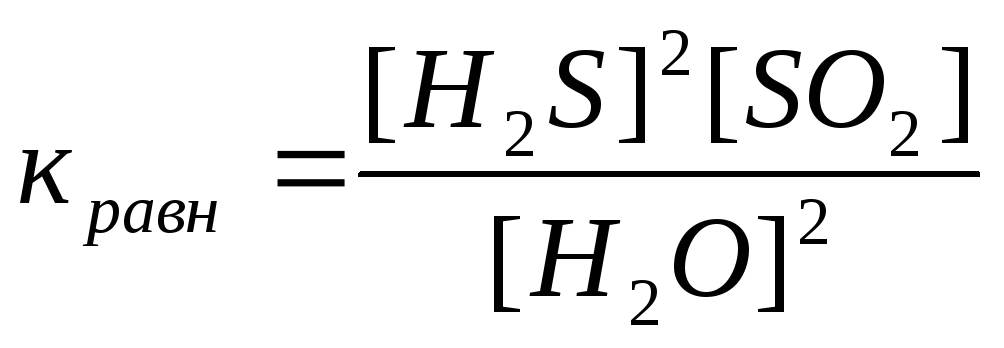 2)
2)
3)
 4 )
4 )
29) Уравнение константы равновесия гетерогенной химической реакции
2СО(г)↔С (графит) +СО2(г) имеет вид…
1)
![]() 2)
2)![]()
3)
![]() 4)
4)![]()
30) Как нужно изменить давление, чтобы реакция гемоглобина с кислородом Hb + O2 « HbO2 была смещена вправо
2) увеличить давление
31) Какое значение константы равновесия соответствует данной реакции 2NO +O2 « 2NO2
2) Kc= [NO2]2 / [NO]2[O2]
32) Как нужно изменить давление реакции N2+3H2 « 2 NH3, чтобы сместить равновесие вправо
2) увеличить
33) Будет ли влиять давление на смещение равновесия данной реакции
H2 + Cl2 = 2 HCl
2) нет
34) Какие значения должна принимать энергия Гиббса, чтобы процесс шёл в обратном направлении
2) DG0 > 0
35) Равновесие в реакции, уравнение которой СН4(г) + 4S(ж) ↔ СS2(г) + 2Н2S(г), ΔH<0, сместиться влево при
4) увеличении концентрации H2S
36) Будет ли проходить реакция в прямом направлении, если DG = 18 кДж/моль
1) нет
37) Система, в которой повышение давления и повышение температуры приведут к смещению равновесия в противоположных направления
4) С2Н2(г) + 2Н2(г) ↔ С2Н6 (г), ΔН<0
38) Как нужно изменить давление, чтобы реакция гемоглобина с кислородом была смещена влево Hb + O2 « HbO2
1) уменьшить давление
39) В реагирующей системе, уравнение которой NO(г) + Cl2(г) ↔ NOCl2(г) ΔH > 0, равновесие сместиться вправо при:
1) повышении давления
40) Какие значения должна принимать энергия Гиббса, чтобы процесс шёл в прямом направлении
1) DG < 0
41) Как нужно изменить давление, чтобы сместить равновесие реакции
N2 + 3H2 «2 NH3 влево
1) уменьшить
42) Для смещения
равновесия в системе SO2(г)+Cl2(г)![]() SO2Cl2(г),
ΔH < 0 в сторону продуктов реакции
необходимо
SO2Cl2(г),
ΔH < 0 в сторону продуктов реакции
необходимо
1) понизить температуру
43) На состояние химического равновесия в системе
2SO2(г) + О2 (г) ↔2 SO3, ΔH0 < 0 не влияет
1) катализатор
44) Какое выражение соответствует константе химического равновесия для данной реакции N2+3H2 = 2NH3
2) Кс = [NH3]2 / [N2][H2]3
45) Будет ли влиять давление на смещение равновесия данной реакции H2 + Cl2 = 2 HCl
2) нет
46) Равновесие в реакции, уравнение которой
СН4(г) + 4S(ж) ↔ СS2(г) + 2Н2S(г), ΔH<0, сместиться влево при
4) увеличении концентрации H2S
47) Как нужно изменить давление, чтобы реакция гемоглобина с кислородом была смещена влево Hb + O2 « HbO2
1) уменьшить давление
48) В каком направлении идёт данная реакция
H3PO4 + аденозин = АТФ + H2O, G0298 = 14 кДж/моль
1) в обратном
49) Согласно уравнению гомогенной химической реакции С2Н2 + Н2 С2Н4; Н0, …
3) повышение давления смещает равновесие вправо
50) При увеличении давления в системе Н2(г) + I2(г) 2HI(г), fH00…
3) состояние равновесия не изменяется
51) Исходя из уравнения реакции C2H4(г) = 2С (графит) + 2Н2(г), ∆Н0=-52,3 кДж, стандартная энтальпия образования этилена равна____кДж/моль
52,3
52) Повышение давления смещает равновесие в сторону продуктов для реакции…
ВаО(к.) + СО2(г) ↔ ВаСО3(к.)
53) Для увеличения выхода продуктов реакции FeO(т) + H2(г)↔Fe(т) + H2O(г), ∆Н>0 необходимо…
повысить температуру
54) Согласно первому началу термодинамики, справедливо выражение…
∆U=Q-A
55) Для нахождения ∆Н0298 реакции 4HCN(г) + 5О2(г) = 2Н2О(ж) + 4СО2(г) + 2N2(г) ,
следует воспользоваться формулой…
∆Н0298 = 2∆Н0298, Н2О (ж) + 4∆Н0298, СО2 (г) - 4∆Н0298, НСN (г)
56) Неверно, что согласно 2 началу термодинамики…
2) тепловой эффект обратной реакции больше теплового эффекта прямой реакции
57) Если прямая экзотермическая реакция протекает с уменьшением количества газообразных веществ, то согласно принципу Ле-Шателье , чтобы сместить равновесие в сторону продуктов, следует…
1) повысить давление
58) Наибольшему значению энтропии соответствует состояние воды…
4) Н2О(г) 398К
59) Количественное соотношение между изменением внутренней энергии, теплотой и работой устанавливает______ закон термодинамики
2) первый
60) Реакция CaCO3= CaO + CO2, для которой ∆Н=178кДж, ∆S=160Дж/моль×К, при стандартных условиях:
2) протекает в обратном направлении
61) Для экзотермического процесса синтеза аммиака одновременное понижение температуры и увеличение давления_________выход аммиака
увеличивает
62) Уравнение реакции, проходящей с увеличением энтропии, имеет вид…
NH4NO3(Т) = N2(Г) + 2 H2O(Г)
63) Выберите соединения с макроэргическими связями:
2) АТФ
2) Окислительно-восстановительные реакции. Электролиз.
1) Перманганат ион MnO4- в кислой среде восстанавливается до …
4) Mn2+
2) Оксид марганца (IV) MnO2 может проявлять в окислительно-восстановительных реакциях свойства
и окислителя, и восстановителя
3) При электролизе водного раствора KCl на катоде выделяется …
H2
4) В качестве восстановителей в промышленных условиях используют…
1) СО и Н2
5) Согласно уравнению Нернста потенциал электрода…
Зависит от его природы
6) Окислителем в реакции KMnO4+KNO2+H2SO4K2SO4+MnSO4+H2O является…
KMnO4
7) ЭДС гальванического элемента, состоящего из медного и цинкового электродов, погруженных в 0,01 М растворы их сульфатов
(Е0Сu2+/Cu=0,34B, Е0Zn2+/Zn=-0,76B) равна___В.
1,10
8) Для вычисления потенциала серебряного электрода в разбавленном растворе серебра с концентрацией CAg+ моль/л используется формула…
1)
![]()
9) Для защиты медных изделий от коррозии в качестве катодного покрытия можно использовать…
Ag
10) При частичном восстановлении Сr2O3 образуется…
СrO
11) Если при электролизе водного раствора соли значение рН в катодном пространстве возросло, то электролизу подвергался раствор…
KCl
12) Эквивалент перманганата калия, если ион MnO4- восстанавливается до Mn+2,равен___ моль
1/5
13) При электролизе раствора, содержащего одинаковые концентрации солей, на катоде в первую очередь будет выделятся…
железо
14) В реакции 3Ca + 2PCa3P2 атомы фосфора выступают в качестве…
3) окислителей
