
3 курс / Патофизиология / Учебник Литвицкий 4 издание
.pdf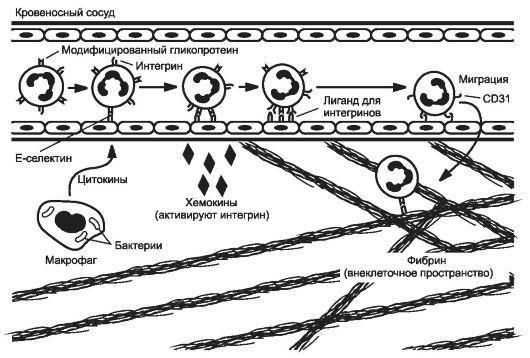
Рис. 5-1. Этапы миграции лейкоцитов через сосудистую стенку (на примере нейтрофилов). [по
4].
Позднее значительная часть лейкоцитов, мигрировавших в очаг воспаления, подвергается дистрофическим изменениям и превращается в «гнойные тельца» или подвергается апоптозу. Часть лейкоцитов, выполнив свои функции, возвращается в сосудистое русло и циркулирует в крови.
При значительном повышении проницаемости стенок сосудов микроциркуляторного русла в очаг воспаления «пассивно» выходят также эритроциты и тромбоциты.
ФАГОЦИТОЗ
Фагоцитоз (греч. phagein - поедать, пожирать + греч. kytos - клетка + греч. osis - процесс, состояние) - активный биологический процесс, заключающийся в распознавании, поглощении и внутриклеточной деструкции чужеродного материала специализированными клетками - фагоцитами: микрофагами (полиморфноядерными лейкоцитами) и макрофагами.
В ходе фагоцитоза выделяют несколько основных стадий (рис. 5-2).

Рис. 5-2.
Стадии фагоцитоза: 1 - адгезия частицы (например, бактерии) с помощью Fc-рецептора мембраны фагоцита; 2 - погружение адгезированной частицы в фагоцит и образование фагосомы; 3 - приближение и присоединение к фагосоме лизосом; 4 - слияние мембран фагосомы и лизосом с образованием фаголизосомы; 5 - разрушение поглощѐнной частицы. [по 4].
• Распознавание фагоцитом объекта поглощения и адгезия к нему происходит в несколько этапов:
♦Обнаружение поверхностных детерминант объекта фагоцитоза.
♦Опсонизация объекта фагоцитоза.
♦Адгезия фагоцита к объекту фагоцитоза. Этот процесс реализуется с участием рецепторов лейкоцита FcyR (при наличии у объекта соответствующего лиганда) и молекул адгезии (при отсутствии лиганда, например, у неклеточных частиц).
• Поглощение объекта фагоцитом с последующим образованием фаголизосомы. Поглощенный материал погружается в клетку в составе фагосомы - пузырька, образованного плазматической мембраной. К фагосоме приближаются лизосомы, мембраны фагосомы и лизосом сливаются, и образуется фаголизосома.
• Внутриклеточное разрушение объекта фагоцитоза реализуется в результате активации двух сложных механизмов: кислородзависимой и кислороднезависимой цитотоксичности фагоцитов.
♦Кислородзависимая цитотоксичность играет ведущую роль в деструкции объекта фагоцитоза. Она сопряжена со значительным повышением интенсивности метаболизма с участием кислорода (респираторный взрыв).
♦Кислороднезависимые механизмы обусловлены действием лизосомальных ферментов фагоцита.
Незавершѐнный фагоцитоз. При незавершѐнном фагоцитозе поглощѐнные фагоцитами микроорганизмы не разрушаются. Это способствует персистенции и распространению инфекции в организме. Причины незавершѐнного фагоцитоза:
•Мембрано- и ферментопатии лизосом фагоцита.
•Повышенная резистентность микробов к ферментам фагоцита.
•Способность некоторых микробов быстро покидать фагосомы и персистировать в цитоплазме фагоцита (риккетсии, хламидии).
•Недостаточный эффект гормонов - регуляторов процесса фагоцитоза.
ПРОЛИФЕРАЦИЯ
Пролиферация - важный компонент механизма развития воспалительного процесса и завершающая его стадия - характеризуется увеличением числа стромальных и паренхиматозных клеток, а также образованием межклеточного вещества в очаге воспаления. Эти процессы направлены на регенерацию или замещение разрушенных тканевых элементов.
♦При благоприятном течении воспаления наблюдается полная регенерация ткани - восполнение еѐ погибших и восстановление обратимо повреждѐнных структурных элементов (реституция).
♦При значительном разрушении участка ткани или органа на месте дефекта паренхиматозных клеток образуется вначале грануляционная ткань, а по мере еѐ созревания - рубец, т.е. наблюдается неполная регенерация.
Неспецифическое и специфическое воспаление
Неспецифическое воспаление не имеет специфических черт и может вызываться различными флогогенными агентами.Специфическое воспаление имеет, наряду с общими, специфические черты и вызывается определѐнным возбудителем. Выделяют
несколько специфических воспалительных заболеваний: туберкулѐз, сифилис, лепра, склерома и др.
ОСТРОЕ И ХРОНИЧЕСКОЕ ВОСПАЛЕНИЕ
По течению различают острое и хроническое воспаление.
Острое воспаление
Острое воспаление характеризуется:
•Интенсивным течением и завершением воспаления, как правило, в течение одной или двух недель.
•Наиболее часто в очаге воспаления преобладают процессы экссудации, и такое воспаление называют «экссудативным».
ЭКССУДАТИВНОЕ ВОСПАЛЕНИЕ
Экссудативное воспаление характеризуется образованием экссудата, состав которого определяется, главным образом, причиной воспаления и реакцией организма на повреждение.
•Серозное воспаление характеризуется формированием мутного экссудата, который содержит небольшое количество лейкоцитов, слущенных эпителиальных клеток и до 2- 2,5% белка. Примеры: воспаление при крапивнице или пузырчатке.
•Фибринозное воспаление характеризуется образованием экссудата, содержащего, помимо лейкоцитов, большое количество фибриногена, который выпадает в тканях в виде нитей фибрина. Фибринозный экссудат пропитывает погибшие ткани, образуя светло-серую плѐнку. В зависимости от структуры эпителиальных покровов и особенностей подлежащей соединительной ткани выделяют два вида фибринозного воспаления:
♦Крупозное воспаление. На однослойном эпителиальном покрове и плотной базальной мембране образуется тонкая, легко снимающаяся фибринозная плѐнка. Такое фибринозное воспаление называется крупозным. Оно встречается на слизистых оболочках трахеи и бронхов, серозных оболочках.
♦Дифтеритическое воспаление. Многослойный плоский неороговевающий эпителий, переходный эпителий и рыхлая широкая соединительнотканная основа органа способствуют развитию глубокого некроза и формированию толстой, трудно снимающейся фибринозной плѐнки, после удаления которой остаются глубокие язвы. Такое фибринозное воспаление называется дифтеритическим. Оно развивается в зеве,
на слизистых оболочках пищевода, матки и влагалища, кишечника и желудка, мочевого пузыря.
• Гнойное воспаление характеризуется образованием гнойного экссудата. Он представляет собой сливкообразную массу, состоящую из детрита, погибших форменных элементов крови (от 17% до 29%),
микробов. Гной имеет специфический запах, синевато-зеленоватую окраску с различными оттенками, содержание белка в нѐм составляет 3-7% и более. Основными формами гнойного воспаления являются абсцесс, флегмона, эмпиема, гнойная рана.
♦Абсцесс - отграниченное гнойное воспаление с образованием полости, заполненной гнойным экссудатом.
♦Флегмона - разлитое гнойное воспаление, при котором экссудат пропитывает и расслаивает ткани.
♦Эмпиема - очаговое гнойное воспаление полостей тела или полых органов.
♦Гнойная рана - возникает либо вследствие нагноения травматической раны, либо в результате вскрытия во внешнюю среду очага гнойного воспаления и образования раневой поверхности.
•Гнилостное воспаление (ихорозное) характеризуется выраженным некрозом тканей.
•Геморрагическое воспаление сопровождается особенно высокой проницаемостью сосудов микроциркуляторного русла, диапедезом эритроцитов и их примесью к уже имеющемуся экссудату (серозногеморрагическое, гнойно-геморрагическое воспаление).
•Катаральное воспаление характеризуется примесью слизи к любому экссудату.
ПРИЗНАКИ ОСТРОГО ВОСПАЛЕНИЯ
Признаки острого воспаления подразделяют на местные и общие (системные).
• Местные признаки острого воспаления. В очаге острого воспаления наблюдаются: покраснение - rubor; припухлость - tumor;
♦ боль - dolor; жар (повышение температуры в очаге воспаления) - calor; нарушение функции - functio laesa.
• Системные изменения при остром воспалении. Вследствие резорбции из очага воспаления в кровь медиаторов воспаления и продуктов распада ткани развивается ряд системных эффектов: лейкоцитоз, лихорадка, диспротеинемия, увеличение скорости оседания эритроцитов, изменение гормонального статуса организма, аллергизация организма.

Таким образом, воспаление, являясь местным процессом, отражает общую, системную реакцию организма на действие флогогенного агента.
Хроническое воспаление
Хроническое воспаление может быть первичным и вторичным.
•Если воспаление после острого периода приобретает затяжной характер, то оно обозначается как «вторично хроническое».
•Если воспаление изначально имеет персистирующее (вялое и длительное) течение, его называют «первично хроническим».
Проявления хронического воспаления. Для хронического воспаления характерен ряд признаков: развитие гранулѐм, формирование капсул, некроз, инфильтрация ткани моноцитами и лимфоцитами. Активация макрофагов иммунными и неиммунными факторами (рис. 5-3) обусловливает дополнительное повреждение тканей и развитие фиброза. При хроническом воспалении часто преобладает процесс пролиферации, и такое воспаление называют пролиферативным.Причины хронического воспаления многообразны:
•Различные формы фагоцитарной недостаточности.
•Длительный стресс и другие состояния, сопровождающиеся повышенной концентрацией в крови катехоламинов и глюкокортикоидов. Указанные группы гормонов подавляют процессы пролиферации, созревания фагоцитов, потенцируют их разрушение.
Рис. 5-3.
Роль активированных макрофагов в развитии и течении хронического

воспаления. Активированные макрофаги синтезируют арахидоновую кислоту, тромбоцитарные факторы роста и другие медиаторы воспаления, потенцирующие вторичную альтерацию. В развитии повреждения тканей принимают участие токсические метаболиты кислорода, протеазы, факторы хемотаксиса нейтрофилов, факторы свѐртывания, метаболиты арахидоновой кислоты и оксид азота. Для развития неиммунной активации важны эндотоксины, фибронектин, химические медиаторы воспаления. Развитие фиброза зависит от перестройки коллагенов под влиянием разных факторов роста и цитокинов, а также от факторов ангиогенеза. [по 4].
• Взаимодействие лимфоцитов и макрофагов, в избытке инфильтрирующих ткани при хроническом воспалении, с высвобождением большого количества повреждающих медиаторов (рис. 5-4).
Рис. 5-4.
Взаимодействие макрофагов и лимфоцитов при хроническом воспалении. Активированные лимфоциты и макрофаги оказывают влияние друг на
друга, а также выделяют медиаторы воспаления, которые повреждают окружающие клетки. TNF - фактор некроза опухоли. [по 4].
•Повторное повреждение ткани или органа (например, лѐгких компонентами пыли), сопровождающееся образованием чужеродных Аг и развитием иммунопатологических реакций.
•Особенности микроорганизмов (устойчивость к действию факторов системы иммунобиологического надзора организма, мимикрия, образование L-форм).
Принципы терапии воспаления
Этиотропное лечение подразумевает устранение, прекращение, уменьшение силы и длительности действия на ткани и органы флогогенных факторов. С этой целью применяют, например, антибактериальные препараты.
Патогенетическое лечение имеет целью блокирование механизма развития воспаления. При этом воздействия направлены на разрыв звеньев патогенеза воспаления, лежащих в основе, главным образом, процессов альтерации и экссудации. Для этого используют, например,
антигистаминные препараты, глюкокортикоиды, ингибиторы циклооксигеназ.
Саногенетическая терапия направлена на активацию общих и местных механизмов компенсации, регенерации, защиты, восстановления и устранения изменений в тканях и клетках, вызванных флогогенным агентом.
Симптоматическое лечение. Мероприятия, направленные на предупреждение или устранение неприятных, тягостных, усугубляющих состояние пациента симптомов (с этой целью применяют, например, анестезирующие ЛС, вещества, способствующие нормализации функций органов и физиологических систем).
ГЛАВА 6. НАРУШЕНИЯ ТЕПЛОВОГО ОБМЕНА
При нарушении теплового баланса организма развиваются либо гипертермические, либо гипотермические состояния. Гипертермические состояния характеризуются повышением, а гипотермические - понижением температуры тела выше и ниже нормы, соответственно.
ГИПЕРТЕРМИЧЕСКИЕ СОСТОЯНИЯ
К гипертермическим состояниям относятся перегревание организма (или собственно гипертермия), тепловой удар, солнечный удар, лихорадка, различные гипертермические реакции.
Собственно гипертермия
Гипертермия - типовая форма расстройства теплового обмена, возникающая в результате, как правило, действия высокой температуры окружающей среды и нарушения теплоотдачи.
ЭТИОЛОГИЯ Причины гипертермии
Выделяют внешние и внутренние причины.
• Высокая температура окружающей среды может воздействовать на организм:
♦в жаркое летнее время;
♦в производственных условиях (на металлургических и литейных заводах, при стекло- и сталеварении);
♦при ликвидации пожаров;
♦при длительном нахождении в горячей бане.
• Снижение теплоотдачи является следствием:
♦первичного расстройства системы терморегуляции (например, при повреждении соответствующих структур гипоталамуса);
♦нарушения отдачи тепла в окружающую среду (например, у тучных людей, при снижении влагопроницаемости одежды, высокой влажности воздуха).
Факторы риска
♦Воздействия, повышающие теплопродукцию (интенсивная мышечная работа).
♦Возраст (легче развивается гипертермия у детей и стариков, у которых понижена эффективность системы терморегуляции).
♦Некоторые заболевания (гипертоническая болезнь, сердечная недостаточность, эндокринопатии, гипертиреоз, ожирение, вегетососудистая дистония).
♦Разобщение процессов окисления и фосфорилирования в митохондриях клеток посредством экзогенных (2,4-динитрофенол, дикумарол, олигомицин, амитал) и эндогенных агентов (избыток тиреоидных гормонов, катехоламинов, прогестерона, ВЖК и митохондриальные разобщители - термогенины).
ПАТОГЕНЕЗ ГИПЕРТЕРМИИ
При действии гипертермического фактора в организме включается триада экстренных адаптивных механизмов: 1) поведенческой реакции («уход» от действия теплового фактора); 2) интенсификации теплоотдачи и снижение теплопродукции; 3) стресса. Недостаточность защитных механизмов сопровождается перенапряжением и срывом системы терморегуляции с формированием гипертермии.
В ходе развития гипертермии выделяют две основные стадии: компенсации (адаптации) и декомпенсации (дезадаптации) механизмов терморегуляции организма. Отдельные авторы выделяют финальную стадию гипертермии - гипертермическую кому. Стадия компенсации характеризуется активацией экстренных механизмов адаптации к перегреванию. Эти механизмы направлены на увеличение теплоотдачи и снижение теплопродукции. За счѐт этого температура тела остаѐтся в пределах верхней границы нормального диапазона. Наблюдаются ощущение жара, головокружение, шум в ушах, мелькание «мушек» и потемнение в глазах. Может развиваться тепловой неврастенический синдром, характеризующийся падением работоспособности, вялостью, слабостью и апатией, сонливостью, гиподинамией, нарушениями сна, раздражительностью, головными болями.
Стадия декомпенсации
Стадия декомпенсации характеризуется срывом и неэффективностью как центральных, так и местных механизмов терморегуляции, что и приводит к нарушению температурного гомеостаза организма. Температура внутренней среды повышается до 41-43 °C, что сопровождается изменениями метаболизма и функций органов и их систем.
♦Потоотделение уменьшается, нередко отмечается лишь скудный липкий пот; кожа становится сухой и горячей. Сухость кожи считают важным признаком декомпенсации гипертермии.
♦Нарастает гипогидратация. Организм теряет большое количество жидкости в результате повышенного потоотделения и мочеобразования на стадии компенсации, что приводит к гипогидратации организма. Потеря 9-10% жидкости сочетается с существенными расстройствами жизнедеятельности. Это состояние обозначают как «синдром пустынной болезни».
♦Развивается гипертермический кардиоваскулярный синдром: нарастает тахикардия, снижается сердечный выброс, МОК поддерживается за счѐт увеличенной ЧСС, систолическое АД может ненадолго возрастать, а диастолическое АД снижается; развиваются расстройства микроциркуляции.
♦Нарастают признаки истощения механизмов стресса и лежащие в основе этого надпочечниковая и тиреоидная недостаточность: наблюдаются гиподинамия, мышечная слабость, снижение сократительной функции миокарда, развитие гипотензии, вплоть до коллапса.
♦Изменяются реологические свойства крови: повышается еѐ вязкость, появляются признаки сладж-синдрома, диссеминированного внутрисосудистого свѐртывания белков крови (ДВС-синдрома) и фибринолиза.
♦Развиваются метаболические и физико-химические расстройства: теряются Cl-, K+, Ca2+, Na+, Mg2+ и другие ионы; из организма выводятся водорастворимые витамины.
♦Регистрируется ацидоз. В связи с нарастанием ацидоза увеличивается вентиляция лѐгких и выделение углекислоты; повышается потребление кислорода; снижается диссоциация HbO2.
♦Увеличивается концентрация в плазме крови так называемых молекул средней массы (от 500 до 5 000 Да) - олигосахаридов, полиаминов, пептидов, нуклеотидов, глико- и нуклеопротеинов. Указанные соединения обладают высокой цитотоксичностью.
♦Появляются белки теплового шока.
♦Существенно модифицируется физико-химическое состояние липидов. Активируется СПОЛ, увеличивается текучесть мембранных липидов, что нарушает функциональные свойства мембран.
