
- •Глава1. История развития биоорганической химии …………………………………
- •Глава 2. Лекции по биоорганической химии …………………………………………
- •Глава 1
- •1.. Характеристика химических связей в биоорганических соединениях
- •2. Сопряженные системы
- •2.1. Общие понятия о строении сопряженных систем
- •Ациклические сопряженные системы. Особенности электронного строения
- •2 . 3 . Циклические сопряженные системы. Ароматичность
- •2. 3. 2. Медико-биологическое значение карбоциклических ароматических
- •2. 3. 3. Гетероциклические ароматические соединения
- •Медико- биологическое значение гетероциклических ароматических соединений
- •2.1. Взаимное влияние атомов в молекулах биоорганических соединений.
- •2.2. Кислотно-основные свойства органических соединений
- •Электроотрицательности атома, несущего неподеленную пару электронов.
- •Влияние природы заместителя
- •2.3. Медико- биологическое значение изучения темы « Кислотно-основные
- •3.1. Виды изомерии
- •3.2. Структурная изомерия.
- •3.2.1. Изомерия скелета
- •3.3. Динамическая изомерия.
- •3. 3.1. Кето-енольная таутомерия.
- •3.3.2. Лактим-лактамная таутомерия
- •3.4 Пространственная изомерия
- •3.4.1 Геометрическая( цис, транс) изомерия
- •Оптическая ( зеркальная) изомерия
- •Пространственное строение шестичленных циклов
- •3.4.4. Медико-биологическое значение стереоизомерии
- •4.1 Классификация реакций в биоорганической химии
- •4.1.1 Типы разрыва химических связей
- •4.1.2. Гомолитический тип разрыва связей.
- •4.1.3. Гетеролитический тип разрыва связей
- •Механизмы биоорганических реакций
- •4.2.1. Реакции электрофильного присоединения в ряду алкенов(а е)
- •4.2.2. Реакции нуклеофильного присоединения
- •Образование полуацеталей и ацеталей
- •Присоединение натрия гидросульфита
- •7. Реакции у α- углеродного атома в карбонильных соединениях
- •8. Альдольная конденсация
- •1. Реакция нитрования
- •2. Реация сульфирования
- •3. Реакция галогенирования
- •4. Реакция алкилирования
- •4.2.4. Реакции нуклеофильного замещения ( s n )
- •Окислительно-восстановительные реакции ( оксидо-редуктазные)
- •Лекция 5 карбоновые кислоты и их гетерофункциональные
- •5.1. Классификация карбоновых кислот
- •5.2. Строение карбоксильной группы
- •5.2.1. Значение величин рКа некоторых карбоновых кислот :
- •5.3. Химические свойства карбоновых кислот
- •Этилацетат
- •5.4. Характеристика отдельных представителей монокарбоновых кислот ,
- •Масляная кислота ( н- бутановая кислота)
- •5.5. Непредельные монокарбоновые кислоты
- •5.6. Дикарбоновые кислоты
- •5.7. Непредельные ди- и трикарбоновые кислоты
- •5.8. Гидроксикислоты
- •5.8.3. Дигидроксидикарбоновые кислоты
- •5.9. Oксокарбоновые кислоты( альдегидо -, кетокарбоновые кислоты)
- •5.10 Приложение : Происхождение названий карбоновых кислот Сn н2n о2
- •6.1. Определение « липиды»
- •Классификация липидов
- •6.3. Основные представители липидов
- •6.3.1. Природные высшие карбоновые кислоты
- •Образование соли
- •3. Тиоэфиры
- •4. Дегидрирование насыщенной кислоты в активной форме с участием фермента.
- •6.3.2. Триацилглицерины( триглицериды)
- •6.3.3. Фосфатиды ( фосфолипиды ) и фосфатидовая кислота
- •Холестерин( холестерол) и его производные
- •6. 4. Принципы создания липотропных лекарственных препаратов
- •6.5 . Строение и химический состав мембран клеток
- •7.1. Номенклатура, особенности пространственного и структурного строения природных аминокислот
- •7. 2 Классификация природных аминокислот
- •7. 3 Физические свойства природных аминокислот
- •7.4 Поведение аминокислот в водных растворах: образование цвиттер-ионов, изменение заряда и электрофоретической подвижности в зависимости от рН-среды. Изоэлектрическая точка
- •7.5. Качественная реакция обнаружения аминокислот
- •7. 6 . Химические свойства аминокислот
- •7 .6. 1 Химические свойства аминокислот in vitro
- •7.6.2. Химические свойства аминокислот in vivo
- •7.7. Строение витамина в6 и механизм реакции с его участием
- •7.8. Реакция поликонденсации, образование полипептидов
- •7. 9. Медико - биологическое значение аминокислот
- •7. 10. Применение аминокислот и их производных в качестве
- •Незаменимые аминокислоты обозначены звездочкой*
- •8.1. Определения « пептид» «белок»
- •8.2. Классификация белков
- •8.3. Строение пептидов и белков.
- •8.3.1. Первичная структура белка
- •8.3.2. Вторичная структура белка
- •8.3.3. Третичная и четвертичная структура белка
- •8.4. Физико-химические свойства белка
- •8.4.1. Амфотерность - кислотно- основные свойства белков.
- •8.4.2. Денатурация белка
- •8.5. Качественные реакции обнаружения белков в биологических объектах.
- •8. 6. Приложение. История развития химии белков
- •9. 1. Классификация углеводов
- •9.2. Моносахариды
- •9.3. Изомерия моносахаридов. Стереоизомерия. L- и д- ряды. Диастереомеры, энантиомеры, эпимеры. Значение отдельных представителей
- •9.4 Химические свойства моносахаридов
- •9.4. 3. Фосфорные эфиры
- •9.4.3 Образование гликозидов
- •9.4.4. Реакции восстановления
- •9.4.5 Реакции окисления моносахаридов
- •9.5. Биологическое значение моносахаридов и их производных.
- •10.1. Олигосахариды. Дисахариды
- •10.1.1. Нередуцирующие дисахариды
- •10.1.2 Редуцирующие дисахариды.
- •10.2. Полисахариды
- •10.2.1. Гомополисахариды
- •11.1. Классификация нуклеиновых кислот, отличия в строении и составе как следствие различных биологических функций
- •11.2. Азотистые основания нуклеиновых кислот
- •Азотистые т основания- производные пиримидина
- •11.2.2. Азотистые основания- производные пурина( аденин, гуанин)
- •11.3. Нуклеозиды
- •11.4. Нуклеотиды
- •11.5. Строение нуклеиновых кислот
- •11.6. Метаболизм пуриновых соединений в клетке
- •11.7. Биологически важные соединения- мононуклеотиды, динуклеотиды- участники важнейших биохимических процессов
- •11.8 Приложение . Справочные материалы к теме лекции
- •1953 – Дж. Уотсон и ф. Крик - модель двухцепочечной структуры днк.
- •12.1 Современная концепция создания биоорганических соединений –
- •12.1.1. Особые химические требования к лекарственному веществу
- •12.1.3. . Пути поиска и создания лекарственных препаратов
- •12.1.4 Классификация лекарственных веществ
- •12.2 Синтез, химические и физические свойства лекарственных соединений
- •12.2.1. Производные 4-аминобензойной кислоты
- •12.2.2. Производные 4-аминобензолсульфокислоты
- •Hso3Cl сульфохлорирование h2nr’ амин AcHn — с6н 5 AcHn — с6н 4— so2Cl ацетиланилин
- •12. 2. 3. Лекарственные средства, производные салициловой кислоты
- •12.2.4. Лекарственные средства, производные 4 –аминофенола
- •12.2.5 Лекарственные средства на основе пиридинкарбоновых кислот
- •12. 2. 6. Производные пиримидина
- •12. 2 .7. Производные пурина- кофеин, теофиллин, теобромин
- •13.1. Номенклатура алкалоидов
- •13.2. Классификация алкалоидов
- •13. 3. Функции алкалоидов
- •13.4. Содержание в растениях
- •13.5. Качественные реакции обнаружения алкалоидов
- •13.6. Фармакологическая активность- общий взгляд
- •13.7. Отдельные представители
- •13. 7.1. Алкалоиды группы фенилэтиламина
- •7.2 Производные пяти – и шестичленных гетероциклических соединений
- •137.3. Группа тропана
- •13.8. Витамины
- •Действие в организме
- •Стадии зрительного процесса на сетчатке глаза
- •14.1. Полимеры-определение. Виды полимеров
- •14. 2. Классификация вмс
- •14.3. Реакции полимеризации
- •14.3.1. Номенклатура полимеров.
- •14.3.2 . Общая характеристика мономеров.
- •14.3.3. Механизмы реакции полимеризации
- •14.4. Радикальная полимеризация
- •14.5. Ионная полимеризация
- •14.5.1. Катионная полимеризация
- •14.5.2. Анионная полимеризация
- •14.6. Координационная полимеризация
- •14.7.1. Блочная полимеризация
- •14.7.2. Эмульсионная полимеризация
- •14.7.3. Полимеризация в растворе
- •14.8. Конфигурация полимеров
- •14. 10. Физическое состояние полимеров
- •14.10.1. Аморфные полимеры
- •14 10.2. Кристаллические полимеры
- •14.11. Натуральный каучук
- •14.12 . Конденсационные полимеры
- •14. 13 Основные представители вмс
- •2. Структурные формулы биоорганических соединений
- •Сопряженные соединения
- •Карбоновые кислоты (указаны тривиальные названия)
- •Незаменимые аминокислоты обозначены звездочкой -*
- •Углеводы и их производные
- •Азотистые основания и их производные
- •1. Теоретические положения строения и свойств биоорганических
- •2. Важнейшие биополимеры организма
- •3. Липиды и низкомолекулярные регуляторы метаболизма.Важнейшие группы лекарственных средств
- •Курс лекций по биоорганической химии
- •060103 – Педиатрия
- •060104 –Медико-профилактическое дело
- •060105 - Стоматология
4. Реакция алкилирования
Самый простой метод – алкилирование по Фриделю- Крафтсу алкилгалогенидом в присутствии хлорида алюминия.
R—>C1 + A1C13 <=> R—>C1… A1C13 <=> R+ [ A1C14 ] –
С6 Н6 + R+ [ A1C14 ] – –———> С6 Н5 – R + НС1 + A1C13
Алкилбензол
В реакциях in vivo переносчиком активной метильной группы ( карбокатиона СН3+) являются витамины В12 и фолиевая кислота , а источником активного одноуглеродного карбокатиона СН 3 служат аминокислоты метионин или серин. Реакция чрезвычайно важна в синтезе тимина из урацила.
5. Реакция карбоксилирования
Возможна для ароматических соединений, активированных заместителями с сильным + М эффектом, например, в синтезе салициловой кислоты, взаимодействие расплава фенолята натрия с СО 2 ( см лекцию «Лекарственные препараты»).
Механизм реакции электрофильного замещения
Этапы реакции:
-
Приближение электрофила к ароматической делокализованной системе электронов
-
Электрофил ориентируется перпендикулярно к бензольному кольцу , образует пи-комплекс
-
Электрофил «забирает» два электрона из пи-электронной системы и образует сигма- комплекс, в котором остается 4 электрона на 5 атомов углерода( возникает рассредоточенный положительный заряд). Пять атомов углерода имеют sp2 –гибридное состояние., а один атом , связанный с заместителем и атомом водорода, в состоянии sp3
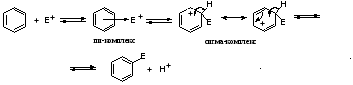 4.
Чтобы вновь вернуть единую пи-электронную
систему, надо в нее вернуть два электрона.
Происходит « выброс» протона и два
электрона возвращаются в общий
ароматический секстет.
4.
Чтобы вновь вернуть единую пи-электронную
систему, надо в нее вернуть два электрона.
Происходит « выброс» протона и два
электрона возвращаются в общий
ароматический секстет.
4.2.4. Реакции нуклеофильного замещения ( s n )
Реакции нуклеофильного замещения заключаются в вытеснении нуклеофильной частицы, связанной с атомом углерода, другой нуклеофильной частицей.
В общем виде можно представить:
У – + R –> X <==> R –> У + X–
|
б+ б- б- | б+
У – + – C –> Х <==> У <– C – + Х –
нуклеофил(1) | | нуклеофил(2)
приходящая уходящая группа
группа
Нуклеофил должен иметь доступную электронную пару ( это может быть анион или молекула, в которой есть атом с неподеленной парой электронов) и атаковать другую молекулу по электрофильному центру, замещая имеющуюся нуклеофильную группу.
Наиболее распространенными in vitro являются превращения :
А. Обратимая реакция: спирт – галогенопроизводное / галогенопроизводное –спирт
R-OH + Н Hal <==> R- Hal + Н2 О
Б. Галогенопроизводное - цианопроизводное
R- Hal + Н- CN ——> R- CN + ННа1
В. Галогенопроизводное - амин
R- Hal + N H3 ——> R- N H2 + НС1
Г. Этерификация ( карбоновая кислота- сложный эфир )
R COOH + R1 ОН <==> R COOR1 + Н2 О
Д. Переэтерификация ( сложный эфир - другой сложный эфир )
R COOR1 + R2 ОН <==> R COOR2 + R1 ОН
Е. Амидирование ( сложный эфир - амид )
R COOR1 + N H3 <==> R CO N H2 + R1 ОН
Ж. Гидролиз ( сложный эфир – кислота, амид - кислота)
R COOR1 + Н2 О <==> R COOH + R1 ОН
R CO N H2 + Н2 О <==> R COOH + N H3
З . Образование ангидрида
R COOH + R COOH <==> R C- O- С R + Н2 О
| | | |
О О
В биохимических процессах in vivo встречаются реакции ( Д – З ).
Выделяют реакции SN 1 и SN 2, которые различаются между собой образованием переходных состояний , и , вследствие этого, могут сопровождаться изомерными отличиями в пространственном строении продуктов реакции.
Реакция S N 2.- бимолекулярная
В образовании переходного состояния участвуют оба нуклеофила : « приходящий и уходящий». Процесс присоединения одного и удаления другого – синхронный: один нуклеофил с противоположной стороны подходит, а другой уходит. Если атом углерода в электрофильном центре , у которого происходит замещение, был оптически активным, то обязательно изменяется пространственное строение – смена одного стереоряда на другой.


| б+ б- + |
У – + –- C –> Х <==> У – … >С– … Х– <==> У – С – + Х –
| атом углерода |
атом углерода тригональный плоское атом углерода
тетраэдрический строение тетраэдрический
карбокатион – изменение стереоряда
переходное состояние
Изменение стереоряда носит название «Вальденовское обращение» по имени ученого, впервые обратившего внимание на этот процесс.
Скорость реакции SN 2 зависит от концентрации обоих реагирующих веществ.
V = k [ Y– ] [ RX ]
Заместители- акцепторы оттягивают электронную плотность , увеличивают заряд б + на атоме углерода в электрофильном центре и увеличивают скорость реакции нуклеофильного замещения. Если уходящая группа способна к сольватации растворителем, то это обстоятельство также способствует увеличению скорости реакции. В связи с этим в реакциях in vitro аминогруппа NH2, связанная с атомом углерода в sp3 - крайне редко обменивается нуклеофильно.
Реакция S N 1.- мономолекулярная
Для реакций in vivo характерен механизм нуклеофильного замещения S N 1- мономолекулярный, что связано с участием в реакции катализатора- фермента. Этот же механизм возможен in vitro в случае образования устойчивого промежуточного карбокатиона.
Критерии S N 1:
- концентрация приходящего нуклеофила Y– не влияет на скорость реакции.
- добавление в среду уходящего нуклеофила X– снижает скорость реакции.
Скорость реакции S N 1 зависит от концентрации только RX и стабильности образующегося промежуточного устойчивого карбокатиона.
V = k [ RX ]
Устойчивость карбокатиона увеличивается под влиянием донорных заместителей, снижающих дефицит электронной плотности в реакционном центре .
Увеличение устойчивости карбокатионов :
СН3 + < СН3 СН2 + < ( СН3 )2 СН + < ( СН3 )3 С +
Рассмотрим образование устойчивого промежуточного карбокатиона

| | | |
– Сб+ —>Х б- <==> —С б+ … Хб- <==> — С + . . . Х – <==> ( – С+ ) ( Х –)
| | | |
переходное ионная пара ( карбокатион) ( анион)
состояние сольватированные
ионы
Карбокатион имеет плоское строение, атом углерода в sp3 – гибридном состоянии, нуклеофильная частица может атаковать карбокатион с любой стороны плоскости. Если в реакции участвует определенный стереоизомер, то в случае механизма S N 1 возникает рацемизация- образуются два разных стереоизомера ( D и L ) в соотношении 1:1, содержащие новую нуклеофильную частицу.
Ферментативные реакции in vivo проходят по механизму S N 1 , образуется всегда только один стереоизомер, который необходим для осуществления биохимических процессов.
Равновероятная атака нуклеофилом плоского карбокатиона с двух противоположных
сторон в химической реакции in vitro
У–
|
У
– С*–

+ |
> С —
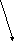
|
– С* –У
|
У–
Пример:
D –бутанол-2 + НС1 ———> Н2 О + 2-хлорбутан ( рацемическая смесь)
L- бутанол-2 + НС1 ———> Н2 О + 2-хлорбутан ( рацемическая смесь)
рацемическая смесь
CН3 СН3
| |
С1 – С – Н Н – С – С1 2-хлорбутан
| |
С2 Н5 С 2 Н 5
энантиомеры , образуют рацемическую смесь в отношении 1:1
К биологически важным процессам нуклеофильного замещения относятся :
А) образование и гидролиз сложных эфиров карбоновых кислот, синтез
триглицеридов-жиров
Б) образование с участием АТФ фосфорных эфиров соединений, содержащих гидроксильные группы
R–ОН + АТФ —> R–О –РО3 Н2 + АДФ
В) образование гликозидных связей между молекулами углеводов или углеводов с веществами других классов( спиртами, аминами, тиолами).
Г) образование полимеров аминокислот- полипептидов и белков.
Д) образование вторичных, третичных, четвертичных аминов, что особенно важно в синтезе адреналина, холина, кофермента НАД+.

б-
б + б
- 
R —NH2 + CН3 —Х ———> R —NH—CН3 + H — Х
первичный амин полярная связь вторичный амин
Аминогруппа , содержащая неподеленную пару электронов, несет отрицательный заряд
б- , и нуклеофильно замещает ион галогенида, который является уходящей группой.
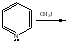
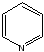
Модельной реакцией синтеза динуклеотида НАД+ может служить образование катиона метилпиридиния . В процессе метилирования пиридина йодометаном образуется соль метилпиридиний йодид
| +
СН3
4.2.5. Реакции элиминирования ( E )
Реакции элиминирования in vitro имеют самостоятельное значение, но и часто конкурируют с реакциями нуклеофильного замещения( происходят одновременно). Представляют собой распространенный способ образования двойной связи. Элиминирование воды из спиртов проходит при нагревании спирта с конц. серной кислотой при температуре выше 1400. В случае вторичных или третичных спиртов реакция идет по правилу Попова( упрощенно - двойная связь располагается внутри цепи)
Механизм реакции элиминирования связан с образованием промежуточного карбокатиона с более устойчивой сопряженной системой.
Н2 S О4 конц t >140
СН3 – СН2 –ОН ———————> СН2 =СН2 + НОН
этанол этен
Н2 S О4 конц t >140
CН3 – СН2 – СН – СН3 ———————> CН3 – СН = СН – СН3 + НОН
|
ОН
бутанол-2 бутен-2
Элиминирование галогеноводорода происходит под влиянием спиртового раствора щелочи( КОН или NаОН )
спирт. р-р
СН3 – СН2 –С1 + КОН ———————> СН2 =СН2 + КС1 + НОН
этанол этен
4 3 2 1 КОН спирт. р-р
СН3 – СН – СН2 –СООН ———————> СН 3 – СН =СН – СООН (А)
|
С1 2- бутеновая( кротоновая) кислота
3-хлорбутановая кислота сопряженная система
СН 2 = СН– СН – СООН (В)
3- бутеновая кислота
нет сопряженной системы
В реакции элиминирования 3-хлорбутановой кислоты возможно образование двух изомеров ( А) и ( В) .
В молекуле 3-хлорбутановой кислоты атом углерода С-2 представляет собой более сильный СН- кислотный центр по сравнению с атомом С-4, удаление протона происходит от атома С-2, возникает сопряженная система. В молекуле 3-бутеновой кислоты отсутствует сопряженная система.
Ферментативные реакции элиминирования in vivo имеют огромное значение в обеспечении множества метаболических процессов( реакции цикла Кребса, синтез и окисление высших жирных кислот). Эти процессы осуществляет особый класс ферментов - лиазы в условиях кислотного катализа при строгом контроле стереоизомерии ( образуется только цис- или только транс- форма )
Наиболее важные биохимические реакции
гидроксилиаза
СН3 – СН – СН2 –СООН < ———————> СН 3 – СН =СН – СООН + НОН
| кротоновая кислота ( транс )
ОН
3-гидроксибутановая кислота (ß– гидроксимасляная)
гидроксилаза
НООС – СН – СН2 –СООН <———————> СН 3 – СН =СН – СООН НОН
|
ОН фумаровая( транс-бутендиовая)
яблочная кислотая (малат)
Механизм реакции элиминирования in vitro .
Н2 S О4 конц t >140 +
СН3 – СН2 – О – Н + Н + ———––—— —––——> СН3 – СН2 – О – Н ——–> НОН +
(1)
| (2)
Н
Нб+ катион гидроксония
| +
Нб+–С –> СН2 —————————> СН2 = СН2 + Н +
| карбокатион ( 3 ) алкен
Нб+
СН-кислотный
центр
Этапы реакции:
1. Среда кислая. В растворе присутствует катион водорода. Происходит протонирование спиртовой гидроксигруппы. Образуется катион гидроксония( используется неподеленная пара электронов атома кислорода)
2. Отщепление молекулы воды. Возникает карбокатион, т.к. пара электронов возвращается для восстановления электронной оболочки атома кислорода( неподеленной пары электронов )в молекуле воды. В соседнем α - положении возникает СН- кислотный центр, атомы водорода приобретают заряды б+ .
3. Карбокатион « выбрасывает» протон Н+ из α - положения , оставшаяся пара электронов связи ( выделена красным цветом) участвует в образовании двойной связи. Катион водорода возвращается в раствор.
Аналогично действует каталитический центр фермента гидролиазы, который участвует в элиминировании воды.
