
Порядок выполнения работы
Опыт №1. Влияние концентрации тиосульфаты натрия на скорость его разложения в кислой среде.
![]()
Табл. 1. Приготовление растворов.
-
№ пробирки
Число капель
Na2S2O3
H2O
H2SO4
Всего
1
4
8
1
13
2
8
4
1
13
3
12
-
1
13
Табл. 2. Результаты опыта.
-
№ пробирки
С(Na2S2O3)
отн. ед.
lnCотн
(Ci/C1)
Время реакции,τ, с
Скорость реакции, с-1
1
1
0
21
4,8 . 10-2
2
2
0,693
7
14,3. 10-2
3
3
1,1
5
20 . 10-2
Найдем значения скорости реакции:
![]()
![]()
![]()
1. График зависимости скорости реакции
от концентрации тиосульфата натрия.
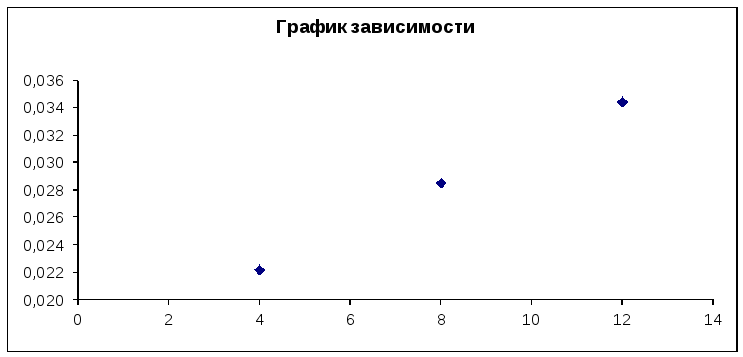
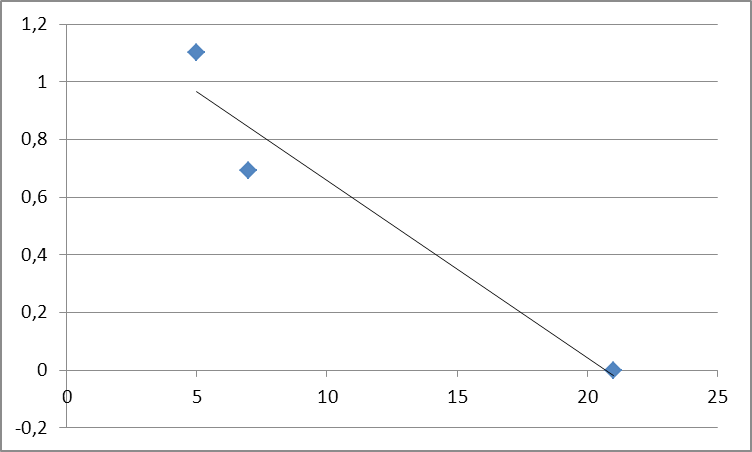
2. График зависимости логарифма
относительной концентрации от
времени протекания реакции.
![]()
![]()
Na2S2O3 + H2SO4 ⇄ Na2SO4 + SO2 + H2O + S¯,
протекает в три стадии:
1. Na2S2O3 + H2SO4 = H2S2O3 +Na2SO4
2. H2S2O3 = H2SO3 + S ¯
3. H2SO3 = SO2 + H2O,
из которых реакции первой и третьей стадий идут практически мгновенно, а реакции второй стадии – медленно. Именно она и определит скорость суммарного процесса, т.е. будет зависеть только от концентрации тиосерной кислоты Н2S2O3, количество которой пропорционально количеству тиосульфата натрия Na2S2O3 при наличии избытка серной кислоты. Таким образом, кинетическое уравнение запишется:
![]()
Вывод: Закон действия масс в нашем опыте подтвердился. При постоянной температуре скорость химической реакции пропорциональна произведению концентрации реагирующих веществ, что видно из графика № 1 «График зависимости скорости реакции
от концентрации тиосульфата натрия».
Опыт №2. Влияние температуры на скорость реакции разложения тиосульфата натрия в кислой среде.
|
№ п/п |
Температура, °С |
Время, , сек. |
|
1 |
23 |
37 |
|
2 |
33 |
15 |
|
3 |
42 |
5 |
Зависимость скорости реакции от температуры
|
№ п/п |
Температура T, K |
Время реакции , сек. |
Скорость реакции v = 1/τ, с−1 |
|
Ea, кДж/моль |
|
1 |
296,15 |
37 |
0,027 |
2,48 |
68,5 |
|
2 |
306,15 |
15 |
0,067 |
||
|
3,37 |
97,4 |
||||
|
3 |
315,15 |
5 |
0,2 |
При обработке результатов эксперимента воспользуемся правилом Вант-Гоффа:
При увеличении температуры на 10 K скорость химических реакций возрастает в 2 – 4 раза
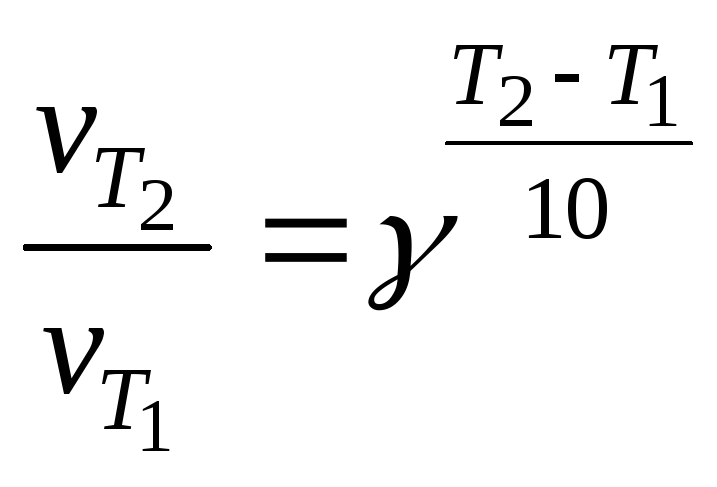 ,
,
где γ – температурный коэффициент скорости реакции.
γ1= 0,067/ 0,027= 2,48
γ2=
![]() =3,37
=3,37
γср= (2,48+3,37) /2= 2,925
Путем проведения опыта было подтверждено эмпирическое правило Вант-Гоффа, только с незначительной погрешностью.
Теперь вычислим энергию активации реакции:
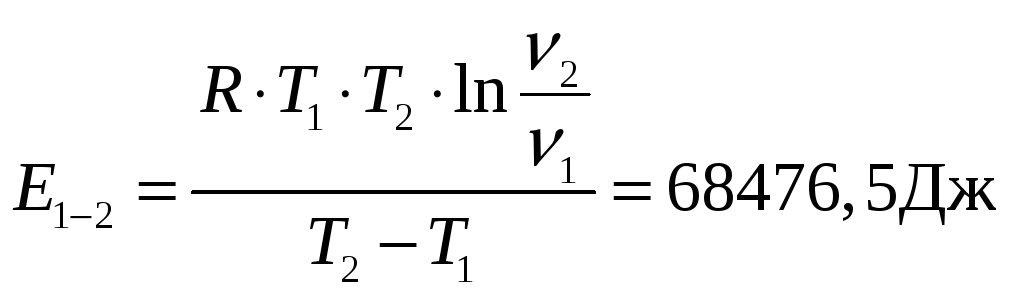
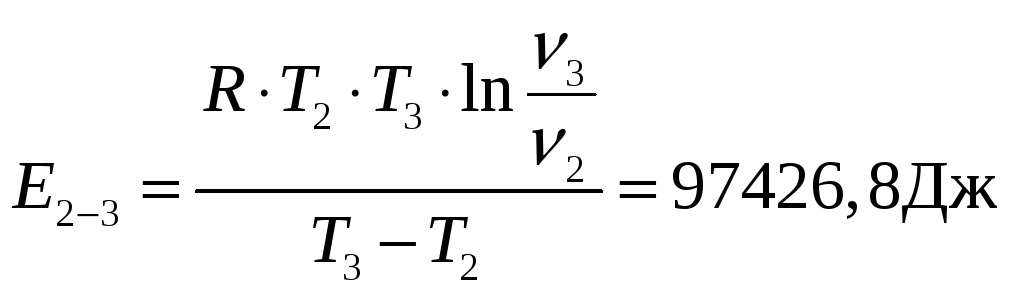
где R = 8,31 Дж/моль.K,
T – температура в K,
![]() i = скорость
химической реакции.
i = скорость
химической реакции.
Вывод: Правило Вант-Гоффа в нашем опыте подтвердилось. Исходя из полученных значений температурного коэффициента (2,48; 3,75) мы можем сделать вывод : с повышением температуры скорость реакций увеличивается в 2-4 раза.
Опыт №5. Влияние концентраций реагентов на равновесие обратимой реакции между хлоридом железа (III) и тиоцианатом аммония.
FeCl3 + 3NH4CNS = Fe(CNS)3 + 3NH4Cl
Налили в химический стаканчик по 5 капель растворов хлорида железа (III) и тиоцианата аммония, перемешали и разлили в 4 пробирки.
-
Без добавок реакция прошла плавно и получился оранжевый раствор.
-
Здесь мы добавили FeCl3 (конц.), раствор окрасился в темно-оранжевый цвет; химическое равновесие сместилось вправо.
-
После добавления NH4CNS (конц.)раствор окрасился в темно-красный цвет; химическое равновесие сместилось вправо.
-
Затем добавили NH4Cl,раствор окрасился в желтоватый цвет, а химическое равновесие сместилось влево.
Зависимость положения равновесия от состава системы
|
№ пробирки |
Состав системы |
Добавленный реактив |
Наблюдения |
|
1 |
5 капель FeCl3 5 капель NH4CNS |
нет |
Получили оранжевый раствор |
|
2 |
FeCl3 |
Темно- оранжевый раствор |
|
|
3 |
NH4CNS |
Темно-красный раствор |
|
|
4 |
NH4Cl |
Желтоватый раствор |
Вывод: При увеличении концентрации реагентов химическое равновесие сместиться вправо.
При увеличении концентрации продуктов реакции, химическое равновесие сместиться влево.
