
- •Содержание
- •Глава I. Исходные данные для выполнения работы. 3
- •Глава II. Практическая часть. 4
- •Глава III. Результаты расчетов. 20
- •Глава IV. Заключение 20
- •Глава I. Исходные данные для выполнения работы.
- •1.1 Состав процессов термодинамических циклов:
- •1.2 Термодинамические параметры в характерных точках:
- •Расчет основных термодинамических параметров в точке 3
- •Расчет основных термодинамических параметров в точке 4
- •П.2.2 Расчет удельного количества теплоты q и удельной работы l в каждом термодинамическом процессе
- •Расчет удельного количества теплоты q и удельной работы l в процессе 1–2
- •Расчет удельного количества теплоты q и удельной работы l в процессе 2–3
- •Расчет удельного количества теплоты q и удельной работы l в процессе 3–4
- •Расчет удельного количества теплоты q и удельной работы l в процессе 4–1
- •Определение внутренней энергии Δu, удельной энтальпии Δh, удельной энтропии Δs в процессе 2-3
- •Определение внутренней энергии Δu, удельной энтальпии Δh, удельной энтропии Δs в процессе 3-4
- •Определение внутренней энергии Δu, удельной энтальпии Δh, удельной энтропии Δs в процессе 4-1
- •Проверка найденных изменений внутренней энергии Δu, удельной энтальпии Δh, удельной энтропии Δs.
- •П.2.4 Расчет величины удельной теплоемкости с и величины показателя политропы n в каждом термодинамическом процессе Расчет удельной теплоемкости с и величины показателя политропы в процессе 1-2
- •Расчет удельной теплоемкости с и величины показателя политропы в процессе 2-3
- •Определение количества работы цикла lc
- •Глава IV. Заключение
- •Список использованной литературы
Расчет удельного количества теплоты q и удельной работы l в процессе 3–4
Определение удельного количества теплоты q в процессе 3-4
Так как процесс 3-4 политропный, то исходя из определения процесса, имеем:
![]()
где Т3 и Т4 – абсолютная температура газа в точках 3 и 4, cn – удельная теплоемкость политропного процесса.
Величины в полученные пункте 2.1 и 2.2 подставляем в выражение , получим:
![]()
![]()
Определение удельной работы l в процессе 3-4
Найденные в пункте 2.1 величины подставляем в выражение , получим:
![]()
![]()
где Т3 и Т4 – абсолютная температура газа в точках 3 и 4, , v3 и v4 – абсолютное давление газа в точках 3 и 4 процесса, n – показатель политропы.
Расчет удельного количества теплоты q и удельной работы l в процессе 4–1
Определение удельного количества теплоты q в процессе 4-1
Найденные в пункте 2.2, и 2.1 величины подставляем в выражение, получим:
![]()
![]()
где сv – удельные теплоемкости при постоянном давлении и объеме
Определение удельной работы l в процессе 4-1
Так как процесс 4-1 изохорный, то исходя из определения процесса, имеем:
![]()
![]()
П.2.3 Расчет изменения удельных величин: внутренней энергии Δu, энтальпии Δh и энтропии Δs в каждом термодинамическом процессе
Определение внутренней энергии Δu, удельной энтальпии Δh, удельной энтропии Δs в процессе 1-2
Определения внутренней энергии Δu в процессе 1-2
Так как процесс 1-2 – политропный, то по определению изменения внутренней энергии, находим:
![]()
![]()
где сv – удельные теплоемкости при постоянном давлении и объеме
Определения удельной энтальпии Δh в процессе 1-2
Так как процесс 1-2 – политропный, то по определению изменения внутренней энергии, находим:
![]()
![]()
где р1 и р2 – абсолютное давление газа в точках 1 и 2 процесса, v1 и v2 – удельный объем газа в точках 1 и 2 процесса.
Определения удельной энтропии Δs в процессе 1-2
Так как процесс 1-2 – политропный, то по определению изменения внутренней энергии, находим:
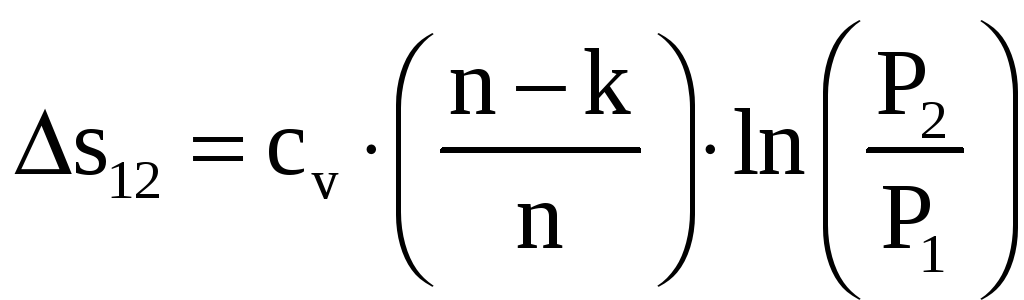
Величины найденные в параграфе 2.1 и заданные в пунктах 1.3 подставляем в , получим:
![]()
![]()
где k – показатель адиабаты (k=1,67 для одноатомных газов), n – показатель политропы.
Определение внутренней энергии Δu, удельной энтальпии Δh, удельной энтропии Δs в процессе 2-3
Определение изменения внутренней энергии Δu в процессе 2-3
Так как процесс 2-3 изотермный, то
![]()
![]()
Определения удельной энтальпии Δh в процессе 2-3
Так как процесс 2-3 изотермный, то
![]()
![]()
Определения удельной энтропии Δs в процессе2-3
Так как процесс 2-3 изотермный, то изменение энтропии находится:

Величины, найденные в параграфах 2.1. и 2.2 значения подставляем в уравнение , получим:
![]()
![]()
где v2 и v3 – удельные объемы газа в 2 и 3 точках процесса
Определение внутренней энергии Δu, удельной энтальпии Δh, удельной энтропии Δs в процессе 3-4
Определения внутренней энергии Δu в процессе 3-4
Так как процесс 3-4 – политропный, то по определению изменения внутренней энергии, находим:
![]()
![]()
где сv – удельные теплоемкости при постоянном давлении и объеме.
Определения удельной энтальпии Δh в процессе 3-4
Так как процесс 3-4 – политропный, то по определению изменения внутренней энергии, находим:
![]()
![]()
где р3 и р4 – абсолютное давление газа в точках 3 и 4 процесса.
Определения удельной энтропии Δs в процессе 3-4
Так как процесс 3-4 – политропный, то по определению изменения внутренней энергии, находим:

Величины найденные в параграфе 2.1 значения и заданные в пунктах 1.3 подставляем в уравнение, получим:
![]()
![]()
где сv – удельные теплоемкости при постоянном давлении и объеме k – показатель адиабаты (k=1,67 для одноатомных газов), n – показатель политропы
