
- •Комплексные соединения
- •Определение комплексных соединений
- •Основные понятия
- •Номенклатура комплексных соединений
- •Одноядерные комплексы
- •Классификация комплексных соединений
- •Катионные комплексы
- •Анионные комплексы
- •Нейтральные комплексы
- •Катионно-анионные комплексы
- •Циклические комплексы (хелаты)
- •Изомерия комплексных соединений
- •Ионизационная изомерия
- •Солевая изомерия
- •Координационная изомерия
- •Геометрическая изомерия (цис-, транс-изомерия)
- •Хлороамминдиэтилен диаминкобальта(III).
- •Природа химической связи в комплексных соединениях Метод валентных связей
- •Теория кристаллического поля
- •Теория поля лигандов
- •Свойства комплексных соединений Окраска комплексных соединений
- •Магнитные свойства комплексных соединений
- •Равновесия в растворах комплексных соединений
- •Устойчивость комплексных соединений
- •Кинетика и механизм реакций обмена лигандов
- •Кислотно - основные свойства комплексных соединений
- •Окислительно-восстановительные свойства комплексных соединений
- •Длины волн спектра и соответствующие им окраски
Классификация комплексных соединений
Комплексные ионы могут входить в состав молекул различных классов химических соединений: кислот, оснований, солей и др. В зависимости от заряда комплексного иона различают катионные, анионные и нейтральные комплексы.
Катионные комплексы
В катионных комплексах центральным атомом-комплексо-образователем являются катионы или положительно поляризованные атомы комплексообразователя, а лигандами - нейтральные молекулы, чаще всего воды и аммиака. Комплексные соединения, в которых лигандом выступает вода, называются аквакомплексами. К таким соединениям относятся кристаллогидраты. Например: MgCl2 6H2O
или [Mg(H2O)6]Cl2,
CuSO4 5H2O или [Cu(H2O)4]∙SO4 ∙ Н2O, FeSO4 7H2O или [Fe(H2O)6]SO4 H2O
В кристаллическом состоянии некоторые аквакомплексы (например, медный купорос) удерживают и кристаллизационную воду, не входящую в состав внутренней сферы, которая связана менее прочно и легко отщепляется при нагревании.
Один из наиболее многочисленных классов комплексных соединений - амминокомплексы (аммиакаты) и аминаты. Лигандами в этих комплексах являются молекулы аммиака или амина. Например: [Cu(NH3)4]SO4, [Pt(NH3)6]Cl4,
[Cd(NH2CH2CH2NH2)3]Cl2.
Анионные комплексы
Лигандами в таких соединениях являются анионы или отрицательно поляризованные атомы и их группировки.
К анионным комплексам относятся:
а) комплексные кислоты H[BF4], H2[SiF6], H[Ag(CN)2].
б) двойные и комплексные соли PtCl4 2KCl или K2[PtCl6],
HgI2·2KI или K2[HgI4].
в) кислородсодержащие кислоты и их соли H2SO4, K2SO4, H5IO6, K2CrO4.
г) гидроксосоли K[Al(OH)4], Na2[Sn(OH)6].
д) полигалогениды: K[I(I)2], Cs[I(I2)4].
Нейтральные комплексы
К подобным соединениям относятся комплексные соединения, не имеющие внешней сферы и не дающие в водных растворах комплексных ионов: [Pt(NH3)2Cl4], [Co(NH3)3(NO2)3], карбонилкомплексы [Fe(CO)5], [W(CO)6].
Катионно-анионные комплексы
Соединения одновременно содержат как комплексный катион, так и комплексный анион:
[Pt(NH3)4][PtCl4], [Ni(NH3)6][Fe(CN)6].
Циклические комплексы (хелаты)
Координационные соединения, в которых центральный атом (или ион) связан одновременно с двумя или более донорными атомами лиганда, в результате чего замыкается один или несколько гетероциклов, называются хелатами. Лиганды, образующие хелатные циклы, называются хелатирующими (хелатообразующими) реагентами. Замыкание хелатного цикла такими лигандами называется хелатированием (хелатообразованием). Наиболее обширный и важный класс хелатов – хелатные комплексы металлов. Способность координировать лиганды присуща металлам всех степеней окисления. У элементов основных подгрупп центральный атом-комплексообразователь обычно находится в высшей степени окисления.
Хелатирующие реагенты содержат два основных типа электродонорных центров: а)группы, содержащие подвижный протон, например, -COOH, -OH, -SO3H; при их координации к центральному иону возможно замещение протона и б)нейтральные электронодонорные группы, например R2CO, R3N. Бидентатные лиганды занимают во внутренней координационной сфере хелата два места, как, например, этилендиамин (рис.3).
Согласно правилу циклов Чугаева, наиболее устойчивые хелатные комплексы образуются в том случае, когда в состав цикла входит пять или шесть атомов. Например, среди диаминов состава H2N-(CH2)n-NH2 наиболее устойчивые комплексы образуются для n=2 (пятичленный цикл) и n=3 (шестичленный цикл).
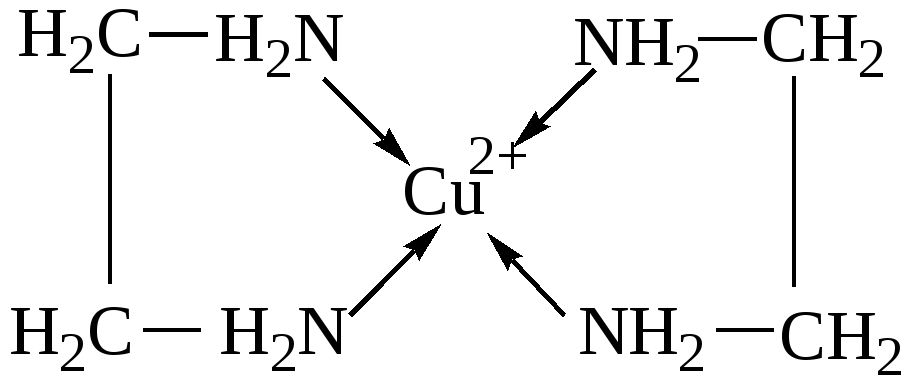
Рис.3. Катион бисэтилендиамин меди(II).
Хелаты, в которых при замыкании хелатного цикла лиганд использует протон-содержащую и нейтральную электронодонорные группы и формально связан с центральным атомом ковалентной и донорно-акцепторной связью, называются внутрикомплексными соединениями. Так, полидентатные лиганды с кислотными функциональными группами могут образовывать внутрикомплексные соединения. Внутрикомплексные соединения – это хелат, в котором замыкание цикла сопровождается вытеснением из кислотных функциональных групп одного или нескольких протонов ионом металла, в частности, внутрикомплексным соединением является глицинат меди(II):
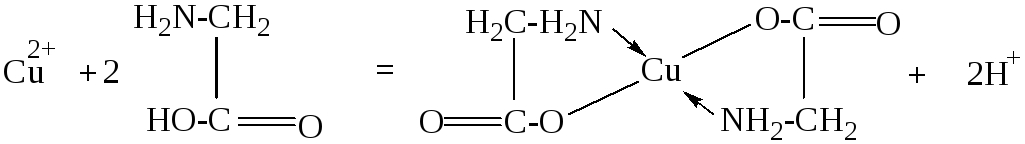
Рис.4. Внутрикомплексное соединение 8-оксихинолина с цинком.
Гемоглобин и хлорофилл также являются внутрикомплексными соединениями.
Важнейшая особенность хелатов – их повышенная устойчивость по сравнению с аналогично построенными нециклическими комплексами.
