
8. Токсичность кислорода
Длительное
вдыхание чистого кислорода может иметь
опасные последствия для организма.
Безопасно длительно дышать при обычном
давлении смесями, содержащими до 60%
кислорода. Дыхание 90% кислородом в
течение 3 суток приводит к тахикардии,
рвоте, пневмонии, судорогам. При повышении
давления токсическое действие кислорода
ускоряется и усиливается. Молодые люди
более чувствительны к токсическому
действию кислорода, чем пожилые. При
отравлении кислородом развиваются
нарушения функций центральной нервной
системы, органов дыхания и кровообращения.
Поэтому при терапии кислородом(оксигенотерапия)
концентрация кислорода во вдыхаемой
смеси не должна превышать 44%. (рисунок
10) [18]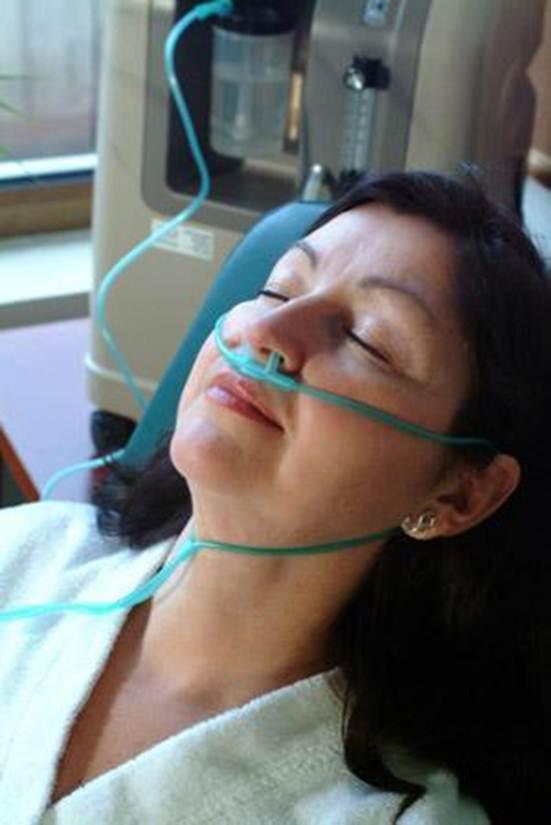
Рис. 10 Кислородная терапия
Некоторые производные кислорода такие, как синглетный (общее название для двух метастабильных состояний молекулярного кислорода с более высокой энергией, чем в основном, триплетном состоянии) кислород, пероксид водорода, супероксид, озон и гидроксильный радикал, являются высокотоксичными продуктами. Они образуются в процессе активирования или частичного восстановления кислорода. Супероксид, пероксид водорода и гидроксильный радикал могут образовываться в клетках и тканях организма человека и животных и вызывают оксидативный стресс.
9. Экологические проблемы
Почти все соединения, так или иначе послужившие возникновению экологических проблем в нашем мире, являются кислородосодержащими.
К глобальным экологическим проблемам современности относятся: изменение климата, кислотные осадки, фотохимический смог, парниковый эффект, истощение озонового слоя, опустынивание, обезлесение, деградация почв, проблемы отходов. [19]
В современном мире наблюдается изменение климата в сторону потепления, которое называется глобальным потеплением. Одной из причин глобального потепления является повышенная концентрация парниковых газов в атмосфере. Основными парниковыми газами Земли являются водяной пар, углекислый газ, метан и озон. То есть, вклад кислородосодержащих соединений в парниковый эффект может составлять до 90%. (Таблица 2) [20] [21]
|
Газ |
Вклад в парниковый эффект(в %) |
|
Водяной пар |
36 — 72 % |
|
Углекислый газ |
9 — 26 % |
|
Метан |
4 — 9 % |
|
Озон |
3 — 7 % |
Таблица 2. Вклад различных газов в парниковый эффект
Фотохимический смог же является пеленой едких газов и аэрозолей повышенной концентрации, возникающая под действием ультрафиолетовой радиации Солнца в воздухе в результате фотохимических реакций, происходящих в атмосфере в присутствии газовых выбросов автомашин и химических предприятий. Фотохимический смог создают диоксид азота и озон. [22]
Кислотный
дождь (Рисунок 11) образуется в результате
реакции между водой и такими загрязняющими
веществами, как оксиды серы (SO2 и SO3) и
различными оксидами азота. Эти вещества
выбрасываются в атмосферу автомобильным
транспортом, в результате деятельности
металлургических предприятий, тепловых
электростанций.
Рис. 11 Последствия кислотных осадков
Истощение озонового слоя стало предметом для обсуждения учёных всего мира ещё в конце 60-х годов. Тревогу вызвала способность оксида азота, который выбрасывается воздушным транспортом на высоте 25 км, как раз в области распространения щита Земли, уничтожать озон. Газ, который закрывает в виде щита нашу планету, разрушается, потому что его повреждают вещества, такие как хлорфторуглероды – фреоны, окислы азота, окислы алюминия. Становится очевидным, что виновником повреждения озонового слоя является человек и его деятельность на земле.
Таким образом, кислород фигурирует в экологических проблемах, связанных с каждой оболочкой Земли. В атмосферном воздухе, чаще всего городских территорий, наблюдается повышенная концентрация загрязняющих кислородосодержащих веществ: диоксида серы, диоксида и оксида азота, оксида углерода. Кислород причастен и к истощению озонового слоя, так как основными разрушителями его являются оксид азота и водяной пар. На литосфере и гидросфере же отражаются кислотные дожди и последствия истощения озонового слоя.
Заключение
Кислород – самый противоречивый элемент в природе. Большинство живых организмов(аэробов) не смогут жить без кислорода, но, если бы концентрация кислорода в атмосфере хоть немного изменилась бы, то погибло бы почти все живое. Мы живем благодаря тому, что вдыхаем кислород, но он же нас и убивает, согласно свободнорадикальной теории старения. Кислород в небольших количествах может оказывать лечебное действие, а в больших вызывать кислородное отравление, которое так же может привести к смерти.
Озоновый слой защищает нас от губительных ультрафиолетовых лучей, но озон же является парниковым газом, производящим достаточный вклад в парниковый эффект. Кислородосодержащие соединения, особенно оксиды, становятся причинами многих глобальных экологических проблем. Кислород все еще требует тщательного изучения для того, чтобы свести его губительное действие к минимуму, а с экологическими проблемами борется огромное количество ученых по всему миру.
Нет сомнения в том, что этот элемент может быть вреден для человека и окружающей среды, но именно он является одним из самых важных элементов таблицы Менделеева. Благодаря нему на Земле зародилась жизнь и живы мы.
Приложения
Приложение 1. Теория флогистона
Первая теория научной химии – теория флогистона – в значительной степени основывалась на традиционных представлениях о составе веществ и об элементах как носителях определённых свойств. Тем не менее, именно она стала в 18 веке главным условием и основной движущей силой развития учения об элементах и способствовала полному освобождению химии от алхимии. Именно во время столетнего существования флогистонной теории завершилось начатое Бойлем превращение алхимии в химию. [23]
Флогистонная теория горения была создана для описания процессов обжига металлов, изучение которых являлось одной из важнейших задач химии конца 18 века. Металлургия в это время столкнулась с двумя проблемами, разрешение которых было невозможно без проведения серьёзных научных исследований – большие потери при выплавке металлов и топливный кризис, вызванный почти полным уничтожением лесов в Европе.
По мнению ученых того времени, все вещества, которые так или иначе подвергаются горению, содержат некую похожую огненную материю, которую и назвали флогистон. Когда металл или вещество подвергалось горению, флогистон улетучивался, оставляя землистый осадок – окалину. Таким образом, реакцию горения в те времена представляли, как разложение металла на флогистон и окалину.
Приложение 2. Легкие планеты
Общеизвестный факт - кислородную атмосферу Земли создали и продолжают поддерживать именно растения. Это случилось потому, что они научились создавать органические вещества из неорганических, используя при этом энергию солнечного света (как мы помним из школьного курса биологии, подобный процесс называется фотосинтезом). В результате этого процесса листья растений выделяют свободный кислород как побочный продукт производства. Этот необходимый нам газ поднимается в атмосферу и потом равномерно распределяется по ней.
На суше, как ни странно, основными поставщиками кислорода являются торфяные болота. Всем известно, что, когда на болоте погибают растения, их организмы не разлагаются, поскольку бактерии и грибы, делающие эту работу, не могут жить в болотной воде — там много природных антисептиков, выделяемых мхами. Таким образом, отмершие части растений, не разлагаясь, опускаются на дно, образуя залежи торфа. А если нет разложения, то и кислород не тратится. Поэтому болота отдают в общий фонд около 50% вырабатываемого ими кислорода.
Весь мировой фитопланктон вырабатывает в 10 раз больше кислорода, чем нужно ему самому для дыхания. Хватает для того, чтобы обеспечить полезным газом и всех остальных обитателей вод, и в атмосферу попадает немало. Что касается затрат кислорода на разложение трупов, то в океане они весьма низки — примерно 20% от общей выработки.
Итак, океан поставляет в атмосферу около 40% того кислорода, которое произвел фитопланктон. Именно этот запас и расходуется в тех областях, где кислорода вырабатывается очень мало. К последним, кроме городов и деревень относятся пустыни, степи и луга, а также горы.
Так что, как это ни странно, мы живем на Земле именно за счет микроскопических "кислородных фабрик", плавающих по поверхности океана.
Приложение 3. Свободнорадикальная теория старения
В традиционной формулировке гипотеза о том, что вдыхание кислорода вызывает старение организма, довольно проста. Свободнорадикальная теория старения утверждает, что старение происходит из-за накопления повреждений в клетках, нанесённых свободными радикалами с течением времени. [24]
В процессе клеточного дыхания внутри каждой клетки нашего тела постоянно образуются свободные радикалы. Свободные радикалы в химии — частицы (как правило, неустойчивые), содержащие один или несколько неспаренных электронов на внешней электронной оболочке. Наличие неспаренного электрона способно значительно усилить реакционную способность, хотя это свойство радикалов широко варьируется. Свободными радикалами являются также молекулы O2, NO, NO2, ClO2.
Бо́льшая часть свободных радикалов устраняется антиоксидантами, но защитные системы организма несовершенны. Некоторые свободные радикалы обходят механизм защиты и повреждают жизненно важные элементы тканей и клеток, такие как ДНК и белки. Со временем повреждения накапливаются, и в какой-то момент организм перестает функционировать. Эту постепенную деградацию организма называют старением. [25]
Список литературы
1. Кислород. Молекула, изменившая мир/ Ник Лэйн – Москва: Издательство «Э», 2016
2. Lavoisier, A. Elements of Chemistry. Dover Publications, New Yourk, 1965(впервые опубликовано в Париже в 1789)
3. Szydlo, Z. Water, which does not wet hands. The Alchemy of Michael Sendivogius. Polish Academy of Sciences, Warsaw, 1994(здесь и далее - издания, обозначенные английским и другими языками, не имеют перевода на русский язык – прим. автора работы)
4. Tractatus duo, quorum prior agit de respiratione, alter de rachitide, a Joh. Mayow, 1671
5. Кнунянц И. Л. и др. Химическая энциклопедия. — Москва: Советская энциклопедия, 1990. — Т. 2.
6. Я. А. Угай. Общая и неорганическая химия. — Москва: Высшая школа, 1997.
7. Радиационная химия. Энциклопедический словарь юного химика. 2-е изд. Сост. В. А. Крицман, В. В. Станцо. — М.: Педагогика, 1990.
8. С. С. Колотов, Д. И. Менделеев. Озон. Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
9. National Academy of Sciences: Link Between Ozone Air Pollution and Premature Death Confirmed, Jennifer Walsh, Alison Burnette, Media Relations Assistant
Режим доступа: http://www8.nationalacademies.org
10. Curie P., Curie M. «Effects chimiques produits par les rayons de Becquerel». Comptes rendus de l'Académie des Sciences. - 1899
11. Радиационная химия // Энциклопедический словарь юного химика. 2-е изд. / Сост. В. А. Крицман, В. В. Станцо. — М.: Педагогика, 1990.
12. Статья “Озон - мирное оружие 21 века”, Автор: Тышкевич Е.В.,
Режим доступа: http://kosmin.ru/ozon
13. Статья Questionable methods of cancer management: hydrogen peroxide and other 'hyperoxygenation' therapies копия от 7 июля 2010 на Wayback Machine, American Cancer Society
14. Ракетное топливо, Энциклопедия Министерства обороны Российской Федерации, Режим доступа: http://encyclopedia.mil.ru/encyclopedia/dictionary
15. Руководство для врачей скорой помощи / Михайлович В. А. — 2-е изд., перераб. и доп. — Л.: Медицина, 1990.
16. Информация о составе пищевых продуктов/ Пищевые добавки
Режим доступа: http://www.food-info.net/uk/e/e948.htm
17. Степанов В. М. Структура и функции белков : Учебник. — М. : Высшая школа, 1996.
18. Вредные химические вещества: Неорганические соединения элементов V-VIII групп. Справочник. - Л., 1989.
19. Адаева А.Х. СОВРЕМЕННЫЕ ГЛОБАЛЬНЫЕ ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ: ПРИЧИНЫ И НЕКОТОРЫЕ ПУТИ ИХ РЕШЕНИЯ // Молодежный научный форум: Естественные и медицинские науки: электр. сб. ст. по мат. XXV междунар. студ. науч.-практ. конф. № 6(24).
Режим доступа: https://nauchforum.ru/archive/MNF_nature/6(24).pdf
20. Горелов А.А. Экология: Учебное пособие. — М.: Центр, 2000.
21. Kiehl, J. T.; Kevin E. Trenberth (1997-02). «Earth's Annual Global Mean Energy Budget». Bulletin of the American Meteorological Society. 78 (2): 197–208
22. Абашева В.М. ФОТОХИМИЧЕСКИЙ СМОГ И ЕГО ВЛИЯНИЕ НА ОКРУЖАЮЩУЮ СРЕДУ // Научное сообщество студентов XXI столетия. ЕСТЕСТВЕННЫЕ НАУКИ: сб. ст. по мат. LIV междунар. студ. науч.-практ. конф. № 7(53).
Режим доступа: https://sibac.info/archive/nature/7(53).pdf
23. Фигуровский Н. А. Очерк общей истории химии. От древнейших времен до начала XIX века. — М.: Наука, 1969.
24. Harman D. The aging process. // Proceedings of the National Academy of Sciences of the United States of America. — 1981.
25. Кислород. Молекула, изменившая мир/ Ник Лэйн – Москва: Издательство «Э», 2016
