
- •Сложение гармонических колебаний
- •Метод векторных диаграмм
- •Энергия простого гармонического движения
- •Период малых колебаний физического маятника
- •1Постулаты эйнштейна
- •Адиабатический процесс
- •Изобарный процесс
- •[Править]Изохорный процесс
- •[Править]Изотермический процесс
- •[Править]Изоэнтропийный процесс
1Постулаты эйнштейна
– основные принципы специальной (или частной) теории относительности, созданной А. Эйнштейном.
Первый постулат Эйнштейна: законы физики во всех инерциальных системах отсчета имеют один и тот же вид (принцип относительности Эйнштейна).
Второй постулат Эйнштейна: скорость света в вакууме во всех инерциальных системах отсчета имеет одно и то же значение (принцип существования инвариантной конечной скорости).
Преобразова́ния Ло́ренца — линейные (или аффинные) преобразования векторного (соответственно, аффинного) псевдоевклидова пространства, сохраняющее длины или, что эквивалентно, скалярное произведение векторов.
Преобразования Лоренца псевдоевклидова пространства сигнатуры (n-1,1) находят широкое применение в физике, в частности, в специальной теории относительности (СТО), где в качестве аффинного псевдоевклидова пространства выступает четырёхмерный пространственно-временной континуум (пространство Минковского).
Преобразование
Лоренца (лоренцево
преобразование)
псевдоевклидова векторного
пространства ![]() —
это линейное
преобразование
—
это линейное
преобразование ![]() ,
сохраняющее индефинитное скалярное
произведение векторов.
Это означает, что для любых двух
векторов
,
сохраняющее индефинитное скалярное
произведение векторов.
Это означает, что для любых двух
векторов ![]() выполняется
равенство
выполняется
равенство
![]()
где
треугольными скобками обозначено
индефинитное скалярное произведение ![]() в
псевдоевклидовом пространстве
.
в
псевдоевклидовом пространстве
.
Аналогично, преобразование Лоренца (лоренцево преобразование) псевдоевклидова аффинного пространства — это аффинное преобразование, сохраняющее расстояние между точками этого пространства.
Под релятиви́стским замедле́нием вре́мени обычно подразумевают кинематический эффект специальной теории относительности, заключающийся в том, что в движущемся теле все физические процессы проходят медленнее, чем следовало бы для неподвижного тела по отсчётам времени неподвижной (лабораторной) системы отсчёта.
Релятивистское замедление времени проявляется[1], например, при наблюдении короткоживущих элементарных частиц, образующихся в верхних слоях атмосферы под действием космических лучей и успевающих благодаря ему достичь поверхности Земли.
Данный эффект, наряду с гравитационным замедлением времени учитывается в системе GPS — ход времени часов спутников скорректирован на разницу с поверхностью Земли[2], составляющую 38 микросекунд в день[источник не указан 483 дня].
Количественное описание замедления времени может быть получено из преобразований Лоренца:
![]()
где Δt — время, проходящее между двумя событиями движущегося объекта с точки зрения неподвижного наблюдателя, Δt0 — время, проходящее между двумя событиями движущегося объекта с точки зрения наблюдателя, связанного с движущимся объектом, v — относительная скорость движения объекта, c — скорость света в вакууме.
1ТЕПЛОВОЕ ДВИЖЕНИЕ, хаотическое движение микрочастиц, из которых состоят все тела. Кинетическая энергия теплового движения растет с абсолютной температурой вещества. Частицы газов беспорядочно движутся по всему объему газа, часто испытывая соударения друг с другом и со стенками сосуда. Частицы жидкостей колеблются около равновесного положения, изредка перескакивая из одного такого положения в другое. В твердых телах тепловое движение - колебания частиц около своих положений равновесия.
Термодинамическая система — это некая физическая система, состоящая из большого количества частиц, способная обмениваться с окружающей средой энергией и веществом. Также обычно полагается, что такая система подчиняется статистическим закономерностям. Для термодинамических систем справедливы законы термодинамики.
Термодинамические параметры - температура, плотность, давление, объем, удельное электрическое сопротивление и другие физические величины: - однозначно определяющие термодинамическое состояние системы; - не учитывающие молекулярное строение тел; и - описывающие их макроскопическое строение.
2Вну́тренняя эне́ргия тела (обозначается как E или U) — это сумма энергий молекулярных взаимодействий и тепловых движений молекулы. Внутренняя энергия является однозначной функцией состояния системы. Это означает, что всякий раз, когда система оказывается в данном состоянии, её внутренняя энергия принимает присущее этому состоянию значение, независимо от предыстории системы. Следовательно, изменение внутренней энергии при переходе из одного состояния в другое будет всегда равно разности между ее значениями в конечном и начальном состояниях, независимо от пути, по которому совершался переход.
Внутреннюю энергию тела нельзя измерить напрямую. Можно определить только изменение внутренней энергии:
![]()
где
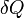 —
подведённая к
телу теплота,
измеренная в джоулях
—
подведённая к
телу теплота,
измеренная в джоулях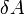 [1] — работа,
совершаемая телом против внешних сил,
измеренная в джоулях
[1] — работа,
совершаемая телом против внешних сил,
измеренная в джоулях
Эта формула является математическим выражением первого начала термодинамики
Для квазистатических процессов выполняется следующее соотношение:
![]()
где
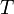 — температура,
измеренная в кельвинах
— температура,
измеренная в кельвинах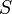 — энтропия,
измеренная в джоулях/кельвин
— энтропия,
измеренная в джоулях/кельвин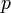 — давление,
измеренное в паскалях
— давление,
измеренное в паскалях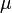 — химический
потенциал
— химический
потенциал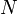 —
количество частиц в
системе
—
количество частиц в
системе
Работа в термодинамике — обобщение понятия «работа в механике» (выраженного в дифференциальной форме). Обобщённые координаты в термодинамике — это внешние параметры термодинамической системы (объём, напряжённость внешние магнитное или электрические поля и т. п.), а обобщённые силы (давление и др.) — величины, зависящие не только от координат, но и от внутренних параметров системы (температуры или энтропии). Работа термодинамической системы над внешними телами заключается в изменении состояния этих тел и определяется количеством энергии, передаваемой системой внешним телам при изменении внешних параметров системы. В квазистатических (т. е. бесконечно медленных) адиабатических процесса работа равна изменению внутренней энергии системы, в квазистатических изотермических процессах — изменению энергии Гелъмголъца
Теплота, количество теплоты, количество энергии, получаемой или отдаваемой системой при теплообмене (при неизменных внешних параметрах системы: объёме и др.). Наряду с работой количество теплоты является мерой изменения внутренней энергии U системы. При теплообмене внутренняя энергия системы меняется в результате прямых взаимодействий (соударений) молекул системы с молекулами окружающих тел.
В отличие от U — однозначной функции параметров состояния, количество Т., являясь лишь одной из составляющих полного изменения U в физическом процессе, не может быть представлено в виде разности значений какой-либо функции параметров состояния. Следовательно, элементарное количество Т. (соответствующее элементарному изменению состояния тела) не может быть в общем случае дифференциалом какой-либо функции параметров состояния. Передаваемое системе количество теплоты Q, как и работа А,зависит от того, каким способом система переходит из начального состояния в конечное.
При обратимых процессах, согласно второму началу термодинамики, элементарное количество теплоты dQ =TdS, где Т — абсолютная температура системы, dS — изменение её энтропии. Т. о., передача системе Т. эквивалентна передаче системе определённого количества энтропии. Отвод Т. от системы эквивалентен уменьшению энтропии. В общем случае необратимых процессов dQ £ TdS.
* 1-й закон — первое начало термодинамики. Представляет собой формулировку обобщённого закона сохранения энергии для термодинамических процессов. В наиболее простой форме его можно записать как δQ = δA + dU, где dU есть полный дифференциал внутренней энергии системы, а δQ и δA есть элементарное количество теплоты, переданное системе, и элементарная работа, совершенная системой соответственно. Нужно учитывать, что δA и δQ нельзя считать дифференциалами в обычном смысле этого понятия, поскольку эти величины существенно зависят от типа процесса, в результате которого состояние системы изменилось.
3Идеальный газ — математическая модель газа, в которой предполагается, что потенциальной энергией взаимодействия молекул можно пренебречь по сравнению с их кинетической энергией. Между молекулами не действуют силы притяжения или отталкивания, соударения частиц между собой и со стенками сосуда абсолютно упруги, а время взаимодействия между молекулами пренебрежимо мало по сравнению со средним временем между столкновениями.
Свойства идеального газа на основе молекулярно-кинетических представлений определяются исходя из физической модели идеального газа, в которой приняты следующие допущения:
объём частицы газа равен нулю (то есть, диаметр молекулы
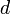 пренебрежимо
мал по сравнению со средним расстоянием
между ними,
пренебрежимо
мал по сравнению со средним расстоянием
между ними, 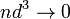 ) [1];
) [1];импульс передается только при соударениях (то есть, силы притяжения между молекулами не учитываются, а силы отталкивания возникают только при соударениях);
суммарная энергия частиц газа постоянна (то есть, нет передачи энергии за счет передачи тепла или излучения)
В этом случае частицы газа движутся независимо друг от друга, давление газа на стенку равно сумме импульсов в единицу времени, переданной при столкновении частиц со стенкой, энергия — сумме энергий частиц газа. Свойства идеального газа описываются уравнением Менделеева — Клапейрона
![]()
где
—
давление, ![]() — концентрация
частиц,
— концентрация
частиц, ![]() — постоянная
Больцмана,
—
абсолютная температура.
— постоянная
Больцмана,
—
абсолютная температура.
Для любого идеального газа справедливо соотношение Майера:
![]()
где ![]() — универсальная
газовая постоянная,
— универсальная
газовая постоянная, ![]() —
молярная теплоемкость при
постоянном давлении,
—
молярная теплоемкость при
постоянном давлении, ![]() —
молярная теплоемкость при постоянном
объёме.
—
молярная теплоемкость при постоянном
объёме.
