
- •Гравиметрический анализ Примерное содержание контрольной работы
- •1. Расчет массы навески
- •Примеры решения типовых задач
- •Задачи для самостоятельного решения
- •2. Расчет объема осадителя
- •Примеры решения типовых задач
- •Задачи для самостоятельного решения
- •3. Расчет потерь вещества при промывании осадка
- •Примеры решения типовых задач
- •Задачи для самостоятельного решения
- •4. Расчет результатов гравиметрического анализа
- •Примеры решения типовых задач
- •Задачи для самостоятельного решения
3. Расчет потерь вещества при промывании осадка
Для очистки осадков от адсорбированных на их поверхности примесей используют промывание. Кристаллические осадки с очень малой растворимостью промывают обычно дистиллированной водой. Кристаллические осадки с достаточно высокой растворимостью промывают разбавленными растворами электролитов, содержащих общие с осадками ионы. Аморфные осадки, для предотвращения их пептизации, промывают разбавленными растворами сильных электролитов, удаляемых при получении гравиметрической формы.
Независимо от того, как промывают осадок – на фильтре или декантацией, очистка его тем эффективнее, чем больше порций промывной жидкости использовано при одном и том же суммарном ее объеме.
При расчете объема промывной жидкости и потерь вещества при промывании принимается, что между осадком и промывной жидкостью устанавливается равновесие.
Примеры решения типовых задач
Пример 3.1. Осадок хромата бария массой 0,40 г промыт 100 мл Н2О. Определите потери осадка в результате его растворения при промывании (в граммах и процентах).
Дано: m(BaCrO4) = 0,40 г
V(H2O) = 100 мл
_________________________________
Найти: Δm(BaCrO4)
Решение. Считая, что между осадком и промывной жидкостью устанавливается равновесие, определим молярную растворимость хромата бария в воде:
![]()
Масса BaCrO4 в100 мл раствора, составляющая потери при промывании осадка, равна:
![]()
=![]()
![]() 7,0·10-2 %
7,0·10-2 %
Ответ: 2.76∙10-4 г, 7,0·10-2 %
Пример 3.2. Рассчитайте потери (в граммах и процентах) при промывании 0,40 г осадка фторида кальция 200 мл 0,010 моль/л раствора фторида аммония.
Дано: m(CaF2)= 0,40 г
V(H2O) = 200 мл
C(NH4F) = 0,010 моль/л
________________________________________
Найти: Δm(CaF2)
Решение. Так как промывная жидкость содержит общий с осадком ион, то молярная растворимость фторида кальция в 0,010 моль/л растворе фторида аммония равна:
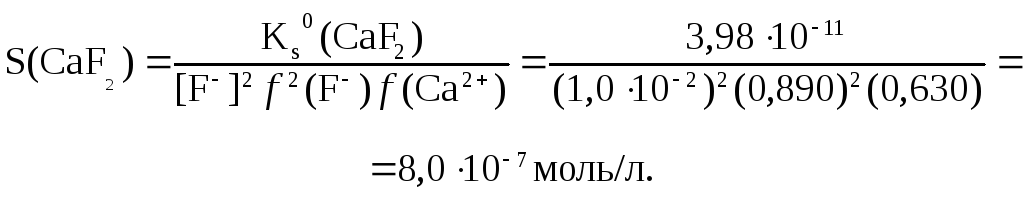
Потери фторида кальция, вследствие его растворимости в промывной жидкости, составляют:
![]()
![]() г.
г.
![]()
Ответ:
1,2∙10-5 г; 3,0![]()
Задачи для самостоятельного решения
3.1 Осадок фторида кальция массой 0,40 г промыт 100 мл воды. Рассчитайте потери осадка в результате его растворения при промывании (в граммах и процентах). Ответ: 1,8∙10-3 г; 0,44%.
3.2. Для промывания 0,41 г осадка магний-аммоний фосфата использовали 100 мл воды. Рассчитайте потери осадка в результате его растворения при промывании (в граммах и процентах).
Ответ: 8,7∙10-4 г; 0,21%.
3.3. Осадок сульфата бария массой 0,42 г промыт 150 мл воды. Рассчитайте потери осадка в результате его растворения при промывании (в граммах и процентах). Ответ: 3,6∙10-4 г, 0,09%.
3.4 Осадок оксалата кальция массой 0,45 г промыт 250 мл воды. Рассчитайте потери осадка в результате растворения осадка при промывании (в граммах и процентах). Ответ: 1,6∙10-3 г, 0,36%.
3.5 Осадок хромата бария массой 0,45 г промыт 250 мл воды. Рассчитайте потери осадка в результате растворения осадка при промывании (в граммах и процентах). Ответ: 6,9∙10-4 г, 0,15%.
