
9 Геохимия ос
Лекция 3
Любая наука стремится к систематизации объектов изучения. В геохимии объектами являются химические элементы (ХЭ) и их изотопы в земной коре (ЗК). Сразу же было обнаружено, что распределение ХЭ в ЗК крайне сильно различается при переходе от одного ХЭ к другому (рис. 1, табл. 1).
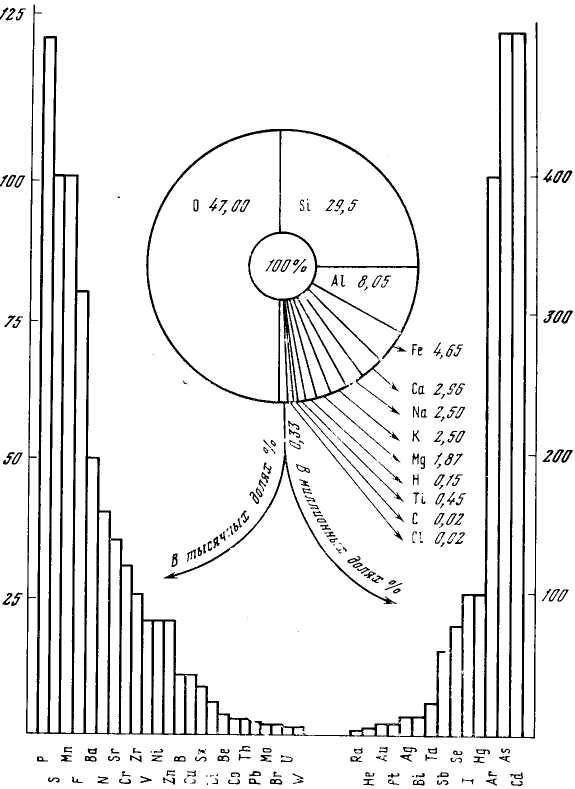
Рис. 1
Эта ситуация была известно Менделееву. Вернадский, взяв за основу логарифмическую шкалу среднего содержания ХЭ в ЗК, показал, что распределение починяется логарифмической зависимости (табл. 1).
Таблица 1 — Классификация химических элементов по декадам В.И. Вернадского (Беус и др., 1976)
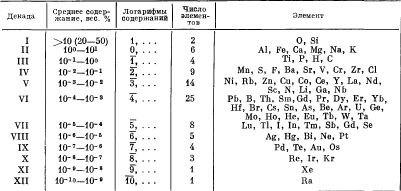
Он создал первую классификацию, выделив 6 групп: 1. благородные газы, 2. благородные металлы, 3. циклические, 4. рассеянные, 5. сильнорадиоактивные элементы и 6. редкие земли (табл. 2).
Таблица 2 — Геохимические группы ХЭ по их участию в геохимических циклах (по Вернадскому, 1934)

В этой таблице п — число химических элементов. Проценты отнесены к 92 химическим элементам периодической системы. Цифры внизу индекса элемента отвечают атомным числам (по Вернадскому, 1934). Атомное число — это сумма протонов и нейтронов.
Оказалось, что наибольшим количеством ХЭ и наибольшей массой в ЗК обладают циклические элементы, а следующие по количеству — это рассеянные ХЭ и редкие земли, которые извлекаются из ЗК с большим трудом. Наименьшие количество в ЗК имеют благородные металлы, хотя добывать их значительно проще по сравнению с рассеянными и редкоземельными ХЭ.
Таблица 3. Массы (т) групп геохимических химических элементов в земной коре

Первая группа — группа благородных газов — включает элементы, которые, во-первых, не принимают участия в главнейших химических земных процессах, и во-вторых, в исключительных случаях дают соединения с другими атомами. Эти атомы в порядке геологического времени сохраняются в значительной массе своей неизменными. В них мы наблюдаем остатки космической истории нашей планеты, но количественная интенсивность их химических проявлений в термодинамическом поле земной коры так отлична от других соединений, так относительно мала, что их реальное отличие от других земных элементов не может возбуждать сомнений. Но их геохимическое значение очень велико, и велика, по-видимому, их роль в мироздании — за пределами солнечной системы. Один из них — гелий. Его количество в земной коре изменчиво, оно увеличивается, благодаря распаду ядер атомов урана, радия, радона, полония, тория и др.
Благородные газы (инертные) — так названные химиками из-за трудности создания их химических соединений в лабораторных условиях. Наконец сюда же может быть отнесен и радон, благородный газ из 5 группы.
Вторая группа — инертные элементы благородных металлов в земной коре — включает в себя два последних ряда восьмой группы периодической системы Д. И. Менделеева, и сюда же можно отнести золото. Эти элементы дают в наших лабораториях множество устойчивых химических соединений. В этом они этим отличаются от благородных газов. Но их соединения почти не образуются в земной коре. Те же соединения и отвечающие им минералы, главным образом сплавы, получены сложным пневматолитическим и магматическим путем. Образование золота происходит в результате глубинных гидротермальных процессов в термодинамических условиях, резко отличных от того, что наблюдается в биосфере. Раз образовавшись, благородные металлы изменяются мало или совсем не изменяются в течение геологического времени. В биосфере образуются кислородные соединения палладия, для него же и для самородков платины и золота существуют многочисленные явления выветривания, связанные с изменением химического состава и строения. Но эти химические реакции не меняют общего характера группы — химической инертности в земной коре, их очень мало содержатся в водных растворах, в рассеянном состоянии, связанными явлениями сорбции.
Третья группа – циклических или органогенных элементов — наибольшая по массе (99,7%). Она включает наибольшее число химических элементов и образует почти всю земную кору. Для нее характерны многочисленные химические обратимые процессы. Геохимическая история всех этих элементов может быть выражена круговыми процессами («циклами»). Каждый элемент дает характерные для определенной геосферы соединения, постоянно возобновляющиеся. После более или менее продолжительных и более или менее сложных изменений элемент возвращается к первичному соединению и начинает новый цикл, завершающийся для элемента новым возвращением к первоначальному состоянию.
В органогенных циклах участвуют и металлы, как например: Fe, Сu, Zn, V, Мn и т.д. Элементы этой группы образуют циклы, характеризуемые химическими соединениями, молекулами или кристаллами. Эти циклы обратимы лишь в главной части атомов, часть же элементов неизбежно и постоянно выходит из круговорота. Этот выход закономерен, т. е. круговой процесс не является вполне обратимым.
Циклические элементы входят и играют видную роль в водных растворах в земной коре, т. е. образуют минералы водным путем. Исключение составляют цирконий (Zr) и гафний (Hf). Те же Zr и Hf не входят в живое вещество; не найдено в нем и германия, несмотря на водный характер его миграции в ЗК.
В группе рассеянных элементов преобладают атомы, которые охватывают небольшую часть массы и циклических элементов. И для них тоже существуют циклы. Их соединения разлагаются более или менее полно в одном участке этих циклов и возобновляются при новых термодинамических условиях в другом их участке. Все эти элементы отличаются отсутствием или редкостью химических соединений как в определенных участках земной коры, так даже и во всей земной коре.
Существуют два случая, резко отличных друг от друга. Некоторые из элементов, как-то: Li, Sc, Rb, Y, Cs, Nb, Та, In, дают химические соединения лишь в глубоких областях земной коры; их минералы разлагаются в поверхностной области в биосфере, но новые соединения этих элементов здесь не образуются. Эти элементы рассеяны во всем окружающем веществе в виде «следов» без всякого видимого отношения к тем минералам и к горным породам, в которых их находят.
Второй случай — йод и бром. Они вступают в соединения с другими элементами лишь в биосфере. Источниками йода и брома служат слабые водные растворы. Из них живое вещество их извлекает и концентрирует. В глубинах коры мы находим йод и бром лишь рассеянном состоянии.
Таким образом, круговые процессы, отвечающие этим элементам, особые: в одном месте элементы дают химические соединения, в другом – то свободные атомы. Но большая часть их вообще не вступает в какие-либо соединения и находятся в окружающем нас веществе в рассеянном состоянии, в состоянии свободных атомов. Удивителен факт, что все эти элементы принадлежат к группе ХЭ с нечетным атомным числом. Это указывает на то, что строение атомных ядер обуславливает такое их поведение. Ферсман показал, что в пегматитовых месторождениях преобладают четные ХЭ. Однако, физического объяснения этому удивительному явлению пока нет.
Пятая группа элементов включает сильно радиоактивные элементы, семейства урана, актиния и тория. Здесь неполная обратимость их круговоротов очевидна. В общем, уран и торий дают соединения, входящие в обратимые циклы, циклы замкнутые, аналогичные круговоротам циклических элементов. Однако часть их атомов теряется и обратно не возвращается; она распадается, изменяется и дает начало другим элементам, из которых два гелий и изотопы свинца — входят в совершенно другие химические группы, группы благородных газов и циклических элементов.
Шестая группа — Редкие земли — уникальное семейство металлов в периодической системе Д. И. Менделеева. Эти элементы считались редкими, несмотря на их широкое распространение. Как церия в земле больше, чем свинца, а самые редкие из редкоземельных металлов распространены в земной коре намного больше, чем ртуть. Все дело в рассеянности этих элементов и сложности отделения их один от другого. Уникальность редкоземельных элементов заключается в том, что все металлы этой группы должны были бы стоять в одной клетке таблицы Менделеева, так похожи они по своим свойствам. Чтобы избежать путаницы в стройной таблице ХЭ, было предложено вынести эти 15 элементов за её пределы — это лантан, церий, празеодим, неодим, прометий, самарий, европий, гадолиний, тербий, диспрозий, гольмий, эрбий, тулий, иттербий и лютеций.
С точки зрения нахождения в природе лантаноиды делятся на 2 группы: цериевую (La, Ce, Pr, Pm, Sm) и иттриевую (Y, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb, Lu). Данное деление основано на том, что в одних минералах встречаются преимущественно церий и его "команда", а в других - иттрий вместе с остальными редкоземельными элементами. К минералам цериевой группы относится монацит (Ce, La, Nb....)PO4. Он образует россыпи монацитового песка, куда кроме него входит кварц, рутил, оксид тория (IV). Второй по важности редкоземельный минерал -- бастнезит -- во многом похож на него. Если монацит -- фосфат, то бастнезит -- фторокарбонат редких земель, его состав обычно записывают так: (La, Ce)FCO3. Распространённость лантаноидов подчиняется общей закономерности: элементов с чётными порядковыми номерами содержится больше, чем с нечётными. Всего известно около 70 собственно редкоземельных минералов и еще около 200 минералов, в которые эти элементы входят как примеси. Геохимические особенности (по Вернадскому) — они не вступают во взаимодействия с ХЭ, находящихся в ЗК в большинстве. Они остаются обычно вместе в минеральном теле при червычайно различающихся природных ситуациях.
