
- •1. 100%-Ные пленкообразующие системы. Сравнительная характеристика жидких и порошковых систем.
- •2. Водоразбавляемые пленкообразователи ( водноспиртовые растворы
- •3.Химические основы синтеза алкидов.
- •5. Ненасыщенные полиэфирные лаки. Состав, отверждение, свойства покрытий
- •6. Общие закономерности получения фенол-, мочевоно- и меламиноформальдегидных смол.
- •Закономерности получения мч смол на формалине
- •7. Исходные материалы, химия, условия получения, свойства и применение маслорастворимых фф смол.
- •4) Маслорастворимые ффо (100% смолы)
- •8. Получение, свойства и применение водоразбавляемых фф смол
- •9. Получение, свойства и применение мочевиноформальдегидных смол
- •10. Получение, свойства и применение мл-смол.
- •11 . Пос на основе афо – состав, реакции отверждения.Св-ва, применение.
- •12. Сравнительная характеристика способов получения эпоксидных пленкообразователей.
- •13. Низкотемпературные отвердители эпоксидных смол. Химия отверждения, свойства отвержденных композиций
- •14. Порошковые композиции на основе эпоксидных смол – состав, условия, химия условия отверждения, свойства покрытия.
- •15. Эпоксиэфиры. Получение, свойства, применение
- •16. Двухупаковочные композиции для полиуретановых покрытий – состав, условия и химия отверждения.
- •17. Одноупаковочные композиции для полиуретановых покрытий высокотемпературной сушки – химия, условия получения, свойства покрытий.
- •18. Получение, свойства и применение уралкидов.
- •19. Полиорганосилоксаны. Получение, свойства, применение.
- •4. Немодифицированные pos.
- •5. Модифицированные pos.
- •20 Полиолефины: полиэтилен, полипропилен.
- •20. Полиолефины и продукты их химической переработки в качестве пленкообразователей.
- •21. Получение, свойства и применение пва
- •22. Получение, свойства и применение пвАц
- •23. Получение, свойства и применение поливинилхлорида.
- •3.Классификация
- •3.1Термопластичные.
- •3.2 Термореактивные органорастворимые.
- •3.3Термореактивные, водоразбавляемые.
- •3.4 Фторсодержащие па для вс.
- •3.5 Полифункциональные акриловые мономеры.(пам)
- •27. Технология производства алкидов и лаков на их основе.
- •1. Модификаторы
- •Технология производства алкидов по периодической схеме моноглицеридным способом и лаков на их основе.
- •Технология производства алкидов по полунепрерывной схеме моноглицеридным способом и лаков на их основе.
- •28 Технология производства 101 смолы.
- •2 9 Технология производства аминоформальдегидных олигомеров.
- •30 Технология производства смолы э-40
- •31. Химические реакторы. Классификация. Устройство реактора периодического действия. Виды обогрева. Типы теплопередающих поверхностей. Оснастки реакторов.
- •3) Конструктивные размеры и объемы.
- •2) Обогрев теплоносителями .
- •33. Смесители и аппараты для охлаждения расплавов полимеров – схемы, критерии выбора.
- •34. Оборудование для очистки растворов полимеров. Классификация. Схемы, технич.Характеристика, критерии выбора.
- •35. Оборудование для транспортирования и дозирования жидкого сырья.
- •Тду для жидкого сырья
- •Тв.Сырье
- •Транспортирующие устройства.
10. Получение, свойства и применение мл-смол.
Исходные материалы:
1. меламин f=6
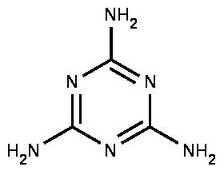
МЛ смолы более (реакционоспособные, чем МЧ из-за более высокой функциональности из-за циклической структуры меламина).
2.СН2О-формальдегид- газообразное вещество, поэтому применяют в виде формалина-37%-формальдегида;
параформа- продукт полимеризации НО[-СН2-О-]nН
3.Алифатические спирты ,которые применяются для:1)регулирования длины цепи для исключения гелеобразования при синтезе; 2)для придания смоле растворимости в растворителях и совместимости с другими п-о.В качестве алифатического спирта применяют- н-бутанол для получения органорастворимых смол, а также метанол – для получения водоразбавляемых смол растворного типа.
4.Катализаторы.1) МеОН,Ме(ОН)2,водорастворимые третичные амины R3N3.Катализаторы основного характера являются слабыми , рпименяются для предотвращения вероятности гелеобразования на начальных этапах синтеза.2)кислоты-НСl,RСООН, где R:Н-муравьиная,СН3-уксусная.Кислоты применяют на конечных стадиях синтеза, когда скорость процесса регулируется избытком спирта.
Процесс получения состоит из ряда последовательных параллельных реакций:
1ст.Растворение меламина в предварительно нейтрализованном формалине рН=7,0-8,0 при 55-60 оС, получение метилольных производных карбамида.
Формальдегид и меламин – берут в мольном соотношении 7:1.
а)замещение атомов углерода
Образуется смесь гидроксиметильных заместителей с f=3-6.Гексаметилолмеламин получается только при большом мольном избытке СН2О. Меламин плохо растворяется в воде и водном растворе формальдегида при низких температурах, поэтому необходимо повышать на стадии гидроксиметилирования до 70-80оС.Снижение величины рН происходит за счет побочных реакций: 2СН2О +Н2О ОН- СН3ОН +НСООН
Окисление СН2О кислородом воздуха 2СН2О + О2 ОН- 2 НСООН Контроль по конверсии формальдегида. При достижении необходимой конверсии СН2О в вакууме отгоняют метанольную воду для уменьшения потерь метанола.
2ст.Реакционную массу растворяют в бутаноле и подкисляют при рН =3,5-5,5 и проводят поликонденсацию и бутанолизацию при азиатропном обезвоживании 90-95 оС в вакууме:
>N-Н+НО-СН2N< -Н2О >NСН2N<
> NСН2О-Н+НО-СН2N< >NСН2О СН2N<
бутанолизация:
> NСН2О-Н + НО-R > NСН2ОR
В результате поликонденсации получается олигомер:
ОНСН2-N-СН2ОR НNСН2ОR
С С
N N N N
НО-СН2-N-С С-N-СН2---- N------С С-N-СН2-О-Н
СН2ОН N СН2ОR СН2ОН N СН2ОН
Контроль по углеводородной совместимости и по вязкости раствора и по содержанию нелетучих.
Параллельно протекают реакции: а)реакции поликонденсации
1)Вз. групп > NН + НОСН2N< > NСН2N< + Н2О
2) Н-ОСН2N< + ОН-СН2N< >NСН2ОСН2N< + Н2О диметиленоксидные связи. При 120 оС разлагаются с образованием метиленовых связей и формальдегида.
б)реакции алкилирования спиртами
>НNСН2-ОН + Н-ОR > NСН2ОR + Н2О N-метоксиалкильная гр.
Алкилирование спиртами приводит к уменьшению реакционной способности смол и уменьшению температуры отверждениякомпозиции. Увеличению поликонденсации способствует высокая температура ,меньшая кислотность, меньшая концентрация спирта. Долю реакции алкилирования способствует большой избыток спирта, высокая температура, большая кислотность.
Исходные материалы.Условия и химия получения п-о на основе ПВХ и ПХВ.Деструкция и стабилизация ПВХ и ПХВ.
Исходные данные ПВХ:
СН2=СН - винилхлорид
Cl
ПВХ продукт радикальной полимеризации винилхлорида в водных дисперсиях и суспензиях:
СН2=СН Iniz -СН2-СН- дисперсия
Cl ПАВ Сl
или дисперг. суспензия
органич
ПВХ один из самых распространенных промышленных полимеров, чрезвычайно хим. стоек к действию конц. кислот ,щелочей и солей, практически не горюч, но отличается крайне низкой термо- и атмосферостойкостью т.к. подвергается дегидрохлорированию с выделением водорода:
-СН2-СН-СН2-СН- -СН=СН-СН=СН-
Cl Cl -НCl
Процесс автокаталитический(самоускоряющейся). Протеккет при нагревании Т>110 С0, при действии УФ при Ткомн..
Недостатком ПВХ, как п-о:
1)практически нерастворим в лаковых растворителях
2)низкая адгезии
3)высокая хрупкость
Эти недостатки устраняются:
1)введением термо- и светостабилизаторов
2)применением пластификаторов
В качестве светостабилизаторов применяются добавки поглощающие и отражающие УФ свет. Действия этих добавок специфично, в зависимости от введенного кол-ва они могут или замедлять, или ускорять процесс.
Добавки хим. действия
1. Добавки, связывающие выделившейся хлористый водород – эпоксидированные растительные масла.
-СН-СН- + НCl -СН-СН-
О ОН Cl хлоргидрин
Эти пластификаторы наз. –пластификаторы.
2.Стабилизаторы, взаимодействующие с образующимися 2-ыми связями – диалкилмолейнаты:
-СН=СН-СН=СН- + - СН=СН- t>100о .дибутил ОС СО
диоксид молейнаты ОR ОR
СН=СН
-СН СН-
СН-СН
ОС СО
ОR ОR хлорпарафины
Диалкилмолейнаты хорошие пластификаторы для ПВХ.
3.Пластификаторами для хим. стойких покрытий служат хлорпарафины.
Все вышеназванные пластификаторпы обладают межструктурным действием. В результате чего в процессе эксплуатации покрытий и изделий из ПВХ происходит разделение из ПВХ (выпотевание) пластификатора. В результате чего изделия из ПВХ приобретают дополнитьельную хрупкость.
Исходные данные ПХВ:
-СН2-СН- -ПВХ
Cl
ПХВ- это продукты хлорирования газообразным хлором водных дисперсий или суспензий ПВХ для получения органорастворимых.
При хлорировании идет замещение части атомов Н в группах СН2 на атомы Cl с отщеплением НCl.
-[СН2-СН-]3n -[-СН2-СН-СН-СН-СН2-СН-]m-
Cl Cl Cl Cl Cl
/ ПВХ ПХВ
+ mНCl 3n>m
Т.е. процесс хлорирования сопровождается деструкцией ПВХ приводящей к уменьшению степени полимеризации. В среднем при хлорировании каждая 3-я группа СН2 заменяется атомом Н на Cl. При хлорировании содержание Cl увеличивается с 56% в ПВХ до 65% в ПХВ.
ПХВ обладает практически всеми преимуществами и недостатками ПВХ, но отличается более высокой огнестойкостью, растворимостью в сложных эфирах и кетонах, и лучшей совместимостью с пластификаторами. ПХВ формирует покрытия при t комн. в течении 15-30 мин., ПВХ при t>200 оС.
В состав растворителей для снижения затрат , вводят разбавитель – толуол. В качестве пластификаторов применяют для хим. стойких покрытий: хлорпарафин; для покрытий общего назначения: нелетучие сложные эфиры, дибутилфталат, каст.масло, диэфиры на основе гликолей и СЖК.
Дегидрохлорирование покрытий под воздействием УФ лучей и t>100 оС.
