
- •Министерство образования Российской Федерации
- •Работа 1. Важнейшие классы неорганических соединений: оксиды, основания (гидроксиды), кислоты, соли
- •Реагенты для проведения качественных реакций
- •Работа 2. Труднорастворимые электролиты.
- •Задание 1. Влияние температуры на растворимость иодида свинца
- •Работа 3. Приготовление растворов
- •Работа 4. Основы электрохимии
- •Задание 3. Расчет отношения активностей окисленной и восстановленной форм ионов в растворе
- •Индивидуальные задания для расчета
- •Работа 5. Комплексные соединения
- •V, VI, VII групп Периодической системы
- •Восстановление перманганата калия нитритом
- •Индивидуальные задания к лабораторной работе 6
- •Работа 7. Свойства металлов (s-, p-, d-элементов)
- •Работа 8. Свойства лантанидов и актинидов
- •Реактивы Кислоты и основания
- •Металлы, индикаторы и другие реактивы
- •Библиографический список
- •Оглавление
- •620002, Екатеринбург, Мира, 19
Министерство образования Российской Федерации
Уральский государственный технический университет
ОБЩАЯ ХИМИЯ
Методические указания к лабораторному
практикуму для студентов дневной формы обучения
физико-технического факультета
Екатеринбург 1999
УДК 546 (076.5)
Составители А.Н.Губанова, Д.Г.Лисиенко, С.Ю.Пальчикова, В.К.Слепухин,
Л.Б.Хамзина
Научный редактор доц., канд. хим. наук С.Ю.Пальчикова
ОБЩАЯ ХИМИЯ: Методические указания к лабораторному практикуму/
А.Н.Губанова, Д.Г.Лисиенко, С.Ю.Пальчикова, В.К.Слепухин, Л.Б.Хамзина.
Екатеринбург: УГТУ, 1999. 32 с.
Методические указания содержат описания лабораторных работ, а также контрольные вопросы и библиографический список. Данные указания составлены для студентов первого курса физико-технического факультета всех специальностей в соответствии с учебными планами.
Библиогр.: 4 назв. Табл. 6.
Подготовлено кафедрой «Физико-химические методы анализа».
© Уральский государственный
технический университет, 1999
К лабораторной работе студент готовится самостоятельно: читает литературу, соответствующую теме занятия, находит в справочниках численные значения констант и другие необходимые данные, делает предварительные расчеты.
Перед выполнением лабораторного практикума студент обязан пройти инструктаж по технике безопасности при работе в химической лаборатории.
Во время выполнения лабораторной работы необходимо быть предельно внимательным и осторожным. Запрещается проводить опыты, не предусмотренные планом, и создавать ситуации, опасные для окружающих.
По окончании работы студент оформляет и сдает отчет.
На титульном листе отчета указывается название работы, фамилия студента, номер группы, фамилия преподавателя и дата выполнения лабораторной работы.
Содержание отчета включает следующие пункты (по каждому заданию):
номер и название (цель) задания;
краткое теоретическое введение по теме задания, необходимые формулы и расчеты;
экспериментальные данные: результаты измерений с указанием погрешности, наблюдаемые явления при выполнении химических реакций (изменение цвета раствора, образование или растворение осадка, выделение газа и др.);
ответы на вопросы, поставленные в задании, запись уравнений химических реакций, выводы по теме работы.
Примеры отчетов, оформленных в соответствии с требованиями ГОСТа, представлены на специальном стенде.
Работа 1. Важнейшие классы неорганических соединений: оксиды, основания (гидроксиды), кислоты, соли
ОКСИДЫ – это соединения элементов с кислородом. Оксиды получают непосредственным взаимодействием простых веществ с кислородом или косвенным путем – термическим разложением солей, оснований, кислот:
2Mg + O2 = 2MgO CaCO3 = CaO + CO2
2Al(OH)3 = Al2O3 + 3H2O H2SO4 = SO3 + H2O
Оксиды подразделяются на солеобразующие (таких большинство) и несолеобразующие (NO, CO и некоторые другие).
Солеобразующие оксиды подразделяются на кислотные, основные и амфотерные, что связано с особенностями их поведения в различных химических реакциях, в частности при взаимодействии с водой, кислотами, основаниями.
Кислотные оксиды – это оксиды типичных неметаллов (CO2, SO3, P2O5, NO2, SiO2 и др.), а также оксиды металлов в степенях окисления +5 и выше (V2O5, CrO3, Mn2O7 и др.). Соединения данных оксидов с водой (гидраты) являются кислотами, поэтому кислотные оксиды называют также ангидридами кислот. Большинство кислотных оксидов непосредственно растворяются в воде, образуя кислоты: CO2 + H2O = H2CO3. Если оксид в воде нерастворим, то соответствующая кислота может быть получена косвенным путем, например, гидрат оксида кремния SiO2H2OH2SiO3 (кремниевая кислота) образуется по реакции Na2SiO3+2HCl=H2SiO3+2NaCl.
Кислотные оксиды взаимодействуют с основаниями, а также с основными и амфотерными оксидами с образованием солей соответствующих кислот:
SO3 + 2NaOH = Na2SO4 + H2O
SO3 + MgO = MgSO4
V2O5 + 2NaOH = 2NaVO3 + H2O
Основные и амфотерные оксиды образуют только металлы.
Основные: оксиды металлов IA и IIA групп Периодической системы (кроме ВеО), а также FeO, NiO, MnO и др.
Основные оксиды, соединяясь с водой, образуют основания.
Оксиды, хорошо растворимые в воде, образуют щелочи: Na2O+H2O=2NaOH.
Оксиды труднорастворимые – дают осадки гидроксидов:
MgO + H2O = Mg(OH)2
Большинство основных и амфотерных оксидов практически нерастворимо в воде. Соответствующие им гидроксиды также труднорастворимы и могут быть получены в водных растворах по реакциям обмена:
FeSO4 + 2NaOH = Fe(OH)2 + Na2SO4.
Основные оксиды взаимодействуют с кислотами, а также кислотными и амфотерными оксидами с образованием солей:
CaO + 2HCl = CaCl2 + H2O
NiO + SO3 = NiSO4
Амфотерные оксиды: BeO, PbO, SnO, ZnO, Cr2O3, Al2O3 и др.
Амфотерные оксиды взаимодействуют как с кислотами (кислотными оксидами), так и с основаниями (основными оксидами). При взаимодействии с кислотой образуется соль, в которой металл является катионом данной соли, например: ZnO + 2HCl = ZnCl2 + H2O, катион соли Zn2+. При взаимодействии с основанием образуется соль, в которой металл входит в состав аниона данной соли, например:
ZnO + 2NaOH = Na2ZnO2 + H2O, ZnO22- - оксоанион соли,
ZnO + 2NaOH + H2O = Na2[Zn(OH)4], [Zn(OH)4]2- - гидроксоанион соли.
ОСНОВАНИЯ (щелочи, гидроксиды) – вещества, в состав которых входят гидроксильные группы ОН- и других анионов нет. Общая формула оснований – Мe(ОН)n.
Основания щелочных металлов, стронция, бария являются хорошо растворимыми. В водном растворе они полностью диссоциированы на ионы (являются сильными электролитами) и называются щелочами:
NaOH = Na+ + OH-
Аммиак хорошо растворяется в воде, его раствор является основанием. Гидроксильные группы образуются в результате разрыва связей в молекулах воды: NH3 + H2O = NH4+ + OH-. Это равновесный процесс и равновесие смещено в сторону обратной реакции, поэтому водный раствор аммиака является слабым основанием.
Все основания других металлов, кроме перечисленных выше, являются троднорастворимыми соединениями, которые обычно и называют гидроксидами. Гидроксиды могут иметь характер основной (это гидраты основных оксидов) или амфотерный (это гидраты амфотерных оксидов).
Амфотерные гидроксиды проявляют как свойства кислот, так и оснований, т.е. диссоциируют по основному и кислотному типам одновременно:
Zn2+ + 2OH- Zn(OH)2 H2ZnO2 2H+ + ZnO22-
КИСЛОТЫ – это соединения, которые в водных растворах диссоциируют на ионы Н+ и кислотный остаток и других положительных ионов не дают. Многоосновные кислоты диссоциируют ступенчато:
H2CO3 H+ + HCO3-
HCO3- H+ + CO32-
По химическому составу различают кислоты бескислородные (HCl, H2S, HBr, HF и др.) и кислородсодержащие (H2SO4, HNO3, H3PO4 и др.). Кислородсодержащие кислоты - это гидраты кислотных оксидов.
СОЛИ – это соединения ионного типа, состоящие из катионов металлов Мen+ или аммония NH4+ и кислотных остатков. Их можно рассматривать как продукты замещения Н+-ионов кислоты ионами Мen+, NH4+ либо как продукты замещения гидроксильных групп основания кислотными остатками. Соли подразделяются на средние, кислые и основные.
Средние (нормальные) соли – это продукты полного замещения Н+-ионов кислоты или ОН- -ионов основания, например: Na2CO3 – карбонат натрия, (NH4)3PO4 – ортофосфат аммония, Al2(SO4)3 - сульфат алюминия.
Средние соли в растворах полностью диссоциированы на ионы Мen+ (или NH4+) и кислотные остатки:
Al2(SO4)3 = 2Al+3 + 3SO42-
Кислые соли – это продукты неполного замещения ионов Н+ в кислоте на ионы Мen+, NH4+, например: NaHCO3 – гидрокарбонат натрия, (NH4)H2PO4 – дигидрофосфат аммония.
Кислые соли в растворе полностью диссоциируют на катионы Мen+ и водородсодержащие анионы, которые, в свою очередь, частично диссоциируют на ионы Н+ и кислотные остатки:
NaHCO3 = Na+ + HCO3-
HCO3- H+ + CO32-
Основные соли – это продукты неполного замещения гидроксильных ионов в основании на кислотные остатки, например: Al(OH)Cl2 – хлорид гидроксоалюминия, Cr(OH)2NO3 – нитрат дигидроксохрома(III). Все основные соли труднорастворимы в воде.
Задание 1. Свойства кислотных оксидов
Приготовьте три пробирки и газоотводную трубку. В первую налейте 1-2 мл дистиллированной воды и добавьте 1-2 капли индикатора на ионы Н+ - метилового красного (или метилового оранжевого). Во вторую пробирку внесите 1-2 мл известковой воды Ca(OH)2 или раствор Ba(OH)2. В третью пробирку поместите небольшое количество кристаллической соды Na2CO3, несколько капель концентрированного раствора уксусной кислоты СН3СООН (сокращенно НАс) и быстро закройте пробкой с газоотводной трубкой. Выделяющийся углекислый газ СО2 пропустите сначала через раствор в первой пробирке – наблюдайте изменение цвета индикатора, а затем через раствор во второй пробирке – наблюдайте образование белого осадка. Если выделение газа идет недостаточно энергично, то подогрейте пробирку. Напишите уравнения всех реакций:

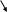 Na2CO3
+ HAc
H2CO3
+ …….
Na2CO3
+ HAc
H2CO3
+ …….
CO2 H2O
CO2 + H2O ⇄ H2CO3
H2CO3 ⇄ H+ + HCO3- ⇄ 2H+ + CO3-
CO2 + Ca(OH)2
Задание 2. Свойства основных оксидов
В фарфоровую чашку поместит стружку магния и сожгите ее: Mg +O2
Полученный белый порошок оксида магния растворите в разбавленной соляной кислоте HCl: MgO + HCl MgCl2 + …….
К полученному раствору соли хлорида магния добавляйте раствор щелочи NaOH до появления студенистого осадка труднорастворимого гидроксида:
MgCl2 + NaOH Mg(OH)2 + …….
Допишите уравнения всех реакций.
Задание 3. Взаимодействие кислот с солями более слабых
или более летучих кислот
Сильные кислоты вытесняют более слабые из их солей:
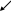
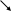 Na2SO3
+ H2SO4
= H2SO3
+ Na2SO4
Na2SO3
+ H2SO4
= H2SO3
+ Na2SO4
SO2 H2O
Na2SiO3 + H2SO4 = H2SiO3 + Na2SO4
Поместите в пробирку несколько кристалликов сульфита натрия Na2SO3 или 2-3 капли насыщенного раствора этой соли. Аккуратно внесите 2-3 капли концентрированной серной кислоты и идентифицируйте выделяющийся сернистый газ по запаху (очень осторожно!).
Налейте в пробирку 1-2 мл насыщенного раствора силиката натрия Na2SiO3 и очень аккуратно внесите 3-5 капель концентрированной серной кислоты. Наблюдайте образование студенистого осадка – геля кремниевой кислоты.
Менее летучие кислоты (H2SO4, H3PO4) вытесняют более летучие (HCl, H2S, HF) из их солей при нагревании:
Na2S + H2SO4 = H2S + Na2SO4
2 NaCl + H2SO4 = 2HCl + Na2SO4
Внесите в пробирку несколько кристалликов хлорида натрия, добавьте 2-3 капли концентрированной серной кислоты. Закройте пробирку пробкой с газоотводной трубкой, осторожно подогрейте и пропустите выделяющийся хлороводород в другую пробирку с дистиллированной водой. Через 1-2 минуты уберите пробирку с водой и только после этого прекратите нагревание (!). Полученный раствор разделите на две пробирки и докажите наличие ионов Н+ с помощью индикатора метилового красного, а ионов С1- - с помощью соли серебра AgNO3.
Задание 4. Свойства солей
Нормальные (средние) соли при растворении в воде полностью распадаются на катионы и анионы, наличие которых можно доказать с помощью различных химических реакций.
В две пробирки поместите по 5 капель раствора одной из следующих солей: а) FeSO4; б) CuC12; в) CuSO4; г) BaC12. Докажите наличие в растворе соответствующих катионов и анионов качественными реакциями с использованием указанных в таблице реагентов. Запишите цвет осадков и уравнения реакций в ионном и молекулярном виде.
Таблица 1
