
- •V. Фотохимические реакции
- •5.1. Основные понятия и сущность фотохимии
- •5.2. Основные законы фотохимии
- •Первичные фотохимические реакции.
- •5.3. Кинетика первичного фотохимического процесса
- •VI. Цепные реакции
- •6.1. Основные понятия и сущность цепного процесса
- •К цепным реакциям относятся:
- •6.2. Механизм цепных химических реакций
- •6.2.1. Зарождение цепей
- •6.2.2. Продолжение цепей
- •Обрыв цепей
- •6.3. Кинетика неразветвленных цепных реакций
- •Принцип стационарности
- •Скорость цепной реакции
- •6.4. Горение и взрыв
6.4. Горение и взрыв
Горением называют химические реакции окисления, которые сопровождаются свечением и значительным выделением теплоты.
Взрывом называют процесс быстрого выделения энергии, сввязанного с внезапным изменением состояния вещества, в резуль-
тате чего в среде образуется ударная или взрывная волна.
При ядерном взрыве совершается почти мгновенный переход внутриядерной энергии в кинетическую энергию их осколков.
Различают цепной и тепловой взрывы. Цепной взрыв или воспламенение наблюдается при протекании цепных разветвленных реакций.
Тепловой взрыв чаще проявляется при высоких температурах, а цепной – при невысоких температурах, т.е. холодные пламена.
Возникновение цепного взрыва объясняется лавинообразным нарастанием числа активных частиц при постоянной температуре.
Тепловой взрыв возникает при обычной (не цепной) экзотермической реакции, когда выделение теплоты при химической реакции становится больше теплоотдачи. При медленном протекании реакции окисления теплота отводится в окружающее пространство и температура в зоне реакции лишь немного выше температуры окружающей среды.
При быстром протекании экзотермических реакций теплота не успевает отводиться в окружающую среду и температура в зоне реакции начинает расти. Дело в том, что скорость реакции и скорость тепловыделения растут с температурой по экспо-ненциальному закону w ~ Ае-E/RT , а скорость теплоотдачи растет с температурой линейно, т.к. тепловой поток пропорционален градиенту температуры. При этом будет наблюдаться саморазогрев реакционной смеси. Различные случаи взаимного расположения кривой тепловыделения и кривых теплоотдачи схематично представлены следующим образом на рис. 6.1.
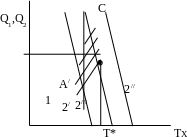 Кривая
1 – кривая тепловыделения.
Кривая
1 – кривая тепловыделения.
Прямые 2/, 2//, 2/// – линии тепло-
отдачи.
От А/ до С саморазогревание в
заштрихованной области.
T* - температура воспламенения.
Рис. 6.1. Взаимное расположение кривых теплоотдачи и
тепловыделения
Разветвленные цепные реакции характеризуются верхним и нижним пределами воспламенения, которые зависят от температуры, формы сосуда и содержания примесей в газовой смеси.
Вообще реакции самовоспламенения были известны давно, но объяснение получили благодаря работам Н.Н. Семенова. В 1926 году открыт нижний предел воспламенения смеси фосфора и кислорода (Харитон, Вальта, Семенов).
Авторы обнаружили, что интенсивное горение паров фосфора в кислороде полностью прекращается при понижении парциального давления О2 до 6,7 Па ~ 0,05 мм рт.ст. (нижний критический предел).
Повышение
давления всего на 0,01 мм рт.ст. приводит
к вспышке. При
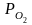 <
6,7 Па смесь (Р + О2)
может существовать бес-конечно долго.
Причем Р1крит
зависит от присутствия инертного газа,
диаметра сосуда, давления паров фосфора.
Это явление объясняется следующим
образом, при низких давлениях, т.е. Р
<
Р1
кр.
среднее число реакций обрыва превышает
число реакций разветвления и горение
невозможно. При Р
>
Р1
крит.
вероятность
обрыва на стенке уменьшается, т.к.
уменьшается вероятность достижения
активной частицей стенки из-за столкновения
с другими частицами. Поэтому начинается
разветвленная реакция с ускорением.
Добавка инертного газа и увеличение
диаметра сосуда затрудняют диффузию
активных центров к стенке, т.е. уменьшается
скорость обрыва и понижается нижний
критический предел.
<
6,7 Па смесь (Р + О2)
может существовать бес-конечно долго.
Причем Р1крит
зависит от присутствия инертного газа,
диаметра сосуда, давления паров фосфора.
Это явление объясняется следующим
образом, при низких давлениях, т.е. Р
<
Р1
кр.
среднее число реакций обрыва превышает
число реакций разветвления и горение
невозможно. При Р
>
Р1
крит.
вероятность
обрыва на стенке уменьшается, т.к.
уменьшается вероятность достижения
активной частицей стенки из-за столкновения
с другими частицами. Поэтому начинается
разветвленная реакция с ускорением.
Добавка инертного газа и увеличение
диаметра сосуда затрудняют диффузию
активных центров к стенке, т.е. уменьшается
скорость обрыва и понижается нижний
критический предел.
Можно построить зависимость давления воспламенения от температуры. Этот график называется полуостровом или треугольником воспламенения (рис.6.2)
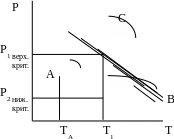
Рис. 6.2. Полуостров воспламенения.
Кривая САВ – граница самовоспламенения горючей смеси.
АВ – нижний предел воспламенения.
Как видим, нижний предел воспламенения слабо зависит от температуры. Рассмотрим систему при температуре Т1. С повышением давления Р > Р1 реакция идет самоускоренно и заканчивается самовоспламенением и взрывом. При достижении верхнего критического предела Р2крит. разветвление цепей затрудняется из-за их обрыва в объеме в результате тройных столкновений (третья частица необходима для стабилизации образующихся продуктов) с частицами примесей. С повышением давления концентрация примесей растет.
Верхний предел Р2 крит. зависит от температуры, природы и количества примесей и мало зависит от размеров, формы сосуда и состояния стенок. Верхний предел будет определяться равенством скорости разветвления цепи и скорости обрыва в объеме. Р2 крит. также растет с температурой.
Важной характеристикой разветвленных цепных реакций является период индукции t:
 ,
,
где t0 – некоторая константа.
Под t понимают время, в течение которого скорость процесса изменяется от незначительной величины до очень большой. Если Р < Р1 или Р > Р2, то t < 0 и процесс затухающий. Если Р1< Р< Р2, то t < 0 и процесс автоускоряющийся.
При Р = Р1 или Р = Р2 t ® ¥.
Для автоускоряющихся процессов было получено выражение для скорости

 ,
,

Dt - время осуществления одного звена;
b - вероятность обрыва;
d - вероятность разветвления.
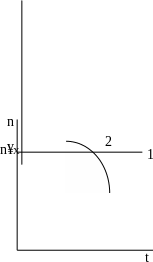
Рис. 6.3. Изменение активных центров со временем
Кривая 1 – стационарная цепная реакция.
Кривая 2 – взрывной процесс.
При d – b < 0 реакции разветвления цепи происходят реже реакций обрыва, и через некоторое время цепная реакция становится стационарной.
При d – b > 0 реакции разветвления происходят чаще реакций обрыва. Число активных частиц постоянно растет, стремясь к бесконечности, т.е. возникает взрыв.
Переход от стационарного режима к взрыву происходит при условии, что d – b = 0.
Зависимость скорости цепных разветвленных реакций от давления изображается графически (рис. 6.4). До наступления взрыва реакция практически полностью отсутствует, а затем скорость резко возрастает.

Рис. 6.4. Зависимость скорости разветвленной реакции от времени.
Эксперимент показывает, что в ряде случаев наблюдается не 2, а 3 предела воспламенения. Например, в реакции О2 + H2S (рис.6.5).
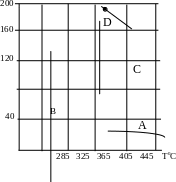

Рис. 6.5. Зависимость границ воспламенения от температуры.
В большинстве случаев третий предел имеет чисто тепловую природу. Но в некоторых случаях, например, при окислении Н2, он имеет цепной характер, т.е. самовоспламенение происходит не за счет ускорения реакции в силу саморазогрева, а за счет развития разветвления реакций. Р3 увеличивается с понижением температуры и зависит от состояния стенок сосуда. При этом на стенках реакционного сосуда осуществляется не только гибель, но и образование активных центров за счет взаимодействия свободных радикалов с адсорбированными молекулами. Кроме того, при высоких давлениях возможны тройные соударения, приводящие к зарождению активных центров.
Критические явления характерны не только для теплового и цепного воспламенения, но и для процессов поджигания и распространения пламени.
