
Билет 1.
В основе МКТ лежит три утверждения : вещество состоит из частиц; эти частицы беспорядочно движутся ; частицы взаимодействуют друг с другом.
Так
как массы молекул очень малы, удобно
использовать в расчетах не абсолютные
значения масс, а относительные.
Относительной молекулярной массой
вещества
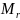 называют отношение массы молекулы (или
атома)
называют отношение массы молекулы (или
атома)
 данного вещества к
данного вещества к
 массы углерода
массы углерода
 :
:
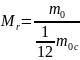
Билет 2.
Вместо реального газа, между молекулы которого действуют сложные силы взаимодействия, мы будем рассматривать как модель- идеальный газ. Идеальный газ – это газ взаимодействия между молекулами которого пренебрежимо мало.
 Основное
уравнение МКТ.
Основное
уравнение МКТ.
Билет 3.
Температура — скалярная физическая величина, описывающая состояние термодинамического равновесия. Как термодинамическая величина температура характеризует тепловое состояние системы и измеряется степенью его отклонения от принятого за нулевое, как молекулярно-кинетическая величина — характеризует интенсивность хаотического движения молекул и измеряется их средней кинетической энергией. Ек = 3/2 kT, где k = 1,38 • 10^(-23) Дж/К и называется постоянной Больцмана.
Измеряется температура термометрами в градусах различных температурных шкал
Существует абсолютная термодинамическая шкала (шкала Кельвина) и различные эмпирические шкалы, которые отличаются начальными точками. До введения абсолютной шкалы температур в практике широкое распространение получила шкала Цельсия (за О °С принята точка замерзания воды, за 100 °С принята точка кипения воды при нормальном атмосферном давлении).
Билет 4.
Уравнение состояния идеального газа — формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой идеального газа. Уравнение имеет вид:
![]()
Процессы, при которых один из параметров p, V или Τ остается постоянным, называют изопроцессами. Законы, описывающие изопроцессы в идеальном газе, были открыты экспериментально задолго до создания MKT идеального газа.
1. Изотермический процесс(закон Бойля-Мариотта)
Для газа данной массы при постоянном давлении температура произведения давления газа на его объем постоянно.

 =>
=>
2. Изобарный процесс(закон Гей-Люссака)
Для газа данной массы при постоянном давлении отношение объема к температуре постоянно.

 =>
=>
3. Изохорный процесс(закон Шарля)
Для газа данной массы отношение давления к температуре постоянно, если объем не меняется.

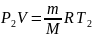 =>
=>
Билет 5.
Вещество в газообразном состоянии, находящееся в динамическом равновесии с жидкостью, называют насыщенным паром. Пар, находящийся при давлении ниже насыщенного, называют ненасыщенным.
С увеличением внешнего давления понижается температура кипения жидкости.
Величина ,характеризующая наличие водяных паров в атмосфере Земли, называется влажностью. Давление водяного пара, находящегося в воздухе при данной температуре, называют абсолютной влажностью, или упругостью водяного пара
Билет 6.
Кристаллические тела. Кристаллы – это твердые тела, атомы или молекулы которых занимают определенные , упорядоченные положения в пространстве. Поэтому кристаллы имеют плоские грани.
Аморфные тела – это твердые тела , атомная структура которых не имеет определенного порядка как у кристаллических тел.
Упругость - свойство материалов восстанавливать форму и объем (у твердых материалов) или только объем (у вязких и жидких) после прекращения действия деформирующих сил.
Твердость - способность материала сопротивляться проникновению в него другого, более твердого тела
Пластичность — способность твердых тел изменять форму без разрушения под воздействием внешних сил (растяжение, сжатие) и сохранять остаточную или полную деформацию после снятия нагрузки
Наиболее простые виды деформации тела в целом:
растяжение-сжатие,
сдвиг,
изгиб,
кручение.
Билет 7.
Механика различает потенциальную энергию и кинетическую энергию . Потенциальная энергия — скалярная физическая величина, характеризующая способность тела совершать работу за счет его нахождения в поле действия сил U
Кинети́ческая эне́ргия — энергия механической системы, зависящая от скоростей движения её точек. Часто выделяют кинетическую энергию поступательного и вращательного движения. Дж
РАБО́ТА, в термодинамике: одна из форм обмена энергией термодинамической системы с окружающими телами;
Работа
при изобарном расширении газа равна
произведению давления газа на изменение
его объема

Коли́чество теплоты́ [Q]— энергия, которую получает или теряет тело при теплопередаче. Количество теплоты является одной из основных термодинамических величин.
