
- •Классификация
- •Пятичленные гетероциклические соединения с одним гетероатомом
- •Способы получения
- •Строение
- •Химические свойства
- •Практическое значение производных пятичленных гетероциклических соединений c одним гетероатомом
- •4. Пятичленные гетероциклические соединения с двумя гетероатомами
- •Шестичленные гетероциклические соединения с одним гетероатомом
- •Пиридин
- •Способы получения
- •Особенности электронного строения
- •Химические свойства
- •Важнейшие производные ряда пиридина
- •Шестичленные гетероциклические соединения с двумя гетероатомами
- •6.1. Пиримидин
- •Упражнения
- •1. Пятичленные гетероциклические соединения с одним и двумя гетероатомами
- •2. Шестичленные гетероциклические соединения с одним и двумя гетероатомами
- •Задания для самостоятельной работы студентов
- •1. Пятичленные гетероциклические соединения с одним и двумя гетероатомами
- •2. Шестичленные гетероциклические соединения с одним и двумя гетероатомами
- •Итоговый контроль знаний студентов по учебной дисциплине «гетероциклические соединения» (банк тестовых заданий)
- •Рекомендуемая литература
- •Содержание
Гетероциклические соединения – циклические соединения, содержащие в кольцах не только атомы углерода, но и атомы других элементов.
Установлено, что в образовании циклов могут принимать участие практически все многовалентные атомы, но наибольшее значение имеют гетероциклические соединения, в циклы которых входят атомы O, N, и S.
Классификация
Наиболее распространены в природе пяти- и шестичленные кислород-, азот- и серосодержащие гетероароматические соединения, которые отличаются друг от друга устойчивостью цикла. Эти соединения подразделяются на группы в зависимости от:
− размера цикла;
− характера гетероатомов;
− количества гетероатомов;
− наличия конденсированных систем, состоящих из одного или нескольких колец бензола и гетероцикла;
− наличия конденсированных систем, состоящих из двух или более гетероциклов.
По размеру цикла и характеру гетероатомов:
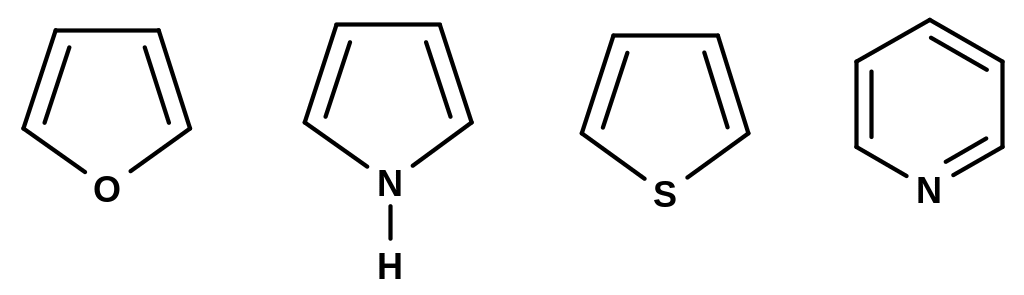
фуран пиррол тиофен пиридин
По количеству и характеру гетероатомов (кислород-, азот- и серусодержащие ГЦС):

пиррол пиразол имидазол оксазол тиазол пиримидин
Конденсированные системы из бензола и гетероцикла:
 индол
акридин
хинолин
индол
акридин
хинолин
(бензопиррол) (бензопиридин) (дибензопиридин)

пурин (цикл пиримидина + цикл имидазола)
Пятичленные гетероциклические соединения с одним гетероатомом
Эти соединения отвечают общей формуле:

К простейшим ароматическим пятичленным гетероциклическим соединениям с одним гетероатомом относятся фуран, пиррол и тиофен.

X = O (фуран) X = N−H (пиррол) X = S (тиофен)
Способы получения
Фуран, пиррол и тиофен представляют собой бесцветные, легкокипящие жидкости, встречающиеcя в каменноугольной смоле, откуда могут быть выделены (за исключением фурана). В практике их обычно получают реакцией циклизации соответствующих 1,4-дикарбонильных соединений путем нагревания их либо с серной кислотой (для получения фурана), либо с аммиаком (для получения пиррола), либо с сульфидом фосфора (для получения тиофена):

Кроме того, по реакции Ю. К. Юрьева фуран, пиррол и тиофен могут переходить друг в друга при нагревании до 450 °С над оксидом алюминия (III). Реакция идет по схеме:

Строение
По типу связей и химическому поведению эту группу пятичленных гетероциклических соединений следует отнести к ароматическим системам. Их ароматический характер, как и у бензола, определяется прежде всего наличием кольцевого секстета р-электронов. При этом все атомы гетероциклической системы (4 атома углерода и гетероатом) находятся в состоянии sp2-гибридизации. Гибридизованные орбитали при аксиальном перекрывании формируют плоский σ-скелет молекулы, а негибридизованные 2рz-орбитали, ориентированные перпендикулярно плоскости цикла, перекрываясь латерально, образуют ароматический секстет:

хх

sp2-гибридная
орбиталь
σ-скелет
молекулы

образование π-электронного
секстета молекулы
Аналогично бензолу фуран, пиррол и тиофен подчиняются правилу ароматичности Хюккеля при n = 1.
Электронные смещения в молекулах пятичленных гетероциклов обусловлены двумя противоположными по направлению эффектами: положительным мезомерным эффектом (p,π-сопряжение) и отрицательным индукционным, направленным из кольца к гетероатому. За счет преобладающего +М-эффекта четыре атома углерода кольца имеют большую электронную плотность, чем атомы углерода бензола. Такое направление электронных смещений подтверждается и расчетами эффективных зарядов методом молекулярных орбиталей (на примере молекулы пиррола):

Это указывает на то, что пятичленные гетероароматические соединения являются электроноизбыточными системами: шесть р-электронов в их молекулах делокализованы между пятью атомами цикла. Ароматический характер фурана, пиррола и тиофена подтверждает и теория резонанса. Структура всех пятичленных гетероциклических соединений – динамическое образование, которое можно представить в виде набора предельных резонансных структур. Наложением предельных резонансных структур друг на друга получаем мезоструктуру, которая обычно характеризует распределение электронной плотности в молекуле.

-I-эффект << +М-эффекта
Исходя из электронного строения пятичленных гетероциклов можно сделать следующие выводы:
1. Молекула плоская, что определяется sp2-гибридизацией всех атомов цикла.
2. Электронная плотность в молекуле распределена неравномерно и смещена в сторону атомов углерода цикла. Это подтверждается расчетом эффективных зарядов на атомах методом МО.
3. Неравномерность распределения электронной плотности, в отличие от бензола, определяет полярный характер молекул рассматриваемых гетероциклических соединений. При этом на величины и направленность дипольных моментов оказывает влияние не только электроотрицательность гетероатомов, но и характер электронных смещений в молекуле. Это хорошо видно из сравнения дипольных моментов фурана, пиррола и тиофена с таковыми у их полностью восстановленных аналогов. Если на величину и направление дипольных моментов последних оказывает влияние только отрицательный индуктивный эффект (–I) гетероатомов, то у первых – значительное снижение дипольного момента обусловлено противоположным по направлению и значительным по величине +М-эффектом. Ниже приведены наблюдаемые дипольные моменты у восстановленных и невосстановленных пятичленных гетероциклов.

тетрагидрофуран тетрагидропиррол тетрагидротиофен
μ =1,68 D μ = 1,57 D μ = 0,52 D

фуран пиррол тиофен
μ = 0,71 D μ = 1,8 D μ = 1,87 D
–I > +M –I < +M
4. Одним из основных признаков ароматических соединений является выравненность всех связей в цикле. В пятичленных гетероциклах они не могут быть выравненными, поскольку длины связей С−С и С−Х неравнозначны. Следовательно, структуры фурана, пиррола и тиофена представляют собой неправильные пятиугольники.

фуран пиррол

тиофен
5. Циклическая делокализация р-электронов кольца и их количественное соответствие правилу Хюккеля (при n = 1) указывает на то, что рассматриваемые гетероциклические соединения являются ароматическими системами. Об этом свидетельствуют их величины энергии сопряжения. Они меньше, чем у бензола (150 кДж/моль), и их значения уменьшаются в ряду тиофен (120 кДж/моль), пиррол (110 кДж/моль), фуран (90 кДж/моль). Это связано с различием в электроотрицательностях гетероатомов, входящих в состав циклов. Естественно, что в этой же последовательности уменьшается и ароматический характер этих соединений.
6. Поскольку пятичленные гетероароматические соединения являются π-избыточными, для них должно быть характерно облегченное (по сравнению с бензолом) протекание SE- и А-реакций. При этом электрофильная атака ориентирована на Сα-замещение, активность которой уменьшается в ряду фуран – пиррол – тиофен. А-процессы, приводящие к разрушению ароматического π-электронного секстета (например, гидрирование), должны протекать для этих соединений в более мягких, чем для бензола, условиях.
Показатели строения и
реакционной способности Тиофен Пиррол Фуран
Электроотрицательность гетероатома 2,5 3,0 3,5
Величина энергии делока-
лизации (Есопр), кДж/моль 130 110 90
Ароматичность у м е н ь ш а е т с я
Отрицательный индуктивный
эффект (–I-эффект) в о з р а с т а е т
Положительный мезомерный
эффект (+М-эффект) у м е н ь ш а е т с я
Участие в реакциях присоедине-
ния (А-реакциях) о б л е г ч а е т с я
Участие в реакциях электрофиль-
ного замещения (SE-реакциях) о б л е г ч а е т с я
