
- •Содержание:
- •1.Определение. Общая формула.
- •2.Классификация. Номенклатура. Важнейшие представители (международное и тривиальное название).
- •3. Изомерия.
- •1. Изомерия углеродного скелета
- •2. Изомерия положения функциональных групп
- •3. Оптическая изомерия
- •4.Строение.
- •5.Получение в лабораторных и промышленных условиях.
- •6.Физические свойства.
- •7. Химические свойства.
- •8.Применение.
6.Физические свойства.
α-Аминокислоты представляют собой бесцветные кристаллические вещества. Большинство из них легко растворимо в воде. Многие α-аминокислоты обладают сладким вкусом, иногда с некоторым неприятным привкусом, у некоторых аминокислот горький вкус.
α-Аминокислоты плавятся с разложением при высоких и довольно близких температурах. Поэтому определение температуры плавления недостаточно для идентификации, и для этой цели обычно пользуются определением Rf аминокислоты с помощью бумажной хромотографии.
Солеобразный характер α-аминокислот проявляется и в их физических свойствах: аминокислоты обладают высокими температурами плавления, нелетучи, в большинстве своем они растворимы в воде и плохо или совсем нерастворимы в неполярных органических растворителях. Вследствие амфотерности аминокислот они способны нейтрализовать небольшие количества других кислот и оснований в водных растворах, и поэтому их растворы обладают буферными свойствами (сохраняют постоянные значения pH).
Производные α-аминокислот, которые не могут образовывать биполярные ионы (например, их эфиры H2NCH2COOC2H5 или ацетильные производные CH3CONHCH2COOH), растворимы в органических растворителях и могут перегоняться в вакууме без разложения.
Во всех (кроме глицина) природных α-аминокислотах имеются ассиметрические α-углеродные атомы:

Так же как для углеводов, буквы L и D обозначают принадлежность данной аминокислоты к L- или D- ряду, а знаки (+) и (-) указывают направление вращения. За исходное соединение, со строением которого принято сравнивать строение аминокислоты, условно принимают L- и D-молочные кислоты; конфигурации этих кислот в свою очередь установлены по L- и D- глицериновым альдегидам.
Аминокислоты, входящие в состав белков и большинства других природных соединений, относятся к L- отряду, D- формы аминокислот встречаются сравнительно редко. Они входят в состав лишь некоторых антибиотиков, например грамицидина-С.
Интересно отметить различие в физиологическом действии аминокислот L- и D- рядов. Большинство аминокислот L- ряда имеет сладкий вкус, а аминокислоты D- ряда – горькие или безвкусные.
Как правило, D- аминокислоты не усваиваются животными организмами. Синтетически полученные аминокислоты являются, естественно, рацематами. Для разделения их на оптические антиподы пользуются химическими, микробиологическими и главным образом ферментативными методами.
7. Химические свойства.
Подобно обычным карбоновым кислотам, аминокислоты вступают во многие реакции, свойственные соединениям, содержащим карбоксил. Они образуют соли, эфиры, амиды и галогенангидриды. При образовании эфиров, амидов и галогенангидридов кислот реагирует неионизированная карбоксильная группа, а потому с аминокислотами эти реакции идут труднее, чем с алифатическими кислотами. Наряду с этими реакциями для аминокислот характерны и реакции, свойственные аминам.
Реакции карбоксильной группы аминокислот.
1. Аминокислоты, как и алифатические кислоты, образуют соли с основаниями. Кроме обычных солей, аминокислоты могут в известных условиях образовывать внутрикомплексные соли с катионами тяжелых металлов. Для всех α-аминокислот очень характерны красиво кристаллизующиеся, интенсивно окрашенные в синий цвет внутрикомплексные (хелатные) соли меди:

2. Эфиры аминокислот получают (обычно в виде солей), действуя на аминокислоты спиртом в присутствии хлороводорода:

3. Галогенангидриды α-аминокислот получают действием тионилхлорида или окись-трихлорида фосфора. Сами они неустойчивы и существуют только в виде солей. Поэтому реакцию проводят, предварительно защитив аминогруппу ацилированием:

Реакции аминогруппы аминокислот.
1. С минеральными кислотами аминокислоты дают соли, подобно аминам.
При действии азотистой кислоты образуются оксикислоты и выделяются азот и вода:
![]()
Этой реакцией пользуются для количественного определения аминных групп в аминокислотах, а также в белках и продуктах их распада.
3.Аминокислоты реагируют с хлорангидридами и ангидридами кислот, образуя N-ацильные производные аминокислот:

N-Ацильные производные аминокислот имеют большое значение при синтезе пептидов.
4. При взаимодействии с CH2O (в растворе pH 9) аминокислоты с первичной аминогруппой образуют N-метиленовые производные, обладающие слабой основностью:

В этих производных, обладающих свойствами обычных карбоновых кислот, карбоксильная группа может быть оттитрована обычным способом.
Реакции, характерные для α-аминокислот.
Реакция декарбоксилирования.
При отщеплении CO2 под действием особых ферментов – декарбоксилаз или некоторых микроорганизмов α-аминокислоты превращаются в амины:
![]()
Так, лизин и орнитрин, декарбоксилируясь при гниении белков, образуют диамины: путресцин NH2(CH2)4NH2 и кадаверин NH2(CH2)5NH2, долгое время ошибочно считавшиеся трупными ядами.
Реакция дезаминирования:

Реакция переаминирования:

Реакции дезаминирования, декарбоксилирования и переаминирования могут протекать в животных и растительных организмах в очень мягких условиях под действием специфических ферментов.
Окрашивание с цингидрином.
В качестве специфического реактива на α-аминокислоты используется нингидрин. При нагревании его с α-аминокислотами возникает фиолетовое окрашивание различных оттенков. Нингидрин широко используется для проявления хроматограмм на бумаге и электрофореграмм α-аминокислот. Общая схема реакции:

Превращения аминокислот при нагревании.
При нагревании α-аминокислоты, а еще легче их сложные эфиры образуют циклические амиды, которые называются дикетопиперазинами:
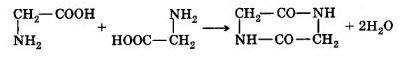
β-Аминокислоты образуют α, β –ненасыщенные кислоты с отщеплением аминогруппы и атома водорода в α –положении:
![]()
γ- и δ- Аминокислоты, как и соответствующие оксикислоты, легко отщепляют воду и циклизуются, образуя внутренние амиды – лактамы, например:

В тех случаях, когда амино- и карбоксильные группы разделены пятью и более углеродными атомами, при нагревании происходит поликонденсация (с отщеплением молекулы воды) по типу «голова – хвост» с образованием полимерных полиамидных цепей.
