
- •Лабораторный практикум Часть 2
- •Предисловие
- •Лабораторная работа № 9 качественный и количественный анализ сплавов с помощью стилоскопа
- •Краткая теория
- •Порядок выполнения работы
- •Контрольные вопросы
- •Лабораторная работа № 12 исследование аберраций оптических систем
- •Краткая теория
- •Геометрические аберрации
- •Аберрации, обусловленные широкими пучками лучей
- •Сферическая аберрация
- •Аберрации, обусловленные тонкими внеосевыми
- •Астигматизм наклонных лучей
- •Искривление плоскости изображения
- •Дисторсия изображений
- •Описание методики измерений
- •Лабораторная работа № 13 измерения спектральных характеристик светофильтров
- •Краткая теория
- •Устройство спектрофотометра spekol
- •Порядок выполнения работы
- •Контрольные вопросы
- •Перейдя от n2 к n и от к 0, получим кривую, изображенную на рис. 3 (дан лишь участок кривой в области одной из резо-
- •Описание гониометра г5
- •Задание 1. Определение преломляющего угла призмы
- •Задание 2. Определение показателя преломления призмы
- •Задание 3. Определение дисперсии призмы
- •Рекомендуемая литература
- •Лабораторные работы
- •Часть 2
Министерство образования
Российской Федерации
Кубанский государственный университет
Н.М. Богатов, Л.Ф. Добро,
М.П. Матвеякин, О.Е. Митина
ОПТИКА
Лабораторный практикум Часть 2
Краснодар 2003
УДК 535 (076.5)
ББК 22.34
Д56
Рецензенты:
Кафедра физики Кубанского государственного
технологического университета
Доктор физико-математических наук, профессор Кубанского
государственного аграрного университета
В.В. Фомин
Печатается по решению редакционно-издательского совета
Кубанского государственного университета
Богатов Н.М., Добро Л.Ф., Матвеякин М.П.,
Митина О.Е.
Д56 Оптика: Лабораторный практикум. Ч. 2/ Кубанский
госуниверситет, 2003 – 104 с.
ISBN 5-8209-0085-5
Дается описание 7 лабораторных работ по курсу «Оптика». Приведены теоретические сведения, методические указания по выполнению работ, контрольные вопросы и список рекомендуемой литературы.
Адресуется студентам физико-технических факультетов.
УДК 535 (076.5)
ББК 22.34
ISBN 5-8209-0085-5 Кубанский государственный
университет, 2003
Предисловие
Лабораторный практикум по курсу “Оптика” (Часть 2) является продолжением вышедшего ранее практикума.
При составлении второй части сохранены общая схема описания лабораторных работ и оформление пособия, принятые в первой части.
Лабораторный практикум по курсу “Оптика” включает описание 15 лабораторных работ (№ 1–8 – часть 1; № 9–15 – часть 2), которые охватывают основные вопросы, предусмотренные программой курса.
Все рекомендации по подготовке, выполнению и сдаче лабораторных работ, изложенные во введении к части 1 практикума, в полном объеме применимы и в данном случае.
Лабораторная работа № 9 качественный и количественный анализ сплавов с помощью стилоскопа
Приборы и принадлежности
Cтилоскоп СЛ-11А, образцы стали, таблица сравнения спектральных линий.
Цель работы – анализ сплавов с помощью стилоскопа.
Краткая теория
Слово "атом" в переводе с греческого означает "неделимый". Под атомом долгое время, вплоть до начала ХХ в., подразумевали мельчайшие неделимые частицы вещества. К началу ХХ в. в науке накопилось много фактов, говоривших о сложном строении атомов.
Большие успехи в исследовании строения атомов были достигнуты в опытах английского ученого Э. Резерфорда по расссеянию ‑частиц при прохождении через тонкие слои вещества. В этих опытах узкий поток –частиц, испускаемых радиоактивным веществом, направлялся на тонкую золотую фольгу. За фольгой помещался экран, способный светиться под ударами быстрых частиц. Было обнаружено, что большинство –частиц отклоняется от прямолинейного распространения после прохождения фольги, т.е. рассеивается, а некоторые –частицы вообще отбрасываются назад. Рассеяние –частиц Резерфорд объяснил тем, что положительный заряд не распределен равномерно в шаре радиусом 10 –10 м, как предполагали ранее, а сосредоточен в центральной части атома – атомном ядре. При прохождении около ядра ‑частица, имеющая положительный заряд, отталкивается от него, а при попадании в ядро – отбрасывается в противоположном направлении. Так ведут себя частицы, имеющие одинаковый заряд, следовательно, существует центральная положительно заряженная часть атома, в которой сосредоточена значительная масса атома. Расчеты показали, что для объяснения опытов нужно принять радиус атомного ядра равным примерно 10 ‑15м.
Резерфорд предположил, что атом устроен подобно планетарной системе. Суть модели строения атома по Резерфорду заключается в следующем: в центре атома находится положительно заряженное ядро, в котором сосредоточена вся масса, вокруг ядра по круговым орбитам на больших расстояниях вращаются электроны (как планеты вокруг Солнца). Заряд ядра совпадает с номером химического элемента в таблице Менделеева.
Планетарная модель атома по Резерфорду не смогла объяснить ряд известных фактов. Электрон, имеющий заряд, должен за счет кулоновских сил притяжения упасть на ядро, а атом это устойчивая система. При движении по круговой орбите, приближаясь к ядру, электрон в атоме должен излучать электромагнитные волны всевозможных частот, т.е. излучаемый свет должен иметь непрерывный спектр. На практике же получается иное: электроны атомов излучают свет, имеющий линейчатый спектр. Разрешить противоречия планетарной ядерной модели строения атома первым попытался датский физик Н. Бор.
В основу своей теории Бор положил два постулата.
Первый постулат: атомная система может находиться только в особых стационарных или квантовых состояниях, каждому из которых соответствует своя энергия; в стационарном состоянии атом не излучает.
Второй постулат: при переходе из одного стационарного состояния в другое испускается или поглощается квант электромагнитного излучения. Энергия фотона равна разности энергий атома в двух состояниях:
h = Еm – Еn, где h – постоянная Планка ( h = 6,62·10-34 Дж·с).
При переходе электрона с ближней орбиты на более удаленную атомная система поглощает квант энергии. При переходе с более удаленной орбиты электрона на ближнюю орбиту по отношению к ядру атомная система излучает квант энергии.
Теория Бора позволила объяснить существование линейчатых спектров.
Спектр излучения (или поглощения) – это набор волн определенных частот, которые излучает (или поглощает) атом данного вещества.
Спектры бывают сплошные, линейчатые и полосатые.
Сплошные спектры излучают все вещества, находящиеся в твердом или жидком состоянии. Сплошной спектр содержит волны всех частот видимого света и поэтому выглядит как цветная полоса с плавным переходом от одного цвета к другому в таком порядке: красный, оранжевый, желтый, зеленый, синий и фиолетовый (каждый охотник желает знать, где сидит фазан).
Линейчатые спектры излучают все тела вещества в атомарном состоянии. Атомы всех веществ излучают свойственные только им наборы волн вполне определенных частот. Как у каждого человека свои личные отпечатки пальцев, так и у атома данного вещества свой, характерный только для него спектр. Линейчатые спектры излучения выглядят как цветные линии, разделенные промежутками. Природа линейчатых спектров объясняется тем, что у атомов конкретного вещества существуют только ему свойственные стационарные состояния со своей характерной энергией, а следовательно, и свой набор пар энергетических уровней, которые может менять атом. Электрон в атоме может переходить только с одних определенных орбит на другие, вполне определенные орбиты для данного химического вещества.
Полосатые спектры излучаются молекулами. Выглядят полосатые спектры подобно линейчатым, только вместо отдельных линий наблюдаются отдельные серии линий, воспринимаемые как отдельные полосы.
Характерным является то, что какой спектр излучается данными атомами, такой же и поглощается, т.е. спектры излучения по набору излучаемых частот совпадают со спектрами поглощения. Поскольку атомам разных веществ соответствуют свойственные только им спектры, то существует способ определения химического состава вещества методом изучения его спектров. Этот способ называется спектральным анализом. Спектральный анализ применяется для определения химического состава ископаемых руд при добыче полезных ископаемых, для определения химического состава звезд, атмосфер планет; является основным методом контроля состава вещества в металлургии и машиностроении.
Спектральный метод анализа заключается в определении химического состава сплава по наличию характерных линий элементов в его спектре излучения и в установлении количественного содержания этих элементов в сплаве по интенсивности линии спектра.
Устройство стилоскопа
Стилоскоп СЛ-11А с фотометрическим клином предназначен для быстрого визуального качественного и полуколичественного спектрального анализа сталей и цветных сплавов в видимой области спектра. Спектральный диапазон стилоскопа 3900–7000 Å, прибор построен по автоколлимационной схеме с горизонтальным расположением элементов.
Оптическая схема прибора показана на рис. 1. Свет от дуги системой из трех линз 1, 2, 3 равномерно заполняет входную щель 4, отражательная призма 5 направляет лучи света на объектив 10, в фокусе которого помещена щель 4. Полученный параллельный пучок света падает на диспергирующие призмы 11 и 12. Большой катет призмы 12 с преломляющим углом 31° посеребрен, поэтому лучи, отражаясь от него, проходят в обратном направлении через призмы на объектив и падают на прямоугольную призму 9 и зеркало 8, которые направляют их в окуляр 7. В фокальной плоскости окуляра расположен фотометрический клин 6.
Электрическая схема стилоскопа представляет собой схему низковольтного генератора, который может работать в режиме дуги или искры.
Стилоскоп состоит из осветительной схемы, щели с объективом, отражательной призмы, диспергирующей системы и окулярной головки. Все части помещены внутри корпуса 6. На основании рис. 2 смонтирован столик для установки образцов.
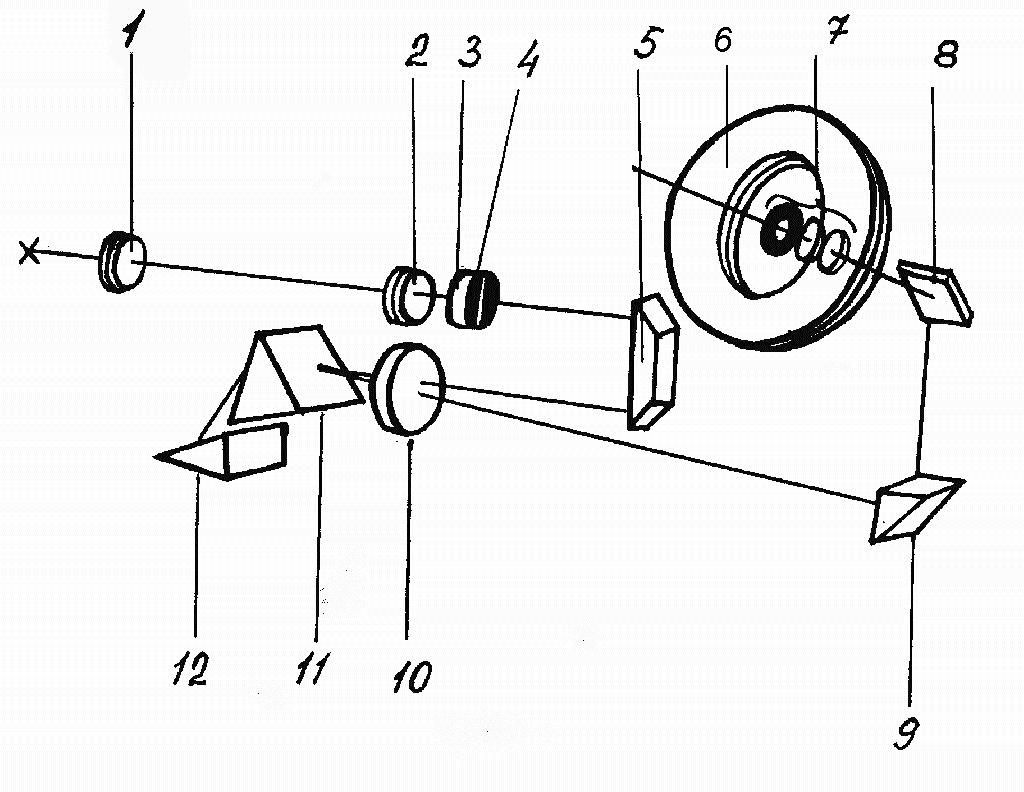
Рис. 1. Оптическая схема стилоскопа
Осветительная система состоит из конденсоров 1, 2, 3 (рис. 1) с фокусным расстоянием соответственно 70, 50, 80 см. Автозащитная щель постоянной ширины 0,015 мм нанесена на стеклянной пластинке, склеенной с 3-й линзой осветителя. Отражательная призма 5 направляет лучи, идущие от щели, на объектив.
Диспергирующая система состоит из двух призм: одна 11 с преломляющим углом 63° закреплена на мостике неподвижно, другая 12 с преломляющим углом 31° вместе со своим мостиком может поворачиваться, вследствие чего спектр перемещается в поле зрения окуляра. Поворот призмы осуществляется маховичком 12 (рис. 2, а), на котором нанесены равномерная шкала 10 и шкала 11 с символами химических элементов.
Символами обозначены группы спектральных линий, используемых для анализа стали на соответствующие примеси. При совмещении символа с отсчетным штрихом барабана в поле зрения окуляра появляется соответствующая группа линий. При вращении маховичка 12 происходит перефокусировка объектива, так как при повороте призмы поворачивается кулачок, который толкает прибор на тубусе объектива, устанавливая объектив в соответствующее положение.
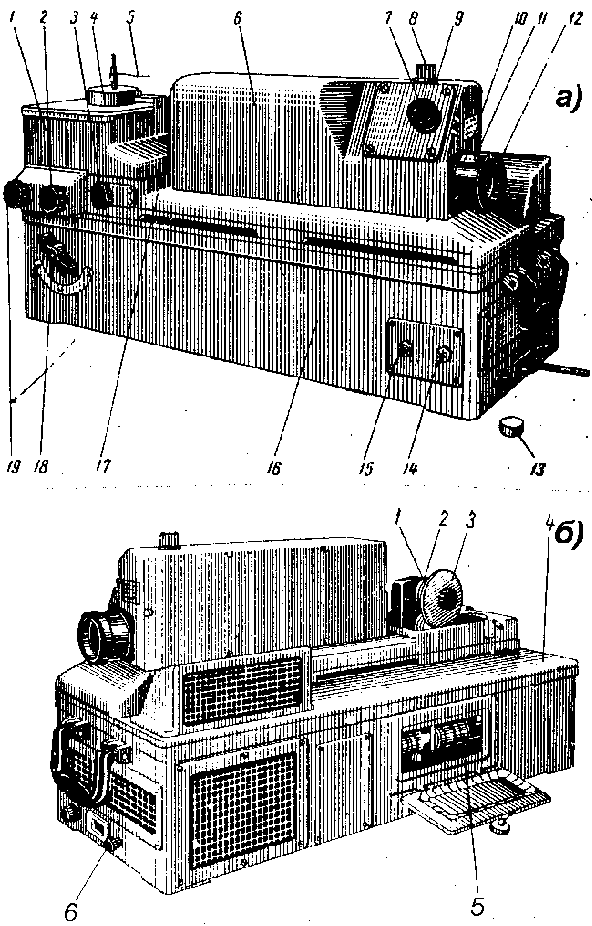
Рис. 2. Общий вид стилоскопа
На кронштейне окулярной головки расположены: прямоугольная призма, фотометрический клин со шкалой и окуляр 7 в оправе.
Для удобства работы имеются два сменных окуляра с различным увеличением. Окуляр с увеличением 20 применяется при изучении спектров, богатых линиями стали и т.п., окуляр с увеличением 13,5 – при анализе цветных металлов.
Фотометрический клин помещен в плоскости изображения спектра и расположен вдоль спектральных линий в виде узкой полоски в центре поля зрения. Перемещение клина производится маховичком 8 и отсчитывается по шкале, наблюдаемой в поле зрения окуляра. В тех случаях, когда нужно работать без фотометрического клина, следует маховичком 8 привести в поле зрения диафрагму, соответствующую установленному окуляру. Для этого необходимо установить точку, нанесенную на маховичке, против соответствующего обозначения (13,5 или 20) на шкале 9.
На основании расположен кронштейн 2 (рис. 2, б) с держателем, на который можно установить дисковый электрод 3 или цилиндрический электрод. Держатель электродов можно перемещать по высоте маховичком 19 (рис. 2, а) в направлении, перпендикулярном к оптической оси, маховичком 3 и в случае применения дискового электрода можно вращать маховичком 2.
Для защиты от радиопомех держатель электродов закрывается съемным кожухом, служащим одновременно и столиком 4 для установки образцов. На столик можно установить образцы любых размеров и форм. Для крепления мелких деталей служит пружинный прижим 5. Расстояние между образцом и электродом, равное 3 мм, устанавливается с помощью съемного шаблона 13, помещаемого вместо образца на столик. Электрод подводится к шаблону до упора.
В качестве источника возбуждения спектра применяется генератор. Генератор обеспечивает работу в режимах искры и дуги. Напряжение от генератора к электроду подводится высоковольтным проводом через контакт на кронштейне держателя, а к образцу, устанавливаемому на столике, через заземленный корпус прибора.
Методика работы
Анализируемый образец помещают на столике стилоскопа. Поверхность образца, очищенная от следов краски и окалины, должна быть расположена на уровне поверхности столика так, чтобы она перекрывала отверстие в столике. Если образец проходил обработку, то этот слой должен быть удален при зачистке. Зачистка производится напильником.
После того как установлен по шаблону сменный электрод, а анализируемый образец помещен на столик, зажигают дугу, для этого переключатель 18 (рис. 2, а) устанавливают в положение «дуга» или «искра», переключатель 14 в положение «2А» или «4А», проверяют, заземлен ли генератор, подводят провод питания от сети и устанавливают переключатель 15 в положение "ВКЛ".
Наблюдая в окуляр прибора за требуемой частью спектра, маховичком 12 приводят ее на середину поля зрения.
Установкой окуляра добиваются максимальной резкости спектральных линий, после чего приступают к оценке содержания элементов в анализируемой пробе.
Порядок выполнения работы
Каждому химическому элементу соответствуют определенные линии спектра излучения. Следовательно, присутствие в спектре линий данного элемента указывает на наличие его в анализируемом образце. По яркости спектральных линий можно судить о количестве вещества в анализируемом образце: чем больше содержание примеси, тем интенсивнее линии ее спектра. Однако спектральные линии примеси надо наблюдать изолированно от других линий спектра, так как интенсивности линий зависят не только от содержания примесей в образце, но и от условий возбуждения спектра, кроме того, довольно трудно судить об интенсивности отдельной линии, не сравнивая с каким-либо стандартом. Интенсивность спектральных линий оценивают путем сравнения их с другими спектральными линиями, интенсивности которых приняты за стандарт.
Таким образом, о концентрации искомой смеси судят по отношению интенсивностей двух линий рассматриваемого спектра: линий примеси и линий сравнения, за которые принимают линии основы сплава.
Для анализа сплава стали на элементы Сг – хром, Ni – никель, W – вольфрам, Мо – молибден, Мn – марганец, Температура – титан, Si – кремний используют несколько групп линий (табл. 3), расположенных в различных частях спектра. Каждая линия данной группы отмечается отдельным номером. Обычно каждая группа линий пригодна для определения одной области концентраций.
Для анализа на какой-либо элемент находят в табл. 2 группы линий, характеризующих данный элемент, и на шкале 11 ставят соответствующий символ химического элемента, при котором данный участок спектра попадает в поле зрения окуляра. После того как линии, приведенные в табл. 1, найдены в спектре, оценивают их интенсивность по отношению к интенсивности соответствующих линий железа.
В табл. 1, соответствующей рисункам табл. 3, приведены соотношения между интенсивностями используемых для анализа спектральных линий данного элемента и железа, а также соответствующее этим соотношениям процентное содержание анализируемого элемента в образце.
Слева в табл. 2 всегда стоит линия определяемого элемента, справа – привлекаемая дня сравнения линия железа. Символ "=" означает, что интенсивности обеих линий равны, "<" – интенсивность линии слева, меньше интенсивности линии справа, ">" – интенсивность линии справа меньше интенсивности линии слева (интенсивность линии, стоящей слева, больше интенсивности линии, стоящей справа), "" означает соответственно больше или равно интенсивности линии, стоящей справа от значка.
Для каждого образца оценку надо делать по всем линиям, приведенным в таблице соответствующей группы. Анализ для молибдена надо проводить в первый момент после включения дуги, так как интенсивность линий молибдена наиболее устойчива в этот момент. Анализ на никель проводится в течение 1–2 мин. после включения дуги.
Анализ V, Сг, Мn, W, Ti производится после 40–60 с с момента включения дуги. Для каждого образца составляется таблица, куда заносятся результаты измерений.
Задание
Проанализировать на содержание V, Cr, Mn, W, Ti стальные образцы.
Контрольные вопросы
Какой спектр испускают раскаленные металлы?
Какая разница между сплошным и линейчатым спектром?
Почему каждый элемент имеет свои характерные линии?
В чем состоит преимущество качественно-спектрального анализа перед химическим?
Для чего предназначен прибор СЛ-11А? Как выглядит оптическая схема стилоскопа?
Что является диспергирующим элементом стилоскопа?
Какова роль призм стилоскопа?
В какой спектральной области работает стилоскоп СЛ-11А, используемый в лабораторной работе?
Какой источник света используется в приборе, каковы его характеристики?
С какой точностью можно проводить измерение?
Рекомендуемая литература
[10], [12], [14].
Таблица 1
Длины волн спектральных линий легирующих элементов и железа
Наименовние элементов, № групп |
№ линии по табл. 3 |
в Å легирующих элементов |
№ линии по табл. 3 |
в Å линий железа |
1 |
2 |
3 |
4 |
5 |
V-2 |
1 |
4379,24 |
4 |
4375,93 |
|
2 |
4384,73 |
|
|
|
3 |
4714,41 |
|
|
|
|
|
|
|
Ni-1 |
1 |
4714,41 |
4 |
4707,28 |
|
|
|
3 |
4709,0 |
|
|
|
2 |
4710,3 |
|
|
|
|
|
Mn-1 |
5 |
4739,0 |
6 |
4736,78 |
|
4 |
4754,0 |
8 |
4789,0 |
|
3 |
4762,37 |
7 |
5789,65 |
|
2 |
4756,42 |
|
|
|
1 |
4783,43 |
|
|
|
|
|
|
|
W-2 |
1 |
4843,0 |
8 |
4786,8 |
|
|
|
7 |
4789,65 |
|
|
|
|
|
V-1 |
1 |
4875,48 |
4 |
4871,33 |
|
|
|
3 |
4872,14 |
|
|
|
2 |
4878,22 |
|
|
|
|
|
Cr-4 |
1 |
4922,3 |
2 |
4919,0 |
|
|
|
3 |
4920,51 |
|
|
|
|
|
Ti-1 |
1 |
4999,5 |
4 |
4994,13 |
|
|
|
2 |
5001,87 |
|
|
|
3 |
5006,13 |
|
|
|
|
|
Ni-2 |
1 |
5035,36 |
2 |
5041,0 |
|
|
|
3 |
5041,76 |
|
|
|
|
|
W-1 |
1 |
5053,3 |
4 |
5049,8 |
|
2 |
5054,62 |
3 |
5051,64 |
|
|
|
|
|
Cr-1 |
1 |
4922,3 |
4 |
5198,7 |
|
|
5206,0 |
|
|
|
2 |
5208,4 |
3 |
5202,3 |
|
2 |
5054,62 |
3 |
5051,64 |
Окончание табл. 1
1 |
2 |
3 |
4 |
5 |
|
|||||
|
|
|
|
|
|
|||||
Сr-3 |
1 |
5345,8 |
8 |
5324,2 |
||||||
|
|
2 |
5348,3 |
7 |
5338,9 |
|||||
|
|
|
|
6 |
5339,9 |
|||||
|
|
|
|
5 |
5341 |
|||||
|
|
|
|
4 |
5371,4 |
|||||
|
|
|
|
|
|
|||||
Сr-2 |
1 |
5409,8 |
4 |
5405,8 |
||||||
|
|
|
|
3 |
5415,2 |
|||||
|
|
|
|
2 |
5416,9 |
|||||
|
|
|
|
|
|
|||||
Mo |
1 |
5533,0 |
4 |
5497,5 |
||||||
|
|
2 |
5570,5 |
3 |
5504,5 |
|||||
|
|
|
|
8 |
5569,6 |
|||||
|
|
|
|
6 |
5572,8 |
|||||
|
|
|
|
7 |
5576,1 |
|||||
|
|
|
|
|
|
|||||
Мn-2 |
3 |
6013,5 |
5 |
|
||||||
|
|
2 |
6016,2 |
4 |
|
|||||
|
|
1 |
6021,79 |
|
|
|||||
|
|
|
|
|
|
|||||
Si |
1 |
6346,7 |
5 |
|
|
|||||
Таблица 2
Соотношение интенсивности спектральных линий
определяемого элемента
Содержание элементов в % |
№ группы |
Линия сравнения |
1 |
2 |
3 |
Cr |
||
0,05 |
Cr-1 |
1=4 |
0,1 |
Cr-1 |
1<3 |
0,2 |
Cr-1 |
1=3 |
0,3 |
Cr-1 |
1=7 |
0,7 |
Cr-3 |
2=7 |
1,0 |
Cr-2 |
1=2 |
Cr-3 |
1=6 27 |
|
2,5 |
Cr-2 |
1=3 |
Cr-3 |
2=6 |
|
4,0 |
Cr-2 |
1=4 |
Cr-3 |
1=8 2=5 |
|
4,5 |
Cr-3 |
615 2>7 |
7 |
Cr-3 |
1>8 2<8 |
10,0 |
Cr-3 |
1=4 2=8 |
Cr-4 |
1<2 |
|
15,0 |
Cr-4 |
1=2 |
20,0 |
Cr-3 |
1>4 24 |
Cr-4 |
3>1>2 |
|
30,0 |
Cr-3 |
1>>4 2>4 |
Cr-4 |
1=3 |
|
Mn |
||
0,15 |
Mn-1 |
1=8 |
0,3 |
Mn-2 |
2=4 |
0,35 |
Mn-1 |
2<7 |
0,5 |
Mn-1 |
4=7 |
0,7 |
Mn-1 |
37 |
Mn-2 |
3=4 |
|
Продолжение табл. 2
1 |
2 |
3 |
||
1 |
Mn-1 |
2=7 |
||
1,3 |
Mn-1 |
4=6 |
||
Mn-2 |
1=5 |
|||
2 |
Mn-1 |
3=6 |
||
4 |
Mn-1 |
5=7 |
||
10 |
Mn-1 |
56 |
||
Mo |
||||
0,1 |
|
1=3 |
||
0,2 |
|
1=4 |
||
0,4 |
|
2=7 |
||
0,8 |
|
2=8 |
||
1,5 |
|
3=6 |
||
3 |
|
1=6 15 |
||
Ni |
||||
0,2 |
Ni-1 |
1<3 |
||
0,5 |
Ni-1 |
13 |
||
1,5 |
Ni-1 |
1=2 |
||
3 |
Ni-1 |
4>12 |
||
|
Ni-2 |
1=2 |
||
9 |
Ni-2 |
1=3 |
||
15 |
Ni-2 |
2=4 |
||
W |
||||
1 |
W-2 |
1<8 |
||
2 |
W-1 |
13 |
||
3 |
W-2 |
1=3 (4>12) |
||
6 |
W-1 |
1<4 |
||
8 |
W-1 |
14 2<3 |
||
13 |
W-1 |
1>4 2=3 |
||
18 |
W-1 |
14 2>3 |
||
V |
||||
0,15 |
V-2 |
1=4 |
||
0,3 |
V-2 |
2=4 |
||
0,5 |
V-2 |
3=4 |
||
Окончание табл. 2
|
1 |
2 |
3 |
|||
|---|---|---|---|---|---|---|
0,8 |
V-1 |
2=2 |
|
|||
1,5 |
V-1 |
2=3 |
|
|||
2,5 |
V-2 |
1=4 |
|
|||
Ti |
|
|||||
0,1 |
|
1=2 |
|
|||
0,3 |
|
1=4 |
|
|||
0,8 |
|
1=3 |
|
|||
1,5 |
|
1>3 |
|
|||
Si |
|
|||||
0,5 |
|
1<<4 |
|
|||
1 |
|
4<1<3 |
|
|||
2,5 |
|
31<5 2<4 |
|
|||
Таблица 3
Таблица сравнения спектральных линий для определения марки стали на стилоскопе с дугой переменного тока с постоянным медным дисковым электродом


Лабораторная работа № 10
ОПРЕДЕЛЕНИЕ ПОСТОЯННОЙ
СТЕФАНА-БОЛЬЦМАНА ПРИ ПОМОЩИ
ОПТИЧЕСКОГО ПИРОМЕТРА
Приборы и принадлежности
Лампа накаливания с вольфрамовой спиралью; оптический пирометр с исчезающей нитью – ОППИР-017Э; ЛАТР (лабораторный автотрансформатор); вольтметр; амперметр; блок питания пирометра.
Цель работы – ознакомление с принципом работы оптического пирометра, определение яркостной температуры и постоянной в законе Стефана–Больцмана.
