
- •Министерство образования российской федерации череповецкий государственный университет
- •По дисциплине «Химия»
- •Моль. Молярная масса
- •Законы газового состояния
- •Эквивалент. Молярная масса эквивалента
- •Закон эквивалентов
- •Математически закон эквивалентов для условной реакции вида
- •По закону эквивалентов
- •Вычислим мэ(о), зная что степень окисления кислорода в оксиде равна –2
- •Дополнительные задания
- •Литература
- •Содержание
Закон эквивалентов
Массы реагирующих друг с другом веществ, а также массы продуктов этой реакции пропорциональны молярным массам эквивалентов этих веществ.
Математически закон эквивалентов для условной реакции вида
А + В С + D
можно выразить следующим образом
![]() или
или
![]() .
.
Если в реакции участвуют газообразные вещества, то закон эквивалентов целесообразнее записать как соотношение объемов
![]() .
.
Наконец, когда один из участников реакции - газ, а другой – твердый реагент, то формула, выражающая закона эквивалентов, принимает вид
![]() .
.
Пример 1. при сгорании 5 г металла образуется 9,44 г оксида металла. Вычислите молярную эквивалентную массу металла. Определите относительную атомную массу металла, если его валентность в оксиде равна трем.
Р е ш е н и е
По закону эквивалентов
МЭ(Ме)
=
![]() .
.
Молярную эквивалентную массу оксида можно представить как сумму МЭ металла и кислорода
МЭ(оксида) = МЭ(Ме) + МЭ(О).
Вычислим мэ(о), зная что степень окисления кислорода в оксиде равна –2
МЭ(О)
=
![]() .
.
Тогда
МЭ(Ме)
=
![]() или МЭ(Ме)
= 9 г/моль.
или МЭ(Ме)
= 9 г/моль.
Относительную атомную массу металла найдем по формуле
Аr(Ме) = МЭ(Ме)В = 9 3 = 27.
Пример 2. Мышьяк образует оксид, содержащий 65,2 % мас. мышьяка. Вычислите молярную эквивалентную массу мышьяка и определите простейшую формулу оксида.
Р е ш е н и е
1. Оксид мышьяка состоит из элементов As и О. Тогда закон эквивалентов можно записать так
![]() .
.
Отношение масс элементов в оксиде равно отношению массовых долей (% мас.) этих элементов, то есть
![]() .
.
Тогда
МЭ(As)
=
![]() .
.
2. Для того чтобы записать химическую формулу оксида, вычислим валентность мышьяка в оксиде по формуле
В =
![]() .
.
Следовательно, химическая формула оксида мышьяка As2O5 .
Пример 3. На восстановление 3,6 г оксида металла израсходовано 1,7 дм3 водорода при н.у. Найдите молярную эквивалентную массу металла.
Р е ш е н и е
1. По закону эквивалентов
МЭ(оксида)
=
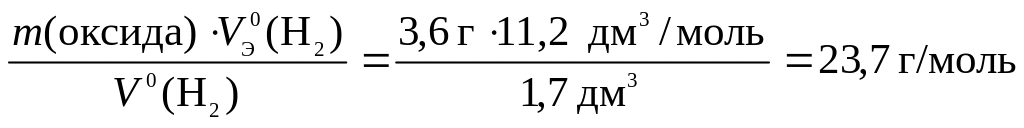 .
.
2. Так как МЭ(оксида) это сумма молярных эквивалентных масс металла и кислорода, то
МЭ(Ме) = МЭ(оксида) - МЭ(О) = 23,7 – 8 = 15,7 г/моль.
Пример 4. Из 3,31 г нитрата металла получено 2,78 г хлорида металла. Вычислите молярную эквивалентную массу оксида металла.
Р е ш е н и е
Закон эквивалентов в данном случае примет вид
![]() .
.
МЭ хлорида и нитрата металла можно представить таким образом
МЭ(нитрата) = МЭ(Ме) + МЭ(NO3-) ,
МЭ(хлорида) = МЭ(Ме) + МЭ(Cl-) .
Вычислим молярные эквивалентные массы ионов нитрата и хлорида
МЭ(NO3-)
=
![]() ,
,
МЭ(Cl-)
=
![]() .
.
Тогда по закону эквивалентов
![]() . Отсюда МЭ(Ме)
= 104 г/моль,
. Отсюда МЭ(Ме)
= 104 г/моль,
а молярная эквивалентная масса оксида металла равна
МЭ(оксида) = МЭ(Ме) + МЭ(О) = 104 + 8 = 112 г/моль.
З А Д А Ч И
1. 2,14 г металла вытесняют из кислоты 2 дм3 водорода при нормальных условиях. Определите молярную эквивалентную массу оксида металла.
2. На восстановление 3,6 г оксида металла израсходовано 1,7 дм3 водорода при нормальных условиях. Вычислите молярную эквивалентную массу металла.
3. Олово образует два оксида. Первый содержит 78,8 % мас. олова, а второй - 88,2 % мас. Вычислите молярные эквивалентные массы олова в данных оксидах. Составьте простейшие формулы оксидов.
4. Из 1,35 г оксида металла получается 3,15 г его нитрата. Вычислите молярную эквивалентную массу металла.
5. Из 1,3 г гидроксида металла получается 2,85 г его сульфата. Вычислите молярную эквивалентную массу металла.
6. Одно и тоже количество металла соединяется с 0,0006 кг кислорода и с 0,009534 кг галогена. Вычислите молярную эквивалентную массу галогена.
7. Вычислите молярную эквивалентную массу металла, если на восстановление 1,017 г его оксида израсходовали 0,28 дм3 водорода при нормальных условиях.
8. В 2,48 г оксида одновалентного металла содержится 1,84 г металла. Вычислите молярную эквивалентную массу металла и его оксида. Чему равна молярная масса металла?
9. На сжигание 1,5 г двухвалентного металла требуется 0,69 дм3 кислорода при нормальных условиях. Вычислите молярную эквивалентную массу и атомную массу данного металла.
10. Из 3,31 г сульфата металла получается 2,08 г хлорида металла. Определите молярную эквивалентную массу металла.
11. На нейтрализацию 0,943 г фосфористой кислоты Н3РО3 израсходовано 1,291 г гидроксида калия. Вычислите молярную эквивалентную массу кислоты и определите ее основность в данной реакции.
12. При окислении 16,74 г металла образовалось 21,54 г оксида. Вычислите молярную эквивалентную массу металла и его оксида.
13. При взаимодействии 3,24 г металла (валентность равна 2) с кислотой выделилось 4,03 дм3 водорода при нормальных условиях. Определите молярную эквивалентную массу металла и его относительную атомную массу.
14. Сульфид мышьяка содержит 38 % мас. серы. Молярная масса эквивалента серы равна 16 г/моль. Вычислите молярную эквивалентную массу мышьяка и запишите химическую формулу сульфида.
15. На нейтрализацию 9,797 г ортофосфорной кислоты израсходовали 7,998 г NaOH. Вычислите молярную эквивалентную массу кислоты и ее основность в данной реакции.
16. 3,04 г некоторого металла вытесняют 0,252 г водорода, 26,965 г серебра и 15,885 г меди из соединений этих элементов. Вычислите МЭ данных металлов.
17. Оксид металла содержит 28,57 % мас. кислорода, а его фторид содержит 48,72 % мас. фтора. Вычислите молярные эквивалентные массы металла и фтора.
18. Вычислите молярную эквивалентную массу металла и его оксида, если на восстановление 1,8 г оксида израсходовано 833 см3 водорода при нормальных условиях.
19. Чему равна молярная эквивалентная масса меди, если цинк массой 13 кг замещает в растворе соли медь массой 12,633 кг? Эквивалент цинка принять равным ½.
20. 0,49 г хлорида металла взаимодействует с AgNO3, при этом получено 0,863 г AgCl. Вычислите эквивалентную массу металла.
21. На восстановление 7,09 г оксида двух валентного металла требуется 0,31 г водорода. Вычислите эквивалентную массу металла и его оксида. Чему равна атомная масса металла? Назовите этот металл.
22. Определите молярные эквивалентные массы металла и серы, если 3,24 г металла образуют 3,48 г оксида и 3,72 г сульфида.
23. Для растворения 16,8 г металла потребовалось 14,4 г серной кислоты. Определите молярную эквивалентную массу металла и объем выделившегося водорода (н.у.).
24. Некоторое количество металла, молярная эквивалентная масса которого равна 27,9 г/моль, вытесняет из кислоты 700 см3 водорода (н.у.). Определите массу металла.
25. Серная и ортофосфорная кислоты имеют одинаковую молярную массу. Каково отношение масс этих кислот, пошедших на нейтрализацию одного и того же количества щелочи, если образовались соответственно сульфат и дигидроортофосфат?
26. Оксид марганца содержит 22,56 % мас. кислорода. Вычислите молярную эквивалентную массу и стехиометрическую валентность марганца в оксиде.
27. Оксид марганца содержит 50,50 % мас. кислорода. Вычислите молярную эквивалентную массу марганца в оксиде. Составьте химическую формулу оксида.
28. Металл образует оксид Me2O3, содержащий 68,4 % мас. металла. Вычислите атомную массу этого металла. Какой это металл?
29. Молярная эквивалентная масса хлора равна 35,5 г/моль. Молярная масса атомов меди равна 63,5 г/моль. Молярная эквивалентная масса хлорида меди равна 99,5 г/моль. Запишите формулу хлорида меди.
30. Вычислите молярную эквивалентную и атомную массу двухвалентного металла, если на окисление 8,34 г этого металла израсходовано 680 см3 кислорода. Назовите этот металл.
