
- •III. Сопряженные системы с замкнутой цепью
- •1. Строение бензола
- •Современная теория строения бензола
- •Понятие ароматичности
- •Изомерия производных бензола
- •Полизамещенные производные бензола
- •2. Общий механизм реакций электрофильного замещения в
- •3. Влияние природы заместителей на направление реакций электрофильного замещения в бензольном кольце Ориентация замещения
- •Электроноакцепторные заместители
- •4. Ароматичность гетероциклических соединений
- •5. Основные термины.
- •6. Эталонное решение задач
- •Решение
- •Эталонное решение задач второго типа
- •Решение
- •Решение
- •Пространственное строение органических
- •Виды изомерии
- •Классификация изомеров.
- •2. Конформационная изомерия
- •Конформации циклических соединений
- •2. Конфигурационная изомерия
- •Проекционные формулы э. Фишера
- •Правила пользования проекционными формулами Фишера
- •4. Пространственное строение молекул и их биологическая активность
- •5. Основные термины.
- •6. Эталонное решение задач эталонное решение задач первого типа
- •Решение.
- •Эталонное решение задач второго типа
- •V. Углеводороды
- •Классификация углеводородов Углеводороды
- •1. Алканы Химические свойства (Sr-реакции)
- •Радикальное замещение у sp3 -гибридизованного атома углерода (sr - реакции)
- •Галогенирование высших алканов
- •Реакции окисления
- •2. Химические свойства циклоалканов
- •3. Электрофильное присоединение к алкенам и циклоалкенам (ае - реакции)
- •Какие экспериментальные данные могут служить доказательством такого механизма?
- •Присоединение водородсодержащих соединений к несимметричным алкенам
- •Реакции электрофильного присоединения против правила Марковникова
- •4. Электрофильное присоединение к диеновым
- •Реакции присоединения к 1,3 – бутадиену
- •Радикальное присоединение и электрофильное
- •5.1 Реакции присоединения (аr - реакции)
- •5.2 Реакции электрофильного замещения (se - реакции)
- •Химические свойства толуола
- •Нафталин в живом организме
- •6. Основные термины
- •7. Эталонное решение задач
- •Решение
- •1. Напишите реакции взаимодействия хлора с пропеном:
- •Решение
- •2. Присоедините бромоводород к следующим алкенам:
- •Решение
- •Решение
- •Решение
- •Эталонное решение задач третьего типа
- •Решение
- •Решение
- •Решение
- •Решение
- •Литература
- •Дополнительная.
Электроноакцепторные заместители
Ориентанты IIго рода
Это группы, которые своими индуктивными и мезомерными эффектами уменьшают электронную плотность кольца (дезактивируют кольцо), создают недостаток электронной плотности в орто- и пара- положениях. Вследствие такого распределения заряда в кольце мета-положение становится более выгодным для атаки электрофилом. Поэтому эти заместители называют мета- ориентантами. К ним относятся:
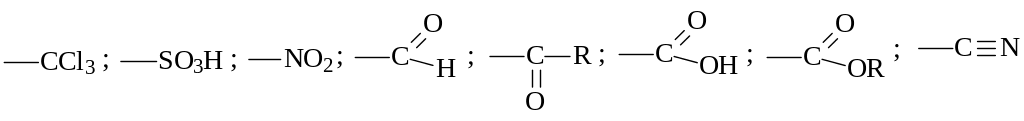
Рассмотрим, например, влияние карбоксильной группы на распределение электронной плотности в молекуле бензойной кислоты. За счёт электроноакцепторного влияния этой группы уменьшается электронная плотность всего кольца в целом, но в орто и пара положениях недостаток электронной плотности больше, чем в мета- положении, и поэтому новая электрофильная частица замещает атом водорода у мета-углеродного атома.
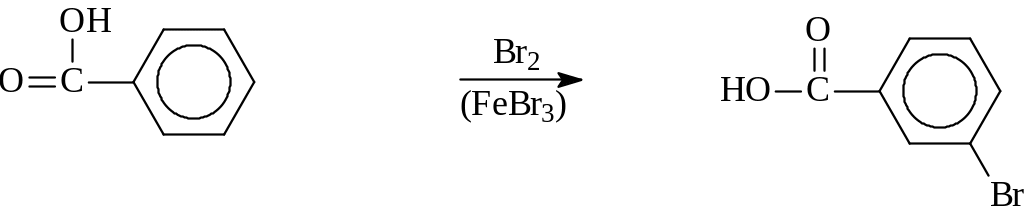
мета-бромбензойная кислота
(3-бромбензойная кислота)
Так как всё кольцо обеднено электронами, реакции замещения затруднены. На основании всего вышеизложенного можно сделать следующие выводы:
любой заместитель, находящийся в бензольном кольце, влияет на распределение электронной плотности в нём;
ориентанты Iго рода увеличивают электронную плотность кольца, создают максимум плотности в орто- и пара- положениях, направляют новую электрофильную частицу в эти положения и облегчают реакции электрофильного замещения (кроме галогенов);
ориентанты IIго рода уменьшают электронную плотность кольца, создают минимум электронной плотности в орто- и пара- положениях и некоторый относительный избыток электронной плотности в мета- положении. Они направляют новую электрофильную частицу в мета- положение и затрудняют реакции электрофильного замещения.
4. Ароматичность гетероциклических соединений
Как уже отмечалось выше, правило Хюккеля применимо к любой (не обязательно содержащей бензольное кольцо) плоской циклической системе, в которой -электроны сопряжены и число их равно 4n + 2
Этим требованиям отвечают и гетероциклические соединения. У гетероциклических соединений в цикле, помимо атомов углерода, имеется один (или несколько) гетероатомов. . Чаще всего гетероатомами бывают атомы азота, кислорода и серы.
Изображённые ниже молекулы таких гетероциклических соединений, как фуран, тиофен, пиррол, имидазол, тиазол имеют плоское строение, и пара электронов на р-орбитали sp2- гибридизованного гетероатома входит в состав ароматической шестерки электронов.
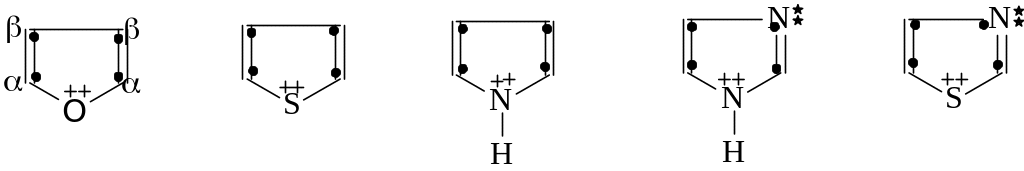
фуран тиофен пиррол имидазол тиазол
Электроны атомов углерода, вовлечённые в ароматическую электронную структуру, обозначены точками, а электроны гетероатома, используемые для дополнения ароматического секстета, обозначены крестиком. Так же, как "бензоидные" ароматические системы, эти гетероциклические соединения отвечают всем требованиям Хюккеля и поэтому относятся к ароматическому ряду. Но, в отличие от бензола, в этих гетероциклических структурах нет такой выровненности электронной плотности, атомы углерода неравноценны. Поэтому различают α-атомы и β-атомы кольца (показаны на примере фурана, но справедливы для тиофена и пиррола). В молекулах имидазола и тиазола два гетероатома. π-Электроны одного атома вовлечены в ароматический секстет, а неподелённые пары электронов другого гетероатома (обозначены звёздочками) свободны и могут участвовать в кислотно-основных превращениях, при этом ароматичность этих соединений не нарушается.
В отличие от них, фуран, тиофен и пиррол основными свойствами не обладают, так как их неподеленные пары электронов участвуют в образовании ароматической π- системы.
Однако следует отметить, что образование ароматической шестёрки электронов с участием π-электронов гетероатомов накладывает определённый отпечаток на природу этих гетероциклических соединений. Так, они легко окисляются, вступают в реакции электрофильного замещения только в мягких условиях. Все химические особенности этих соединений мы рассмотрим ниже, в главе, посвящённой химии гетероциклических соединений.
Шестичленные гетероциклические соединения - пиридин и пиримидин - ароматические гетероаналоги бензола. Свободные электронные пары атомов азота в молекулах пиридина и пиримидина не используются для образования единой ароматической системы, поэтому они могут присоединять протон, и, следовательно, в кислотно-основных превращениях пиридин и пиримидин проявляют свойства оснований.
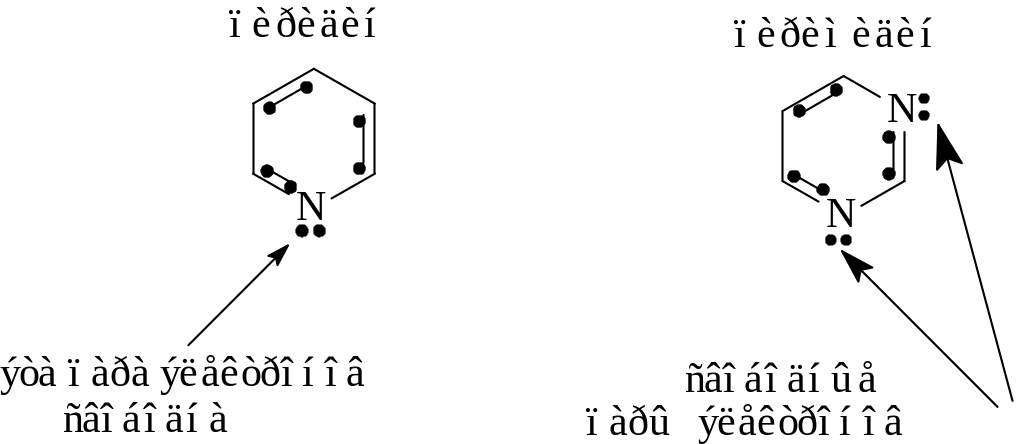
Следовательно, различие между пирролом с одной стороны и пиридином и пиримидином с другой состоит в том, что атомы азота, входящие в циклы этих соединений, имеют разную химическую природу.
Пиридиновый азот может присоединять протон, пиррольный азот - нет.
Соединения, содержащие пиридиновый азот, могут участвовать в кислотно - основных превращениях, выступая в них в качестве оснований, а соединения, содержащие пиррольный азот, основными свойствами не обладают.
Хинолин и изохинолин - ароматические 10-π- электронные системы, являются азотными аналогами нафталина.

Нафталин Хинолин Изохинолин
Они содержат пиридиновый азот, могут присоединять протон и, следовательно, являются основаниями.
Рассмотрев строение гетероциклических соединений, можно сделать следующий основной вывод: понятие ароматичности не ограничивается лишь бензоидными структурами, а распространяется и на многие вещества, так называемого «небензоидного» строения. Во всех случаях, при решении вопроса о принадлежности данного соединения к ароматическому ряду, необходимо помнить о том, что главным критерием является выполнение правила Хюккеля.
