
- •Вопросы входного контроля
- •Вязкость жидкости
- •Поверхностное натяжение
- •Зависимость коэффициента поверхностного натяжения от температуры
- •Зависимость коэффициента поверхностного натяжения от примесей
- •Определение вязкости жидкости
- •Практическая часть
- •Ход работы
- •Определение вязкости жидкости методом Стокса
- •Практическая часть
- •Лабораторная работа №8 Определение коэффициента поверхностного натяжения жидкостей разными методами
- •Определение коэффициента поверхностного натяжения методом отрыва капель
- •Теоретическое обоснование метода
- •Практическая часть
- •Определение коэффициента поверхностного натяжения методом отрыва кольца
- •Теоретическое обоснование метода
- •Практическая часть
- •Вопросы выходного контроля
Поверхностное натяжение
Поверхностное натяжение является важной силовой и энергетической характеристикой жидкости и играет большую роль в медицине. Коэффициент поверхностного натяжения биологических жидкостей в некоторых случаях может служить диагностическим фактором. Так, например, при заболевании желтухой поверхностное натяжение мочи резко уменьшается вследствие появления в моче желчных кислот. При диабете и некоторых других заболеваниях повышается содержание липазы в крови. О содержании липазы судят по изменению коэффициента поверхностного натяжения раствора трибутилена при добавлении в него крови. Силы взаимодействия между молекулами жидкости значительно превышают силы взаимодействия между молекулами газа. Рассмотрим действие этих сил на молекулы, находящиеся внутри и на поверхности жидкости.
Молекула, находящаяся внутри жидкости, взаимодействует с окружающими ее молекулами. Так как взаимодействия симметричны, то равнодействующая равна нулю (рис. 2а) Для молекулы, находящейся вблизи поверхности, симметрия нарушается и возникает сила, нескомпенсированная действием других молекул и направленная внутрь жидкости - эта сила вызывает давление на нижележащие слои и называется силой молекулярного давления. (Рис. 2а, 2б).
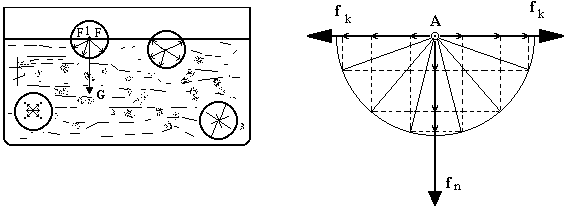
а) б)
Рис. 2.
Несмотря на то, что сила очень велика, она действует только на молекулы самой жидкости в радиусе сферы молекулярного взаимодействия и не ощущается телами, погруженными в жидкость.
При отсутствии внешних сил молекулы жидкости стремятся занять положение, соответствующее минимуму потенциальной энергии, поэтому жидкость в свободном состоянии стремится занять минимальную площадь поверхности и принимает форму шара. Поверхностный слой уплотняется, что похоже на упругую пленку, в которой действуют упругие силы (силы поверхностного натяжения, направленные по касательной поверхности).
Е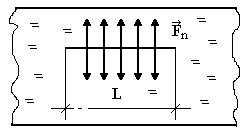 сли
условно выбрать на поверхности жидкости
отрезок длиной «L», то межмолекулярные
силы Fn
можно
изобразить стрелками, перпендикулярными
отрезку (рис. 3а).
сли
условно выбрать на поверхности жидкости
отрезок длиной «L», то межмолекулярные
силы Fn
можно
изобразить стрелками, перпендикулярными
отрезку (рис. 3а).
Рис. 3а.
Соотношение
= F/L (5), коэффициент поверхностного
натяжения, где
![]()
![]() .
.
Его можно рассматривать как силовую характеристику поверхностного натяжения жидкости. Так как молекулы поверхностного слоя обладают большей потенциальной энергией по сравнению с молекулами, находящимися внутри жидкости, то для увеличения площади поверхности жидкости необходимо совершить работу против сил поверхностного натяжения. Значит, коэффициент поверхностного натяжения жидкости можно рассматривать как энергетическую характеристику поверхностного слоя жидкости.
= А/S
=
![]() (6)
(6)
Действие сил поверхностного натяжения легко продемонстрировать на мыльных пленках (рис. 3б).
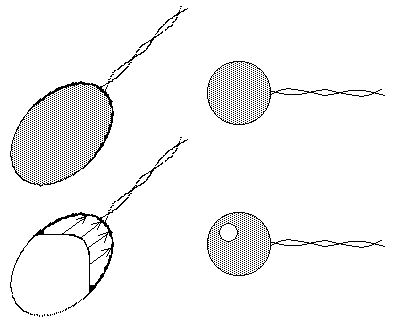
Рис. 3б.
Зависимость коэффициента поверхностного натяжения от температуры
Вблизи поверхностного слоя жидкости находится насыщенный пар этой жидкости. Насыщенным паром называется пар, находящийся в динамическом (подвижном) равновесии со своей жидкостью. Это значит, сколько молекул в единицу времени вылетит из жидкости, столько же обратно возвращается. В этом случае скорость испарения равна скорости конденсации.
При низких температурах, когда плотность насыщенного пара над жидкостью мала, можно пренебречь взаимодействием молекул в поверхностном слое жидкости с молекулами пара. С ростом температуры растет плотность насыщенного пара, а плотность жидкости уменьшается. Поэтому равнодействующая сила молекулярного притяжения, действующая на каждую молекулу поверхностного слоя, уменьшается. При критической температуре, когда исчезает различие между жидкостью и ее паром, эта равнодействующая обращается в нуль, исчезает поверхностный слой, обращается в нуль поверхностная энергия и, соответственно, обращается в нуль коэффициент поверхностного натяжения.
Вдали от критической температуры коэффициент поверхностного натяжения убывает при возрастании температуры.
