
- •Энергетический баланс окисления насыщенных жк с четным количеством атомов углерода
- •Энергетический баланс окисления насыщенных жк с нечетным количеством атомов углерода
- •Энергетический баланс окисления ненасыщенных жк с четным количеством атомов углерода
- •4.Пути использования ацетил КоА. Механизм образования и значение ацетоуксусной кислоты. Биосинтез кетоновых тел. Кетоацидоз.
- •5.Биосинтез и катаболизм глицерофосфолипидов
- •6.Биосинтез холестерола: стадии процесса, регуляция. Транспорт холестерола (лпонп, лпнп, лпвп, роль лхат).
- •7. Гиперхолестеролемия и развитие атеросклероза. Лпвп как антиатерогенный фактор
- •10.Регуляция липидного обмена. Роль печени в нарушении липидного обмена. Жировая дистрофия печени и факторы ее вызывающие.
- •1. Центральный уровень регуляции липидного обмена
- •I фаза голодания
- •II фаза голодания
- •III фаза голодания
- •3. Клеточный (метаболический) уровень регуляции липидного обмена
- •12.Классификация гормонов, их роль и место в регуляции обменных процессов Гипоталамус и его гормоны. Роль гипоталамуса в иерархии регуляторных систем.
- •2. Классификация гормонов по месту синтеза
- •3. Классификация гормонов по биологическим функциям
- •13.Характеристика и функции гормонов передней доли гипофиза. Регуляция образования и механизм действия. Соматотропный гормон.
- •14.Ось гипоталамус-гипофиз-щитовидная железа. Гормоны щитовидной железы: структура, синтез, транспорт и метаболизм. Функция щитовидной железы и роль ее гормонов. Заболевания щитовидной железы.
- •1. Биосинтез йодтиронинов
- •2. Регуляция синтеза и секреции йодтиронинов
- •3. Механизм действия и биологические функции йодтиронинов
- •15.Ось гипоталамус-гипофиз-гонады. Женские половые гормоны. Гормоны плаценты и их роль. Система мать-плацента-плод.
- •16.Ось гипоталамус-гипофиз-гонады. Мужские половые гормоны. Применение анаболиков в медицине.
- •2. Передача сигналов через внутриклеточные рецепторы
- •18.Гормоновитамин а, структура, суточная потребность проявления авитаминоза и гипервитаминоза, биологические функции.
- •19.Гомоновитамин д, его роль в регуляции обмена кальция и фосфатов. Суточная потребность. Авитаминоз д, его проявления. Понятие о гипервитаминозе д.
- •Первичная недостаточность надпочечников (болезнь Аддисона)
- •Вторичная недостаточность надпочечников
- •Врождённая гиперплазия надпочечников
- •Гиперпродукция глюкокортикоидов (гиперкортипизм)
- •21.Гормоны мозгового слоя надпочечников. Синтез и секреция катехоламинов. Механизм действия, биологические функции.
- •22.Гормоны поджелудочной железы и желудочно-кишечного тракта. Инсулин, строение, синтез и секреция, регуляция. Механизм действия инсулина. Глюкагон. Эффекты глюкагона.
4.Пути использования ацетил КоА. Механизм образования и значение ацетоуксусной кислоты. Биосинтез кетоновых тел. Кетоацидоз.
На первой стадии из двух молекул ацетил-КоА образуется ацетоацетил-КоА:
![]()
Реакция катализируется ферментом ацетил-КоА-ацетилтрансферазой (ацетоацетил-КоА-тиолазой). Затем ацетоацетил-КоА взаимодействует еще с одной молекулой ацетил-КоА. Реакция протекает под влиянием фермента гидроксиметилглутарил-КоА-синтазы:
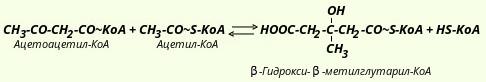
Образовавшийся β-гидрокси-β-метилглутарил-КоА способен под действием гидроксиметилглутарил-КоА-лиазы расщепляться на ацетоацетат и ацетил-КоА:

Ацетоуксусная кислота способна восстанавливаться при участии НАД-зависимой D-β-гидроксибутиратдегидрогеназы; при этом образуется D-β-гидроксимасляная кислота (D-β-гидроксибутират). Следует еще раз подчеркнуть, что фермент специфичен по отношению к D-стереоизомеру и не действует на КоА-эфиры:
![]()
Существует также и второй путь синтеза кетоновых тел. Образовавшийся путем конденсации двух молекул ацетил-КоА ацетоацетил-КоА способен отщеплять коэнзим А и превращаться в свободную ацетоуксусную кислоту. Этот процесс катализируется ферментом ацетоацетил-КоА-гидролазой (деацилазой):
![]()
Однако второй путь образования ацетоуксусной кислоты не имеет существенного значения, так как активность деацилазы в печени низкая. В крови здорового человека кетоновые тела содержатся лишь в очень небольших концентрациях. При патологических состояниях (например, у лиц с тяжелой формой сахарного диабета, при голодании, а также у животных с острым аллоксановым диабетом) концентрация кетоновых тел в крови увеличивается и может достигать 20 ммоль. Такое состояние, которое получило название кетоза, возникает в тех случаях, когда скорость образования кетоновых тел превышает способность периферических тканей их утилизировать.
В последние годы начали постепенно накапливаться данные, указывающие на важную роль кетоновых тел в поддержании энергетического гомеостаза. Кетоновые тела - своего рода поставщики топлива для мышц, мозга, почек и действуют, возможно, как часть регуляторного механизма с обратной связью, предотвращая чрезвычайную мобилизацию жирных кислот из жировых депо. Печень в этом смысле является исключением, она не использует кетоновые тела в качестве энергетического материала.
В периферических тканях β-гидроксимасляная кислота окисляется до ацетоуксусной кислоты, а последняя активируется с образованием соответствующего КоА-эфира (ацетоацетил-КоА).
Существует два ферментативных механизма активации ацетоуксусной кислоты. Первый путь -это использование АТФ и HS-КоА аналогично тому, как при активации жирных кислот:
![]()
Реакция катализируется ферментом ацил-КоА-синтетазой, или тиокиназой. Второй путь активации - это перенос КоА от сукцинил-КоА на ацетоуксусную кислоту:
![]()
Данная реакция катализируется ферментом сукцинил-КоА-ацетоацетат-трансферазой. Возможно, что биологически более важным является именно этот путь активации ацетоацетата.
Образовавшийся в ходе этих реакций ацетоацетил-КоА подвергается далее тиолитическому расщеплению с образованием двух молекул ацетил-КоА:
![]()
А уже ацетил-КоА, как это известно, окисляется в цикле трикарбоновых кислот (цикл Кребса) до СО2 и Н20.
Кетоацидоз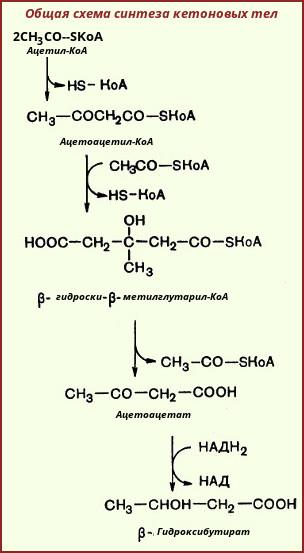
В норме концентрация КТ в крови составляет 1—3 мг/дл (до 0,2 мМоль/л), но при голодании значительно увеличивается. Увеличение концентрации КТ в крови называют кетонемией. При кетонемии развивается кетонурия - выделение КТ с мочой. Накопление КТ в организме приводит к кетоацидозу, так как КТ (кроме ацетона) являются водорастворимыми органическими кислотами (рК~3,5).
Ацидоз достигает опасных величин при сахарном диабете, так как концентрация КТ при этом заболевании может доходить до 400—500 мг/дл. Тяжёлая форма ацидоза — одна из основных причин смерти при сахарном диабете.
Биосинтез триацилглицеринов: стадии процесса. Липотропные факторы и их роль в биосинтезе липидов в печени.
Биосинтез триацилглицеринов. Образующиеся в результате биосинтеза жирные кислоты в организмах животных и человека в свободном виде встре- чаются лишь в незначительных количествах, а присутствуют главным образом в виде триацилглицеринов. Синтез триацилглицеринов происходит в печени и жировой ткани из КоА-производных жирных кислот через фосфатидную ки- слоту по реакции:
2 R C SКоА + О Н2С ОН НС Н2С О РО3Н2 ОН Н2С О СH Н2С О РО3Н2 С R O R C O O + 2 HS-KoA Фосфатидная кислота Фосфорилирование глицерина осуществляется глицеролкиназой за счет энергии АТФ. Глицерол-3-фосфат может образовываться и при восстановлении диоксиацетонфосфата. Гидролиз фосфатидной кислоты фосфатазой приводит к образованию 1,2-диацилглицерина, который, реагируя с другой молекулой ацил-КоА, обра- зует нейтральный триацилглицерин. В слизистой кишечника триацилглицерины синтезируются из свободных кислот, моно- и диацилглицеринов, но эти процессы характерны только для слизистой оболочки кишечника. Перенос остатка жирной кислоты происходит через ацильное производное КоА.
Липотропные факторы – вещества, способствующие синтезу фосфолипидов и препятствующие отложению триацилглицеролов в тканях.
Липотропный эффект этих соединений связан с тем, что общим предшественником триацилглицеролов и фосфолипидов является фосфатидная кислота. При недостатке липотропных факторов фосфатидная кислота используется преимущественно для синтеза триацилглицеролов. Они нерастворимы в воде и накапливаются в клетках, способствуя их жировому перерождению. Запомните, какие липотропные факторы можно использовать в качестве препаратов для его предупреждения:
1) холин – самое распространённое азотистое основание фосфолипидов;
2) метионин – незаменимая аминокислота, предшественник S-аденозилметионина, универсального донора метильных групп;
3) фолиевая кислота и витамин В12 – предшественники коферментов, участвующих в реакциях переноса СН3-групп.
При введении липотропных факторов снижается синтез триацилглицеролов и усиливается выведение жира из клеток при участии липопротеиновых комплексов
