
Коноплева 2013
.pdfстая (Остро-пёстро) – |
ноиды, жир. |
Карсил, |
дулирующее, |
Silybum marianum |
масло, биоген- |
Силимар, |
антиокси- |
(L.) Gaerth., |
ные амины |
Силибин, |
дантное |
Астровые – |
|
Сибектан, |
|
Asteraceae |
|
Гепабене, |
|
|
|
Гепатофит |
|
|
|
(сбор) |
|
|
|
|
|
Подофилла корне- |
Лигнаны тетра- |
Подофил- |
Цитостати- |
вища с корнями – |
гидронафтали- |
лин |
ческое; |
Podophylli rhizoma- |
нового типа: |
|
желчегонное, |
ta cum radicibus, |
подофиллоток- |
|
слабительное |
Подофилл щитовид- |
син, |
|
(в виду ток- |
ный – Podophyllum |
пельтатины, |
|
сичности с |
peltatum L., |
флавоноиды |
|
такой целью |
Барбарисовые – |
|
|
не использу- |
Berberidaceae |
|
|
ется) |
153

ТЕМА 11. КУМАРИНЫ И ХРОМОНЫ
Кумарины - природные кислородсодержащие гетероциклические соединения, в основе структуры которых лежит бензо-α-
пирон (лактон цис-орто-гидроксикоричной (о-кумаровой) кислоты).
История изучения этого класса соединений началась с 1820 г., когда немецким ученым Фогелем было выделено вещество из семян ("бобов тонко") южноамериканского дерева Dipteryx odorata, семейства Бобовые. По местному названию дерева "кумарина" (coumarouna) это вещество было названо кумарином.
КЛАССИФИКАЦИЯ КУМАРИНОВ
Впервые предложена Е.Шпетом в 1937 г., затем пересматривалась другими учеными.
В основу классификации кумаринов положены:
1)степень насыщенности пиронового кольца кумарина,
2)характер заместителей,
3)конденсация кумарина с фурановым, пирановым или бензольным кольцами.
Кумарины подразделяют на следующие основные группы:
1. Кумарин, изокумарин, дигидрокумарин и их гликозиды:
5 |
4 |
|
глюкоза-O |
|
|
6 |
3 |
|
|
||
|
|
|
|
||
|
2 |
O |
|
|
|
7 |
|
O O |
HO |
O O |
|
8 |
O |
O |
|||
|
1 |
|
|
|
|
|
|
O |
|
|
|
КУМАРИН |
ИЗОКУМАРИН |
ДИГИДРОКУМАРИН |
|
ЭСКУЛИН |
|
Эти соединения обнаружены в траве донника лекарственного. 2. Гидрокси-, метокси- и метилендигидроксикумарины.
С гидроксильными или метоксильными группами в бензольном или пироновом кольцах:
|
|
HO |
|
HO |
O O |
HO |
O O |
УМБЕЛЛИФЕРОН |
|
ЭСКУЛЕТИН |
|
(7-гидроксикумарин) (6,7-дигидроксикумарин)
154
Эти соединения обнаружены в растениях семейств Сельдерейные, Рутовые.
3. Фурокумарины. Различают:
1) производные псоралена, т.е. фурокумарины, фурановое ядро которых сконденсировано с кумарином в 6,7-положениях:
OCH3
O |
O O |
O |
O O |
O |
O O |
|
|
|
OCH3 |
|
|
ПСОРАЛЕН |
КСАНТОТОКСИН |
БЕРГАПТЕН |
|||
(8-метоксипсорален) (5-метоксипсорален)
OCH3
OO O
OCH3
ИЗОПИМПИНЕЛЛИН
(5,8-диметоксипсорален)
Псорален выделен из плодов псоралеи костянковой, ксантотоксин, бергаптен, изопимпинеллин выделены из плодов амми большой и пастернака посевного.
2) производные изопсоралена (ангелицина), т.е. фурокумарины, фурановое ядро которых сконденсировано с кумарином в 7,8 положениях:
O  O O
O O
АНГЕЛИЦИН
Фурокумарины - наиболее часто встречающаяся группа кумари-
нов.
4. Пиранокумарины, содержащие ядро пирана, сконденсированное с кумарином в 5,6; 6,7; 7,8 - положениях, и имеющие заместители в пирановом, бензольном или пироновом кольцах:
155
O  O O
O O
КСАНТИЛЕТИН
К этой группе относятся - самидин, дигидросамидин, виснадин, которые выделены из корневищ и корней вздутоплодника сибирского.
5. Бензокумарины - соединения, содержащие бензольное кольцо, сконденсированное с кумарином в 3, 4-положениях:
OH
O O |
OH |
HO |
O O |
O O |
|
OH |
|
ЭЛЛАГОВАЯ КИСЛОТА |
3, 4-БЕНЗОКУМАРИН |
|
6. Куместаны - кумарины, содержащие систему бензофурана, сконденсированную с кумарином в 3,4 положениях (куместролы):
OH
O
HO |
O O |
|
КУМЕСТРОЛ |
Они выделены из различных видов клевера семейства Бобовые. 7. Соединения более сложной структуры, содержащие кумариновую систему (афлатоксины и др.). Их известно несколько серий,
которые обозначаются буквами латинского алфавита.
Помимо различия в структуре циклических систем природные кумарины различаются по характеру, числу и положению замещающих радикалов. Из радикалов наиболее часто встречается ОН-группа, она бывает свободной или находится в виде простых или сложных эфиров. Алкилирующим компонентом является метильная группа - СН3. Из углеводных компонентов чаще всего встречается глюкоза, которая присоединяется у С6, С7 или С8 кумаринового ядра. В составе сложных эфиров - остаток кислот ангеликовой или изовалериановой.
156
РАСПРОСТРАНЕНИЕ КУМАРИНОВ В РАСТИТЕЛЬНОМ МИРЕ
Кумарины широко распространены в растительном мире. Они обнаружены в высших, низших растениях и грибах. Найдены они в бобровой струе - жидкости парных желез бобра, селедке. Совсем не обнаружены в водорослях, незначительно представлены в папоротникообразных и голосеменных. Практически все многообразие кумаринов отмечено среди покрытосеменных.
В небольшом количестве кумарины встречаются в растениях, используемых человеком в пищу (петрушка, пастернак, укроп).
Они найдены у представителей 34 семейств: |
|
||
Сельдерейные |
(Apiaceae), |
Камнеломковые (Saxifragaceae), |
|
Рутовые |
(Rutaceae), |
Пасленовые |
(Solanaceae), |
Бобовые |
(Fabaceae), |
Астровые |
(Asteraceae) и др. |
В растениях кумарины находятся обычно в виде агликонов, но иногда могут быть в форме гликозидов.
ЛОКАЛИЗАЦИЯ В РАСТЕНИЯХ
Кумарины локализуются в растворенном состоянии в клеточном соке в различных органах и частях растений.
Чаще всего в плодах - псоралея костянковая, амми большая, укроп огородный (в зонтичных кумарины обычно локализуются в эфиромасличных канальцах);
вподземных органах - вздутоплодник сибирский;
всеменах - конский каштан;
втраве - донник лекарственный.
Содержание кумаринов в различных растениях колеблется от 0,5% до 2-5%. В одном растении может содержаться от 5 до 10 кумаринов различной структуры.
ДИНАМИКА НАКОПЛЕНИЯ
Динамика накопления меняется по фазам вегетации: максимальное содержание в цветках и траве в период цветения, а затем содержание снижается; в плодах и семенах - в период молочной зрелости, полного созревания; в корнях - в период увядания надземной массы осенью.
БИОЛОГИЧЕСКАЯ РОЛЬ
Роль кумаринов в растительном мире до конца не установлена. Предполагают, что:
157
•некоторые кумарины являются ингибиторами роста растений,
•другие стимулируют прорастание семян,
•третьи выступают в качестве защитных средств при вирусных заболеваниях растений, а также ультрафиолетового облучения (кумарины, поглощая УФ - лучи, защищают молодые растения от чрезмерного солнечного облучения. В условиях интенсивного освещения увеличивается количество кумаринов),
•выполняют роль инсектицидов.
ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА
1.Кумарины представляют собой кристаллические бесцветные или слегка желтоватые вещества без запаха (за исключением кумарина, имеющего запах свежего сена).
2.Агликоны хорошо растворимы в органических растворителях (хлороформе, метиловом и этиловом спиртах, в эфирах: петролейном, диэтиловом), жирах, жирных маслах. В воде не растворяются.
3.Гликозиды растворяются в воде, в спиртах, в водноспиртовых растворах, но не растворяются в органических растворителях.
4.Для кумаринов характерна высокая устойчивость лактонного кольца. Кумарины не раскрывают лактонного цикла при длительном кипячении водных растворов. Они не взаимодействуют с аммиаком и кислотами.
5.Одним из самых характерных свойств кумаринов как лактонов является их специфическое отношение к щелочам. Раскрытие лактонного кольца происходит лишь при воздействии разбавленной щелочи при нагревании с образованием солей гидроксикоричных кислот, но при подкислении кольцо вновь замыкается, образуя исходный кумарин.
|
+ NaOH |
|
|
+ HCl |
COONa |
O |
O |
OH |
КУМАРИН |
NA СОЛЬ О-КУМАРОВОЙ К-ТЫ |
|
(кумаринат натрия)
6.При нагревании до 100°С кумарины возгоняются.
7.Кумарины флуоресцируют в УФ свете желтым, голубым, фиолетовым цветом. В щелочной среде флуоресценция усиливается, при
158

подкислении флуоресценция становится менее интенсивной и характер ее меняется.
8. Некоторые кумарины димеризуются под действием УФ света.
OH OH

 CH2
CH2

O O O O
ДИКУМАРОЛ (ДИКУМАРИН)
9.Кумарины способны давать окрашенные (от коричневокрасного до вишневого цвета) растворы с диазосоединениями.
10.Гликозиды подвергаются кислотному и ферментативному гидролизу.
ВЫДЕЛЕНИЕ КУМАРИНОВ ИЗ ЛРС
Для выделения кумаринов из ЛРС применяют этиловый и метиловый спирты, которые позволяют извлекать как агликоны, так и гликозиды. Для экстракции гликозидированных кумаринов целесообразно также применять 40-70% этиловый спирт. Исчерпывающая экстракция агликонов возможна с использованием хлороформа, диэтилового эфира, ацетона и др.
При выделении кумаринов используется свойство кумаринов раскрытия и закрытия лактонного кольца (схема 8). Для выделения кумаринов проводят:
1.Экстракцию ЛРС органическим растворителем (эфиром) получают сумму кумаринов и балластных веществ.
2.Эфирный слой отделяют, отработанное сырье выбрасывают.
3.Полученное эфирное извлечение обрабатывают 0,5% водным раствором КОН для очистки от фенолов и кислот.
4.Затем это же извлечение обрабатывают 10% спиртовым раствором КОН. Происходит разрыв лактонного кольца и образуются кумаринаты, которые переходят в водный слой. А в органическом растворителе остаются балластные вещества (смолы, стерины, спирты), органическую фазу выбрасывают.
5.Водно-щелочной слой подкисляют разбавленной HCl. Происходит замыкание лактонного кольца, образуются кумарины, которые экстрагируют органическим растворителем.
6.Органический слой отгоняют - получают сумму кумаринов, которую разделяют хроматографически.
159
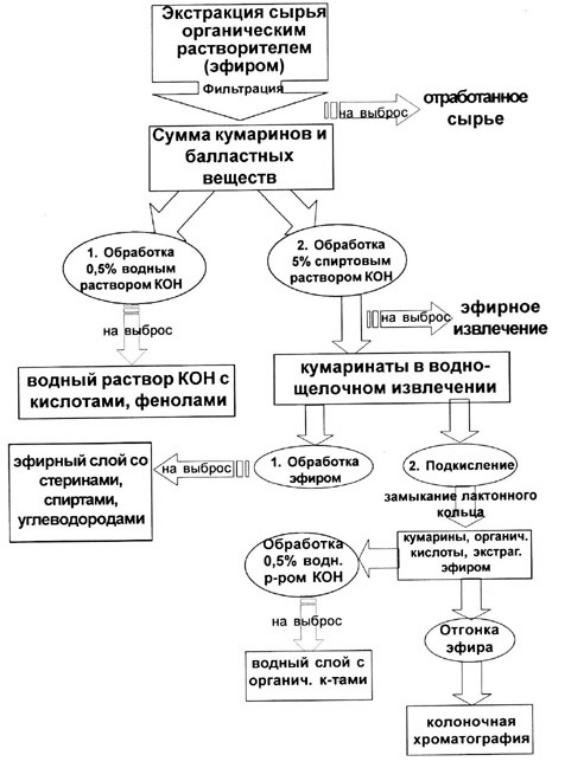
Схема 8
Схема выделения кумаринов из ЛРС
160
РАЗДЕЛЕНИЕ КУМАРИНОВ
Для разделения кумаринов используется колоночная хроматография. В качестве сорбента используется оксид алюминия и силикагель. Кумарины хорошо элюируются с колонки смесью петролейного эфира с хлороформом, бензола с этилацетатом, бензола с метанолом.
Проведение хроматографического разделения на колонке облегчается применением бумажной или тонкослойной хроматографии для качественного анализа элюатов.
КАЧЕСТВЕННЫЕ РЕАКЦИИ
Для обнаружения кумаринов в растительном сырье используют их лактонные свойства, способность флуоресцировать в УФ свете и сублимироваться, давать окрашенные растворы с диазосоединениями, а также хроматографический анализ.
Для проведения качественного анализа готовят спиртовое извлечение из ЛРС.
Лактонная проба
1.К спиртовому извлечению из ЛРС прибавляют 10% спиртовой раствор КОН, нагревают - раствор желтеет (происходит разрыв лактонного кольца, образуются кумаринаты, имеющие желтое окрашивание).
2.Затем прибавляют дистиллированную воду, перемешивают, раствор становится прозрачным (кумаринаты растворимы в воде).
3.Затем подкисляют 10% HCI до кислой реакции, при этом наблюдается помутнение или выпадение осадка, это указывает на присутствие кумаринов в сырье (образовавшиеся кумарины не растворимы в воде).
Диазореакция
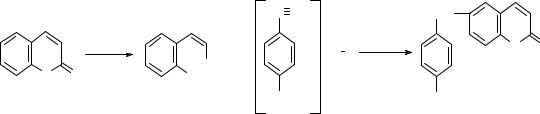
К спиртовому извлечению прибавляют 10% спиртовой раствор КОН, нагревают - раствор желтеет, прибавляют свежеприготовленный диазореактив (смесь равных объемов пара-нитроанилина и раствора нитрита натрия в концентрированной HCl).
При взаимодействии солей диазония с кумаринами в слабощелочной среде диазорадикал присоединяется в С6 положении кумариновой системы, т.е. в п-положении к фенольному гидроксилу кислоты цис-о-коричной. Получаемые соединения дают окраску от коричневокрасной до вишневой.
161
|
|
|
N N |
+ |
N=N |
|
|
|
|
||
|
+ KOH |
+ |
|
Cl |
O O |
O O |
COOK |
|
|
||
OH |
|
|
|
|
|
|
|
|
SO2NH2 |
|
SO2NH2 |
КУМАРИН |
КУМАРИНАТ К |
|
ДИАЗОРЕАКТИВ |
ОКРАШЕННЫЙ |
|
|
|
|
|
|
КОМПЛЕКС |
ХРОМАТОГРАФИЧЕСКИЙ АНАЛИЗ
Для определения кумаринов применяют ТСХ, БХ. Для ТСХ используют системы: Н-ГЕКСАН-БЕНЗОЛ-МЕТАНОЛ (5:4:1), ПЕТРОЛЕЙНЫЙ ЭФИР-БЕНЗОЛ-МЕТАНОЛ (5:4:1), БЕНЗОЛ-ЭТИЛАЦЕТАТ, БЕНЗОЛ-ХЛОРОФОРМ в различных соотношениях.
Для БХ - 15%, 60% растворы уксусной кислоты. Для обработки хроматограмм используют:
•10% спиртовой раствор КОН,
•диазотированный сульфаниламид - кумарины окрашиваются в оранжевый, красно-оранжевый или фиолетовый цвет,
•пары йода - кумарины окрашиваются в коричневый цвет. Кумарины на хроматограммах определяют по флуоресценции в
УФ свете до и после проявления спиртовым раствором КОН.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
В основу количественного определения кумаринов положены их специфические физико-химические свойства.
1.Гравиметрический метод, в основе которого лежит способность лактонного кольца к обратимому размыканию и замыканию в зависимости от рН среды.
2.Колориметрический метод основан на способности кумаринов вступать во взаимодействие с солями диазония. В качестве реагентов применяют диазотированный п-нитроанилин, сульфаниловую кислоту, сульфаниламид.
3.Специфическое отношение кумаринов к щелочи лежит в основе метода нейтрализации (обратное титрование), которое применяется как для определения суммы кумаринов, так и для индивидуальных компонентов.
162
