- •Методичні вказівки до виконання практичних робіт з дисципліни «Теорія спікання дисперсних систем»
- •Практична робота №1 Вивчення твердофазних реакцій, що протікають при високотемпературному окускуванні тонкодисперсних залізорудних матеріалів
- •Практична робота №2 Термодинамічні розрахунки імовірності протікання твердофазних реакцій у процесах спікання металургійної сировини
- •Теоретичні передумови
- •Зміст роботи
- •Контрольні питання
- •Приклад виконання розрахунку
- •Варіанти завдань
- •Практична робота №3 Вивчення хімічних дефектів кристалічної решітки
- •Практична робота №4 Структурні дефекти кристалічної решітки
- •Контрольні питання
- •Практична робота №5 Вивчення дифузії при спіканні кристалічних тіл
- •3. Контрольні питання
- •Література
-
Контрольні питання
-
Які найважливіші типи дефектів будови кристалів?
-
Охарактеризуйте крапкові дефекти.
-
Як можна досягти концентрації дефектів за Шотки й Френкелем?
-
Охарактеризуйте крайові й гвинтові дислокації.
-
Як можна описати дислокацію?
-
Опишіть поверхневий дефект у вигляді границі зерен.
-
Охарактеризуйте дефекти впакування.
-
Опишіть поверхневий дефект у вигляді двійників.
Практична робота №5 Вивчення дифузії при спіканні кристалічних тіл
-
Причини й закони дифузії [4, c. 231-235]
Дифузія - це поширення речовини в якому-небудь середовищі в напрямку зменшення його концентрації, обумовлене тепловим рухом іонів, атомів, молекул, а також більш крупних часток. Дифундувати можуть як розчинені в речовині сторонні частки, так і частки самої речовини (самодифузія). Якщо в системі підтримується нерівномірний розподіл температури або на систему діють зовнішні сили, наприклад електричні, то відбувається відповідно термодифузія, електродифузія тощо, у результаті яких установлюється нерівномірний розподіл концентрації.
Причини дифузії, тобто рушійні сили, можна пояснити законами термодинаміки. Процеси дифузії можливі, якщо при цьому зменшується вільна енергія системи або підвищується ентропія. Так як дифузійні процеси пов'язані з підвищенням ентропії, вони необоротні. Якщо система перебуває в рівновазі, тобто ентропія максимальна, дифузія не може відбуватися мимовільно. Таким чином, процеси дифузії завжди відбуваються при відхиленні від термодинамічної рівноваги.
Дифузія - особливий процес переносу речовини (у результаті елементарних блукань часток).
Розрізняють гетерогенну (або хімічну) дифузію (звичайно -- просто «дифузія»), що протікає при наявності різниці хімічних потенціалів (концентраційних потенціалів) в обсязі системи; і самодифузію, коли мова йде про однокомпонентні системи й дифузія відбувається шляхом вирівнювання різних кінетичних енергій атомів (аналогічно броунівскому руху в рідинах).
Атомний механізм дифузії в кристалах можна представити як механізм обміну місць. Щоб частка, що перебуває у вузлі решітки, могла покинути своє нормальне місце, їй необхідно додати певну енергію (енергію активації). Остання особливо низька для часток кристала, що перебувають на поверхні, тому що вони мають менше зв'язків, ніж атоми усередині кристала (поверхнева дифузія або дифузія Фольмера). Рух власних, а також адсорбованих атомів або іонів на поверхні кристала не є безладним, а відбувається по певних кращих напрямках (рис. 5.1.).
|
а б |
|
Рис. 5.1. Напрямки переважної поверхневої дифузії по грані куба: а) кристал з кубічною примітивною решіткою б) кристал з кубічною гранецентрованою решіткою |
Дифузія різних атомів також здійснюється за рахунок процесів обміну місць, причому на безладний рух (вирівнювання різних кінетичних енергій) накладається спрямований рух, обумовлений розходженнями в хімічних потенціалах компонентів системи.
Дифузійний перенос речовини описується законами Фіка.
Перший
закон Фіка
справедливий для дифузії в ідеальних
розчинах при відсутності зовнішніх
сил: кількість перенесеної речовини
(dn) пропорційна градієнту концентрації
![]() ,
,
поперечному перерізу (q) і часу (t):
![]() , (5.1)
, (5.1)
де х - координати уздовж шляху дифузії;
D
– коефіцієнт дифузії, що залежить від
концентрації,
![]() .
.
Негативний
знак вводиться тому, що градієнт
![]() приймає негативне значення, якщо напрямок
дифузії вважається позитивним.
приймає негативне значення, якщо напрямок
дифузії вважається позитивним.
Другий
закон Фіка
(для нестаціонарних систем, у яких
коефіцієнт концентрації![]() залежить від часу):
залежить від часу):
![]() [частки
похідні] (5.2)
[частки
похідні] (5.2)
Якщо розглядати D як незалежну від концентрацій величину, що строго виконується тільки для самодифузії, а в першому наближенні виявляється справедливим для багатьох практичних випадків, співвідношення (5.2) переходить в
![]() . (5.3)
. (5.3)
Використання цього диференціального рівняння можливо при встановленні певних граничних умов. Його можна проінтегрувати за допомогою функції помилок Гауса. Результатом цього розрахунку є параболічний закон виду
![]() , (5.4)
, (5.4)
де а- константа.
Формула (5.4) надає коефіцієнту дифузії наочний фізичний зміст. Якщо х – середній зсув атомів, що дифундують, що відповідає середній глибині проникнення, то коефіцієнт дифузії приблизно може бути виражений через квадрат середнього зсуву
![]()
![]() (5.5)
(5.5)
У багатьох випадках для рішення параболічного диференціального рівняння в частинних похідних простіше користуватися графічним методом (метод Матано).
-
Методи дослідження [4, c. 235-238]
Для дослідження процесів дифузії застосовуються металографічні, хімічні й фізичні способи. Останнім часом все більше місце займають методи із застосуванням радіоактивних ізотопів (особливо при дослідженні самодифузії).
Тамман увів поняття температури початку помітної дифузії. Температурна залежність швидкості дифузії має експонентний вигляд, що дозволяє чітко розмежовувати температурні області, так що поняття температури початку дифузії має відомий сенс і дуже виправдало себе практично. По Тамману:
ТП.Д.=(0,3-0,4)ТПЛ – для металів;
ТП.Д.≈0,6ТПЛ – для оксидів;
ТП.Д.≈(0,8-0,9)ТПЛ – для органічних вуглецевих сполук.
2.1. Металографічні й хімічні методи часто засновані на використанні двох циліндричних зразків, що перебувають у тісному контакті. При досить високих температурах відбувається міграція атомів по напрямку осі циліндрів. Зміна концентрації уздовж шляху дифузії можна здійснити, зокрема, хімічним аналізом тонких пластин, отриманих шляхом зрізу на стінці (рис. 5.2).
Процеси дифузії можна вивчати, визначаючи загальну кількість атомів, що дифундують через відомий поперечний переріз. Якщо привести в контакт дві пластинки, які після досвіду можна відокремити одну від одної по місцю контакту, то після цього пластинки будуть мати в загальному випадку іншу масу в порівнянні з вихідними пластинками (метод особливо придатний для сульфідів і оксидів, тому що в металах після дифузії відокремити пластини взагалі не вдається).
|
|
Рис.
5.2. Експериментальна залежність
|
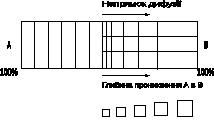
2.2. Фізичні методи. Один з найважливіших - випробування на мікротвердість. Принцип методу полягає в тому, що після проведеної дифузії роблять відбитки, наприклад, алмазною пірамідкою на різному віддаленні від їх вихідної граничної поверхні. Так як твердість змішаних кристалів звичайно вище, ніж у чистих компонентів, одержують закономірну зміну мікротвердості залежно від концентрації (рис. 5.3).
|
Розміри відбитків |
Рис. 5.3. Визначення глибини дифузійного проникнення за допомогою виміру мікротвердості |
Наступний метод полягає у вимірі змін елетропровідності. У цьому випадку досліди з дифузією доцільно проводити на дротах, у яких радіально дифундує другий компонент. Потім по каліброваній кривій одержують кількісний зв'язок між провідністю й концентрацією.
2.3. Метод радіоактивних ізотопів має свої особливості для вивчення різних систем. Для визначення коефіцієнта самодифузії використовують циліндричні зразки, один із яких мічений радіоактивним ізотопом. Після закінчення досліду виготовляють тонкі пластинки й вимірюють їхню радіоактивність.
Також можна використовувати авторадіографічний метод, який полягає в тому, що радіоактивний компонент, перебуваючи в контакті з фотоплівкою, викликає почорніння емульсії, по якому можна судити про глибину проникнення.