
Скорость химических реакций. Лимитирующие звенья процессов
По уравнению Аррениуса константа скорости химической реакции
![]() ,
(5.9)
,
(5.9)
где
![]() – константа скорости при температуре
– константа скорости при температуре
![]() или
или
![]() ;
;
– энергия активации,
характеризующая разность между минимально
необходимым уровнем внутренней энергии
частиц для эффективного их столкновения
и средним уровнем энергии реагирующих
веществ,
![]() .
.
Физический смысл энергии активации виден на рис. 5.1.
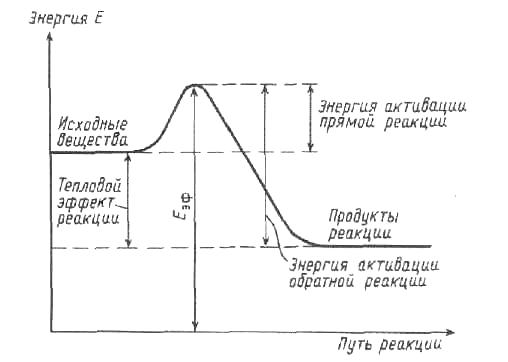
Рисунок 5.1 — Схема изменения энергии системы при химической
реакции
Если реагирующие
вещества характеризуются средним
уровнем внутренней энергии, меньшим
необходимого для эффективного столкновения
молекул, то в химическую реакцию вступают
лишь те молекулы, которые в результате
флуктуации энергии обладают уровнем
энергии, который равен или больше
![]() (рис. 5.1). Доля таких молекул будет тем
меньше, чем больше энергия активации
.
(рис. 5.1). Доля таких молекул будет тем
меньше, чем больше энергия активации
.
Для прямой реакции:
![]() ;
;
для обратной
реакции
![]()
Таким образом, энергия активации представляет собой энергетический барьер, через который система должна перейти по пути из исходного состояния в конечное.
При низких
температурах
увеличивается (более
![]() ),
так как средний уровень внутренней
энергии молекул значительно ниже
,
что обусловливает малую скорость
динамической реакции.
),
так как средний уровень внутренней
энергии молекул значительно ниже
,
что обусловливает малую скорость
динамической реакции.
При высоких
температурах, характерных для
сталеплавильных процессов, энергия
активации
![]() (средний уровень энергии молекул
превышает
).
В этих условиях скорость гомогенных
химических реакций огромна (скорость
взрыва) и почти не зависит от температуры.
Ярким примером служит конвертерный
процесс, где в результате мощного
перемешивания металла и интенсивности
подвода кислорода в ванну скорость всех
процессов примерно в 100 раз больше, чем
в мартеновской ванне. В этих условиях
скорость многостадийного гетерогенного
процесса лимитируется интенсивностью
диффузии реагирующих компонентов к
месту реакции. Наблюдаемое сравнительно
небольшое влияние температуры на
скорость процесса обусловлено ее
влиянием на коэффициенты массопереноса
(средний уровень энергии молекул
превышает
).
В этих условиях скорость гомогенных
химических реакций огромна (скорость
взрыва) и почти не зависит от температуры.
Ярким примером служит конвертерный
процесс, где в результате мощного
перемешивания металла и интенсивности
подвода кислорода в ванну скорость всех
процессов примерно в 100 раз больше, чем
в мартеновской ванне. В этих условиях
скорость многостадийного гетерогенного
процесса лимитируется интенсивностью
диффузии реагирующих компонентов к
месту реакции. Наблюдаемое сравнительно
небольшое влияние температуры на
скорость процесса обусловлено ее
влиянием на коэффициенты массопереноса
![]() и не связано с изменением скорости
химической реакции. Поэтому в условиях
сталеплавильной ванны вычисленная
энергия активации называется «кажущейся»
и не связано с изменением скорости
химической реакции. Поэтому в условиях
сталеплавильной ванны вычисленная
энергия активации называется «кажущейся»
![]() .
.
Для практических целей имеет большое значение, поскольку даже при сохранении порядка константы скорости процесса увеличение ее в 1,5 – 2,0 раза весьма существенно для производительности агрегата.
Обычно считают,
что если
![]() ,
то процесс находится в кинетической
области (лимитируется скоростью
химической реакции).
,
то процесс находится в кинетической
области (лимитируется скоростью
химической реакции).
Если
![]() ,
процесс находится в диффузионной области
(лимитируется скоростью диффузии).
,
процесс находится в диффузионной области
(лимитируется скоростью диффузии).
Если процесс содержит несколько диффузионных звеньев, его скорость в целом лимитируется наиболее медленными из этих звеньев.
Примеры
лимитирующих диффузионных звеньев.
Процесс обезуглероживания стали часто
лимитируется подводом кислорода через
пограничный слой в газе или диффузией
в шлаке, а иногда -диффузией в недостаточно
перегретом выше линии ликвидуса вязком
металле; еще реже – условиями зарождения
пузырей
![]() .
Процессы удаления фосфора и серы из
металла лимитируются диффузией продуктов
реакций в шлаке; в некоторых случаях –
диффузией фосфора и серы в металле.
.
Процессы удаления фосфора и серы из
металла лимитируются диффузией продуктов
реакций в шлаке; в некоторых случаях –
диффузией фосфора и серы в металле.
