
- •2. Молекулярная физика и термодинамика
- •Молекулярно-кинетическая теория Основные понятия и определения молекулярной физики и термодинамики
- •Давление. Основное уравнение молекулярно-кинетической теории
- •Термометры. Единицы измерения температуры
- •Законы идеальных газов
- •(Уравнение Менделеева – Клапейрона)
- •Распределение газовых молекул по скоростям и энергиям Скорости газовых молекул. Опыт Штерна
- •Понятие о распределении молекул газа по скоростям
- •Наиболее вероятная, среднеквадратичная и средняя арифметическая скорости молекул газа
- •Формула Максвелла для относительных скоростей
- •Зависимость функции распределения Максвелла от массы молекул и температуры газа
- •Барометрическая формула
- •Первое начало термодинамики. Внутренняя энергия. Работа и теплота
- •Теплоёмкость идеального газа. Уравнение Майера
- •Теплоемкости многоатомных газов
- •Применение первого начала термодинамики к изопроцессам идеальных газов
- •Круговые процессы. Тепловые машины
- •Энтропия. Второе и третье начала термодинамики
- •Фазовый переход «твердое тело – жидкость»
- •Фазовый переход «жидкость – газ»
- •Обратимый цикл Карно
- •Необратимый цикл
- •6.6. Свободная и связанная энергии
- •Термодинамические свойства реальных газов
- •7.1. Реальные газы
- •7.2. Уравнение Ван–дер–Ваальса
- •7.3. Изотермы уравнения Ван–дер–Ваальса
- •7.4. Внутренняя энергия газа Ван–дер–Ваальса
Теплоемкости многоатомных газов
Опыты с двухатомными газами, такими как азот, кислород и др., показали, что

Для водяного пара и других многоатомных газов (СН3, СН4 и так далее)
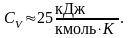
Таким образом, молекулы многоатомных газов нельзя рассматривать как материальные точки. Необходимо учитывать вращательное движение молекул и число степеней свободы этих молекул.
Числом степени свободы (i) называется число независимых переменных, определяющих положение тела в пространстве.
Положение одноатомной молекулы, как и материальной точки, задаётся тремя координатами, поэтому она имеет три степени свободы (рис. 4.3).
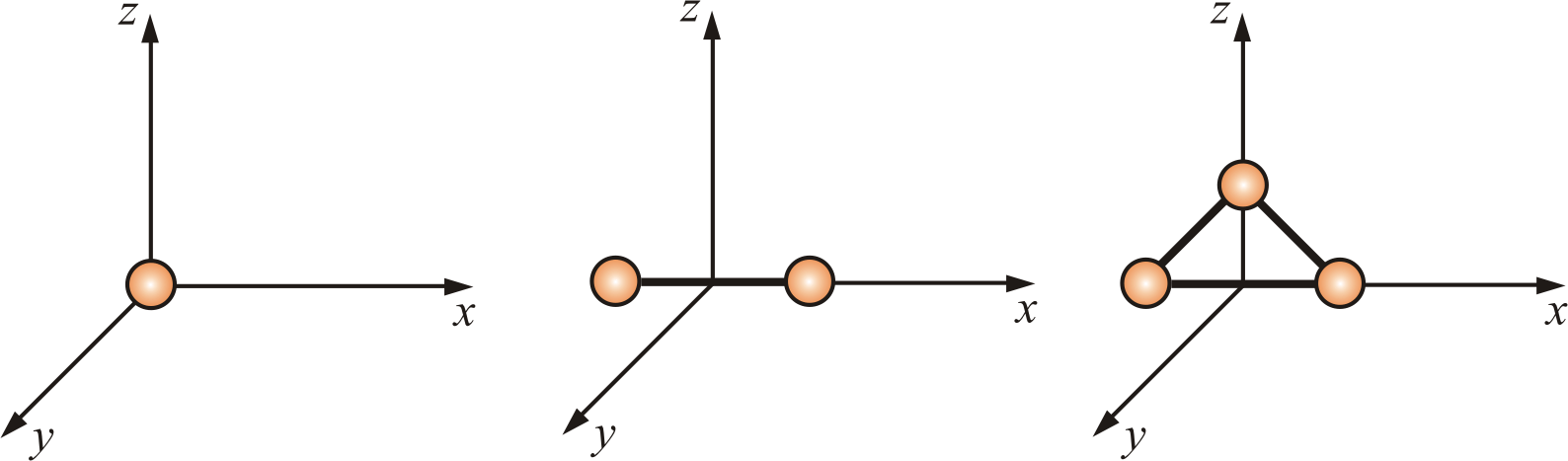
Рис. 4.3
Многоатомная молекула может ещё и вращаться. Например, у двухатомных молекул вращательное движение можно разложить на два независимых вращения, а любое вращение можно разложить на три вращательных движения вокруг взаимно перпендикулярных осей. Но для двухатомной молекулы вращение вокруг её собственной оси не изменит её положение в пространстве, а момент инерции относительно этой оси равен нулю (рис. 4.3).
Таким образом, у двухатомных молекул пять степеней свободы (i = 5), а у трёхатомных шесть степеней свободы (i = 6).
При
взаимных столкновениях молекул возможен
обмен их энергиями и превращение энергии
вращательного движения в энергию
поступательного движения и обратно.
Таким путём было установлено равновесие
между значениями средних энергий
поступательного и вращательного движения
молекул. Больцман
доказал,
что
для не слишком низких температур
средняя
энергия
,
приходящаяся
на
одну
степень
свободы, равна
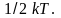
Итак, средняя энергия приходящаяся на одну степень свободы:
 (4.4.1)
(4.4.1)
У одноатомной молекулы i = 3, тогда для одноатомных молекул
 (4.4.2)
(4.4.2)
для двухатомных молекул
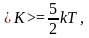 (4.4.3)
(4.4.3)
для трёхатомных молекул
 (4.4.4)
(4.4.4)
Таким образом, на среднюю кинетическую энергию молекулы, имеющей i-степеней свободы, приходится
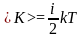 . (4.4.5)
. (4.4.5)
Это и есть закон Больцмана о равномерном распределении средней кинетической энергии по степеням свободы.
Если система находится в состоянии термодинамического равновесия, при температуре Т, то средняя кинетическая энергия равномерно распределена между всеми степенями свободы. На каждую поступательную iп и вращательную iвр степени свободы приходится энергия 1/2 kT. Для колебательной iкол степени свободы она равна kT. Таким образом число степеней свободы i = iп + iвр + 2iкол
Закон о равномерном распределении энергии по степеням свободы перестает быть справедливым при квантовом описании системы частиц, когда каждому квантовому состоянию системы с i-степенями свободы соответствует ячейка объемом hi в фазовом пространстве “координаты – импульсы” тождественных (неразличимых между собой) частиц, где h – постоянная Планка.
При этом энергии вращения и колебания молекул принимают дискретные значения или говорят, что они квантуются. Энергия колебания молекулы, как квантового гармонического осциллятора равна
Eкол = (1/2+n) hv,
где v – собственная частота колебаний; n = 0,1,2,… - квантовое число.
Энергия
Eкол
при n
= 0, равная Е0
= 1/2 hv,
называется нулевой колебательной
энергией (энергией
нулевых колебаний).
Разность энергий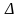 Екол
между соседними уровнями энергии равна
hv.
Энергия вращательного движения молекулы
зависит от её вида. Для двухатомной
молекулы с жесткой связью эта энергия
имеет вид
Екол
между соседними уровнями энергии равна
hv.
Энергия вращательного движения молекулы
зависит от её вида. Для двухатомной
молекулы с жесткой связью эта энергия
имеет вид
Евр
=
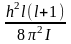
Где I – момент инерции молекулы вокруг оси, проходящей через центр инерции молекулы; l = 0,1,2,… - вращательное квантовое число. Расстояние между соседними уровнями энергии вращения Евр приблизительно в тысячу раз меньше Екол
Для
двухатомных молекул:

для
трехатомных молекул:
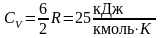 .
.
В общем случае для молярной массы газа
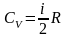 . (4.4.6)
. (4.4.6)
 . (4.4.7)
. (4.4.7)
Для произвольного количества газов:
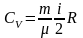 , (4.4.8)
, (4.4.8)
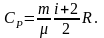 (4.4.9)
(4.4.9)
Из теории также следует, что СV не зависит от температуры (рис. 4.4).
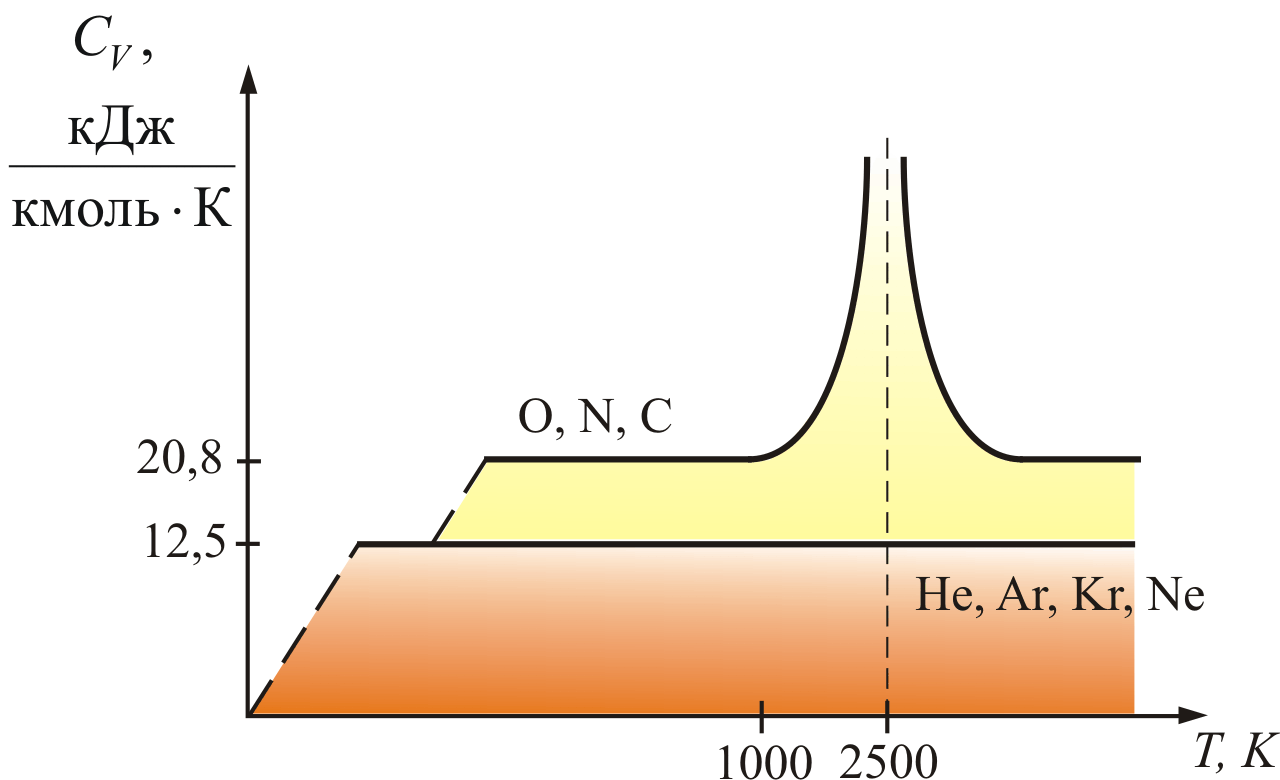
Рис. 4.4
Для одноатомных газов это выполняется в очень широких пределах, а для двухатомных газов только в интервале от 100 до 1000 К. Отличие связано с проявлением квантовых законов. При низких температурах вращательное движение как бы «вымерзает» и двухатомные молекулы движутся поступательно, как одноатомные; равны их теплоёмкости.
При
увеличении температуры, когда Т
> 1000 К, начинают сказываться
колебания
атомов молекулы вдоль оси z
(атомы в молекуле связаны не жёстко, а
как бы на пружине). Одна колебательная
степень свободы несет
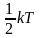 энергии, так как при этом есть и
кинетическая, и потенциальная энергия,
то есть появляется шестая степень
свободы – колебательная. При температуре
равной 2500 К, молекулы диссоциируют. На
диссоциацию молекул тратится энергия
раз в десять превышающая среднюю энергию
поступательного движения. Это объясняет
сравнительно низкую температуру пламени.
Кроме того, атом – сложная система, и
при высоких температурах начинает
сказываться движение электронов внутри
него.
энергии, так как при этом есть и
кинетическая, и потенциальная энергия,
то есть появляется шестая степень
свободы – колебательная. При температуре
равной 2500 К, молекулы диссоциируют. На
диссоциацию молекул тратится энергия
раз в десять превышающая среднюю энергию
поступательного движения. Это объясняет
сравнительно низкую температуру пламени.
Кроме того, атом – сложная система, и
при высоких температурах начинает
сказываться движение электронов внутри
него.
