
Проверка знаний по всему курсу. Часть 3 (pdf)
.pdf
МИНИСТЕРСТВО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
АЛТАЙСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ ХИМИЧЕСКИЙ ФАКУЛЬТЕТ
КАФЕДРА ОРГАНИЧЕСКОЙ ХИМИИ
ОРГАНИЧЕСКАЯ ХИМИЯ
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ
ЧАСТЬ III
Для студентов биологического факультета
Барнаул • 2000
Составители: И.Б. Катраков, канд. хим. наук В.И. Маркин, канд. хим. наук О.А. Панченко
П.И. Сиянко, канд. хим. наук, доцент
Представленное пособие является рабочей тетрадью, для самостоятельной работы студентов при изучении органической химии по модульно рейтинговой технологии обучения. Предназначено для студентов очного и вечернего отделений по специальности 01.09 "Биология".
Во вторую части пособия вошли три темы: "Особенности строения, реакционной способности и методы синтеза карбонилсодержащих и азотсодержащих соединений", "Особенности строения, реакционной способности и методы синтеза карбоновых кислот и их производных, окси- и оксокислот", "Особенности строения, реакционной способности и методы синтеза альдегидо- и кетоспиртов. Углеводы. Особенности строения, реакционной способности и методы синтеза аминокислот. Белки. Особенности строения, реакционной способности и методы синтеза гетероциклических соединений".
Пособие может быть полезно студентам нехимических специальностей вузов, школьникам специализированных классов, а также всем интересующимся органической химией.
Подписано в печать 20.10.2000. Формат 60*80/16. Бумага офсетная. Печать офсетная. Усл. п.л. 1,3. Тираж 100 экз. Заказ
Типография Алтайского государственного университета: 656099, Барнаул, ул. Димитрова, 66

3
Студент(ка) |
|
Группа |
|
Фамилия, имя, отчество |
|
Указания к выполнению задания: Предлагаемое Вашему вниманию задание предназначено для самостоятельной работы в свободное от аудиторных занятий время. Задания предполагают индивидуальное и самостоятельное выполнение! Только в этом случае Вас ждет успех при изучении органической химии.
Задание состоит из нескольких разделов. Только первый раздел "Программа" носит информативный характер и определяет тот минимум знаний, которым Вы должны владеть после выполнения данной модульной программы. Все ответы на упражнения в остальных разделах следует вносить в данное задание на свободном, специально предназначенном для этого месте. После ответа на все вопросы данное задание сдается преподавателю, ведущему лабораторные занятия.
ОСОБЕННОСТИ СТРОЕНИЯ, РЕАКЦИОННОЙ СПОСОБНОСТИ И МЕТОДЫ СИНТЕЗА КАРБОНИЛ- И АЗОТСОДЕРЖАЩИХ СОЕДИНЕНИЙ
ПРОГРАММА
Классификация карбонильных соединений.
Альдегиды и кетоны. Предельные альдегиды и кетоны. Изомерия. Номенклатура. Физические свойства. Связь с другими классами соединений. Строение карбонильной группы.
Методы получения из спиртов, производных карбоновых кислот, алкенов (озонолиз), алкинов (гидроборирование), на основе металлоорганических соединений. Ацилирование и формилировение аренов. Промышленное получение формальдегида, ацетальдегида (Вакер-процесс) и высших альдегидов (гидроформилирование).
Строение карбонильной группы, ее полярность и поляризуемость. Сравнение свойств двойной углерод-углеродной и углерод-кислородной связей. Общие представления о механизме нуклеофильного присоединения по карбонильной группе альдегидов и кетонов. Кислотный и основной катализ. Присоединение воды, спиртов, меркаптанов, магний органических соединений. Реакции с аммиаком, аминами, гидроксиламином, гидразином и его производными. 1,3-Дитианы и использование их в органическом синтезе.
Получение бисульфитных производных и циангидринов. Бензоиновая конденсация. Взаимодействие альдегидов и кетонов с азотистыми основаниями. Получение аминов и енаминов. Оксимы, гидразоны, фенилгидразоны. Перегруппировка Бекмана. Реакции с металлоорганическими соединениями. Синтез спиртов, побочные реакции в этом синтезе.
Кето-енольная таутомерия. Енолизация альдегидов и кетонов в реакциях галогенирования, изотопного обмена водорода и рацемизации оптически активных кетонов. Кислотный и основной катализ этих реакций.

4
Альдольно-кротоновая конденсация альдегидов и кетонов в кислой и основной среде, механизм реакции. Биохимическое значение реакции конденсации.
Восстановление альдегидов и кетонов до спиртов, реагенты восстановления, восстановление С=О-группы до СН2-груплы. Окисление альдегидов, реагенты окисления. Аутоокисление альдегидов. Окисление кетонов перкислотами по Байеру–Вил- лигеру. Диспропорционирование альдегидов по Канниццаро. Реакция углеводородных радикалов альдегидов и кетонов (галогенирование и галоформная реакция).
β –Дикетоны. Кето-енольная таутомерия 1,3-дикетонов. Влияние структурных факторов и природы растворителя на положение кето-енольного равновесия и зависимость его от соотношения С-Н- и O-H-кислотности кетона и енола. Двойственная реакционная способность енолят-ионов в реакциях их алкилирования. Влияние природы катиона, среды и алкилирующего агента на направление (С– или О–) алкилирования. Ацилирование енолят-иона. Алкилирование и ацилирование енаминов. Интерпретация в рамках принципа ЖКО.
Органические соединения азота. Классификация.
Нитросоединения. Номенклатура. Физические свойства. Реакция восстановления (Зинин) и ее значение в ароматическом ряду. Промежуточные продукты восстановления. Синтетическое значение.
Амины. Номенклатура. Физические свойства. Классификация аминов. Методы получения: алкилирование аммиака и аминов (Гофман), фталимида калия (Габриэль), восстановление азотсодержащих производных карбонильных соединений и карбоновых кислот, нитросоединений.
Амины как основания. Сравнение основных свойств алифатических и ароматических аминов. Влияние на основность аминов заместителей в ароматическом ядре. Четвертичные аммониевые основания и их соли.
Сульфамидные препараты. Взаимодействие первичных, вторичных и третичных алифатических и ароматических аминов с азотистой кислотой. Окисление и галогенирование аминов. Реакции электрофильного замещения в бензольном ядре ароматических аминов. Ацилирование аминов. Защита аминогруппы.
Ароматические диазосоединения. Номенклатура. Физические свойства. Образование, строение, свойства. Диазониевый катион, причины его особой устойчивости и электрофильный характер. Азосочетание как реакции электрофильного замещения. Реакции диазосоединений без выделения азота: восстановление до арилгидризинов, азосочетание. Азо- и диазосоставляющие условия сочетания с аминами и фонолами. Азокрасители – представители класса органических красителей. Цвет и строение органических соединений.
ОСНОВНЫЕ ТЕРМИНЫ, ПОНЯТИЯ, ОПРЕДЕЛЕНИЯ
Дайте определения следующим понятиям и терминам:
Азосочетание –

5
Альдольная конденсация –
Бензоиновая конденсация –
Гидразон –
Кетали –
Кето-енольная таутомерия –
Реакция Канниццаро –
Реакция Кижнера-Вольфа –
Реакция Клемменсена –
Реакция Кучерова –
Реакция Удриса-Сергеева –
6
НОМЕНКЛАТУРА, ИЗОМЕРИЯ, ГОМОЛОГИЯ
а)
в)
д)
ж)
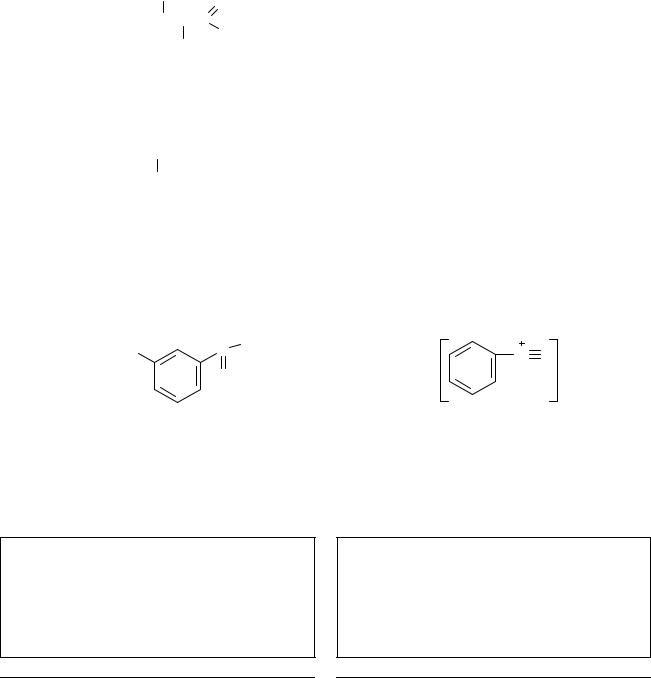
1. Нижеприведенным соединениям дайте названия по номенклатуре ИЮПАК.
|
|
|
|
|
CH3 |
O |
|
б) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||||||||||||||
CH3CHCHC |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
H |
|
|
|
CH2 |
|
|
CH |
|
|
|
C |
|
|
CH3 |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
________________________________ |
|
________________________________ |
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
O |
|
|
|
|
г) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
CHCH2CCH3 |
|
|
H2C CH C |
|
CH2 CH CH2 |
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
________________________________ |
|
________________________________ |
||||||||||||||||||||||||||||||||||||||||||
|
|
|
CH3 |
|
|
O |
|
е) |
CH3 |
|
|
CH |
|
|
N |
|
CH2CH3 |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
CH3 |
|
C |
|
|
CH |
|
C |
|
CH3 |
|
|
|
|
|
|
CH3 |
CH3 |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
________________________________ |
|
________________________________ |
||||||||||||||||||||||||||||||||||||||||||
H2N |
|
|
|
|
|
C |
H |
з) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N N Cl- |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
O
________________________________ ________________________________
2. Напишите структурные формулы следующих соединений и дайте им название
по другой номенклатуре: |
|
метилизобутилкетон |
п-толуиловый альдегид |
2,7-диметил-2,6-октадиеналь |
|
бензофенон |
|
|
|
|
|
|

7
3. Напишите структурные формулы изомерных альдегидов и кетонов общей формулы C5H10O и назовите их.
4. Напишите структурные формулы аминов состава C4H11N. Укажите первичные, вторичные и третичные амины.

8
ФИЗИЧЕСКИЕ СВОЙСТВА, ЭЛЕКТРОННОЕ СТРОЕНИЕ
1. Укажите электронные эффекты в нижеприведенных соединениях. Расположите эти соединения в ряд по увеличению реакционной способности в реакциях нук-
леофильного присоединения. |
|
|
|
||||||
а) |
O |
|
|
б) |
CH3 |
O |
|||
|
|
C |
|
|
|
C |
|||
H |
H |
|
|
H |
|||||
в) |
O |
|
|
г) |
|
O |
|||
|
|
|
|
|
CH2 |
C H |
|||
CH3 |
|
|
|
|
|
|
|
||
|
C |
|
CH3 |
|
Cl |
|
|||
|
|
|
|
||||||
2. Расположите нижеприведенные соединения в порядке увеличения основности:
NH2
CH3
а) CH3CH2CH2CH2NH2 б) CH3CH2 N CH3 в) CH3CH2 NH CH2CH3 г)
___________________________________________________
СПОСОБЫ ПОЛУЧЕНИЯ
1. Напишите уравнения нижеприведенных реакций:
Br
CH3 CH C CH2 CH3 + H2O
CH3 Br
Br CH3
CH CH2 CH CH2 CH2 CH3 + H2O 
Br

9
2. Напишите уравнение реакций пиролиза:
(HCOO)2Ca t
(C6H5CH2COO)2Ca t
3. Из толуола получите 2,4-динитробензальдегид.
4. Приведите промышленные способы получения альдегидов и кетонов.

10
ХИМИЧЕСКИЕ СВОЙСТВА И МЕХАНИЗМЫ РЕАКЦИЙ
1. Осуществите превращения:
NH2NHC6H5 NH3
NH2OH O H2O
H
HCN CH3OH
H+, t
