
АБСОРБЦИОННЫЙ ФОТОМЕТРИЧЕСКИЙ АНАЛИЗ
Оптические методы анализа основаны на использовании явлений испускания электромагнитного излучения атомами или молекулами исследуемого вещества или взаимодействия этого излучения с веществом. Так как природа излучения зависит от качественного и количественного состава вещества, то это позволяет проводить его анализ.
По характеру взаимодействия излучения с исследуемым веществом (по поглощению излучения) и способу его измерения различают: абсорбционную спектроскопию; нефелометрию; турбидиметрию; люминесцентный анализ.
В фотометрическом анализе используют поглощение электромагнитного излучения в УФ, видимой и ИК -областях спектра. Наибольшее распространение получили фотометрические методы анализа, основанные на поглощении в видимой области спектра, Т.е. в интервале длин волн 400 - 780 нм. Это объясняется возможностью получения множества интенсивно окрашенных органических и неорганических соединений, . при годных для их фотометрического определения в видимой области спектра с помощью достаточно несложных и относительно недорогих приборов.
Химические реакции, используемые в фотометрическом анализе, несмотря на различия в их химизме, должны обязательно сопровождаться возникновением или ослаблением светопоглощения раствора. Как и каждая реакция, используемая в количественном анализе, цветная реакция должна протекать избирательно, быстро, полностью и воспроизводимо. Кроме того, окраска образующейся аналитической формы должна быть устойчивой во времени и к действию света, а поглощение раствора, несущее информацию о концентрации поглощающего вещества, должно подчиняться физическим законам, связывающим поглощение и концентрацию, конкретно закону Бугера - Ламберта - Бера.
При прохождении потока излучения через частично поглощающую среду интенсивность прошедшего потока I согласно закону Бугера - Ламберта - Бера равна
![]()
где I0 - интенсивность падающего потока;
ε - молярный коэффициент поглощения при данной длине волны;
I - толщина поглощающего слоя;
с - концентрация поглощающего вещества, моль/дмЗ.
Или в логарифмической форме: lgI = lgI0 - εlc
Lg(I/I0) = A = εlc
Величину lg(I/I0), характеризующую поглощающую способность вещества в растворе, называют оптической плотностью. В аналитической практике, стремясь подчеркнуть сущность процесса, лежащего в основе фотометрического определения, а именно поглощение квантов электромагнитного излучения оптического диапазона аналитической формой, эту величину называют поглощением или светопоглощением и обозначают буквой А. Для раствора поглощающего вещества при постоянных концентрациях и толщине поглощающего слоя А зависит от длины волны. Серию аналитических определений выполняют при постоянной толщине поглощающего слоя.
На основе закона Бугера - Ламберта - Бера разработан ряд фотометрических методов по определению концентрации вещества в окрашенном растворе.
Работа 1. Определение содержания меди (11) в растворе методом градуировочногографика
Цель работы: изучение явления поглощения света веществом, устройства и принципа действия двухлучевого фотоколориметра и определение с его помощью концентрации растворов.
Задача: Определить массу меди в растворе сульфата меди методом градуировочного графика.
Приборы и реактивы:
Фотоэлектроколориметр ФЭК-56, мерная колба на 1000 мл, 7 мерных колб на 50 мл, пипетка, фильтровальная бумага; сульфат меди CUS 04-5 Н2О, концентрированная серная кислота, раствор аммиака, дистиллированная вода.
Определение меди Си2+ В растворах представляет большой практический интерес: оно про водится на предприятиях текстильной промышленности, цветной металлургии, при анализе промышленных сточных вод и др. Соли меди СП) широко применяют в сельском хозяйстве как ядохимикаты. Кроме того, ион Си2+ входит В состав медных микроудобрений.
Фотометрические определения меди выполняют аммиачным, ферроцианидным и другими методами. Аммиачный метод основан на образовании ионом Си2+ с аммиаком комплекса [Сu(NНЗ)4]2+, окрашенного в интенсивно-синий цвет.
Фотоэлектроколориметр ФЭК-56 работает по двухлучевой схеме, предназначен для определения концентрации вещества в окрашенных или коллоидных растворах путем сравнения их оптической плотности с оптической плотностью стандартных растворов в диапазоне длин волн 315-670 нм.
Оптическая схема двухлучевого фотоэлекrpoколориметра ФЭК - 56
5'
Q.
1- ИСТОЧlШК излучения; 2 - светофильтр; 3 - делитель светового потока; 4 и 4 '- конденсорные линзы; 5 и 5' - зеркала; 6 и 6 '- кюветы; 7 и 7 '- диафрагмы; 8 и 8 ' - линзы; 9 и 9' - фотоприемники световой энергии; 10- микроамперметр
От источника излучения 1 свет проходит через светофильтр 2 и разделяется призмой 3 на два равных пучка, которые, пройдя конденсорные линзы 4 и 4' направляются зеркалами 5 и 5' на кюветы 6 и 6'. Затем световые пучки проходят щели диафрагм 7 и 7', линзы 8 и 8'и попадают на фотоприемники световой энергии 9 и 9', которые соединены с микроамперметром 1 О по компенсационной схеме. В качестве приемников световой энергии используются сурьмяноцезиевые фотоэлементы Ф-4.
В правый световой пучок могут включаться последовательно одна или другая кюветы (с раствором или растворителем).
Правый световой пучок является измерительным, левый - компенсационным.
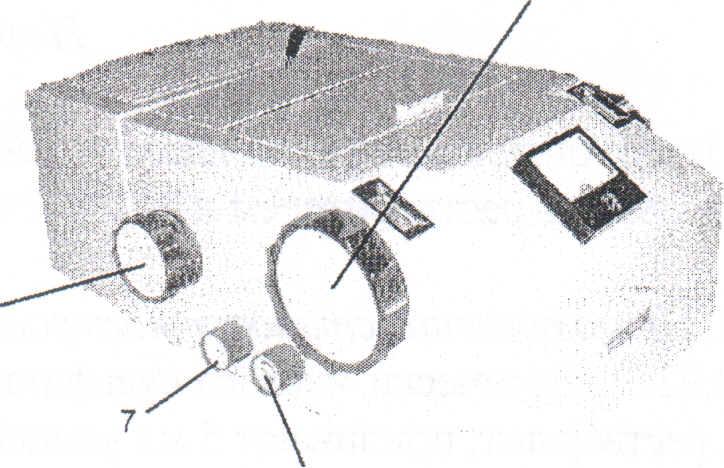
Внешний вид фотоэлектроколориметра ФЭК-56

5
8
5
6
1- микроамперметр,
2- переключатель шторки,
3- рукоятка чувствительности,
4- рукоятка переключения кювет, 5- барабаны,
6- рукоятка чувствительности,
7 - рукоятка «ноль» микроамперметра, 8- рукоятка светофильтра.
Кюветодержатели.
В левом кюветодержателе устанавливается кювета с растворителем. В правом кюветодержателе устанавливаются две кюветы - с растворителем и испытуемым раствором. Переключение кювет в правом световом пучке про водится поворотом рукоятки 4 до упора. Раствор в кюветы наливается до метки.
Измерительные диафрагмы с отсчетными барабанами.
Диафрагма состоит из двух металлических пластинок с прямоугольными вырезами. При вращении барабана обе пластинки двигаются в противоположные стороны, меняя величину светового потока.
На барабане нанесены две шкалы. Одна шкала - черная - называется шкалой коэффициента светопропускания. Другая шкала - красная - соответствует оптической плотности А.
Общие правила эксплуатации прибора
1. Измерения на приборе можно начинать спустя 10-15 минут после включения питающего устройства, так как это время необходимо для установления стабильного режима работы электросхемы прибора.
2. Рабочие поверхности кювет должны перед каждым измерением тщательно протираться.
При установке кювет в кюветодержатели нельзя касаться пальцами рабочих участков поверхностей (ниже уровня жидкости в кювете). Наличие загрязнений или капель раствора на рабочих поверхностях кюветы приводит к получению неверных результатов измерений.
3. Если в процессе работы светофильтр меняется на другой, то измерения следует производить не ранее, чем через 1 минуту после смены светофильтра.
4. После выполнения работы выключить прибор и вымыть кюветы проточной водой.
Техника безопасности
-
Приступить к выполнению работы только после изучения методической разработки.
-
Не открывать кюветную камеру при открытой шторке.
3. Работать только с заземленным прибором. При поражении током обесточить цепь: вынуть вилку из розетки либо выключить рубильник.
Порядок выполнения работы
Перед определением концентраций меди в растворе необходимо построить градуировочный график, пользуясь растворителем и стандартным раствором соли меди.
1. Приготовление стандартного раствора соли меди.
3,927 г химически чистого сульфата меди CuS04'5H20 переносят в мерную колбу вместимостью 1000 МЛ, растворяют, приливают 5 мл концентрированной серной кислоты (пл. 1 ,84 г/cм3) и доводят водой до метки. В 1 мл этого раствора содержится 1 мг иона Си2+.
2. Построение градyuровочного графика.
В шесть мерных колб вместимостью по 50 мл отмерьте пипеткой соответственно 25, 20,15,10,5 и 2,5 мл стандартного раствора соли меди. В каждую из колб прибавьте по 1 О мл разбавленного (1 :3) раствора аммиака и доведите объемы дистиллированной водой до метки.
Измерение оптической плотности стандартных растворов.
-
Включить прибор в электросеть и прогреть 15 мин.
-
Закрыть шторки (2).
-
Рукоятку светофильтра (8) поставить в положение «7» (желтый светофильтр).
-
При закрытых шторках (2) поставить рукоятку чувствительности (6) в среднее положение.
-
Ручкой (7) стрелку на амперметре привести в положение «О» (при закрытых шторках).
-
На барабанах (5) установить «О» по красной шкале.
-
Рукоятку (3) поставить в положение «3».
-
Поставить воду в кюветах в держатели кювет. Рукояткой (4) установить их в проходящем свете, закрыть крышку, открыть шторки.
-
Установить стрелку на микроамперметре (1) в положение «О», вращая правый барабан (5).
Затем правый барабан больше не трогать!
-
Закрыть шторки, открыть крышку. Поставить первый стандартный раствор (имеющий наибольшую концентрацию меди) в правый держатель кювет и перевести его в нужное положение (в поток световых лучей). закрыть крышку, откpыть шторки. Вращая левый барабан (5) установить стрелку на микроамперметре (1) в положение «О». Сделать отсчет по красной шкале левого барабана и записать.
-
Аналогично определить оптическую плотность остальных стандартных растворов, данные занести в таблицу.
|
|
|
|
|
|
|||||||
|
|
1 |
2 |
3 |
4 |
5 |
6 |
Исп. р-р |
||||
|
С,мг/мл |
0,5 |
0,4 |
0,3 |
0,2 |
0,1 |
0,06 |
|
||||
|
А |
|
|
|
|
|
|
|
||||
Таблица. Оптическая плотность растворов
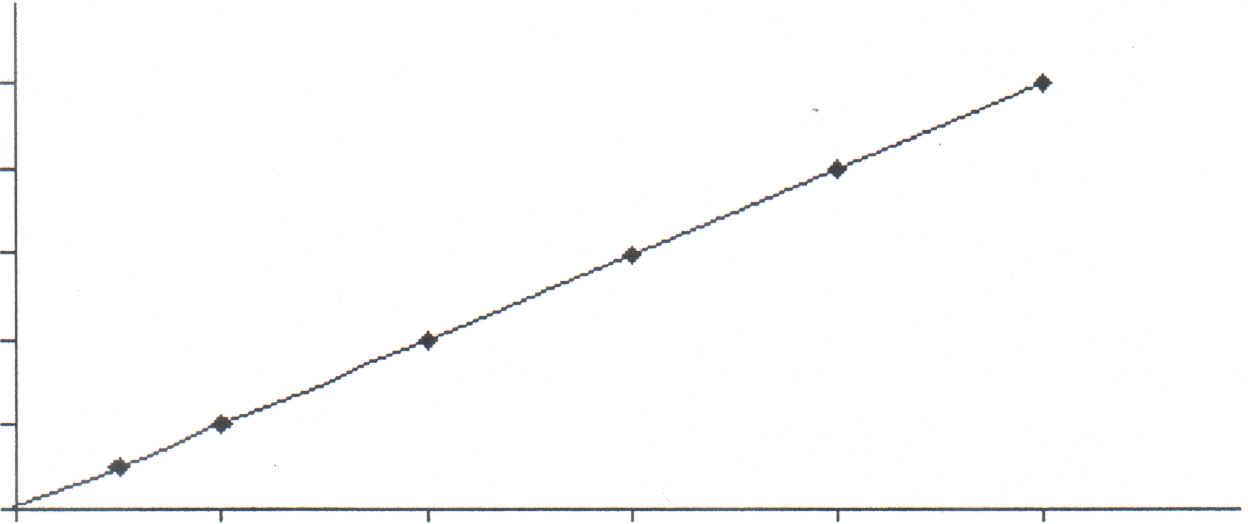
Измерив оптическую плотность А всех растворов, постройте градуировочный график. При этом по горизонтали оси откладывайте известные концентрации ионов Си2+ (т.е. 0,5; 0,4; 0,3; 0,2; 0,1; 0,06 мг меди в 1 мл), а по вертикальной - соответствующие им оптические плотности растворов.
Градуировочный граqик
А
о
0,1
0,2
0,3
0,4
0,5
С, мг/мrr
3. Определение меди в исследуемом растворе.
В колбу с исследуемым раствором (получить у лаборанта) прилейте разбавленный раствор (1:3) аммиака в объеме 10 мл и доведите объем в колбе водой до метки.
Раствор тщательно перемешайте, наполните им кювету с рабочей шириной 1 см и измерьте его оптическую плотность при тех же условиях, при каких был получен градуировочный график.
Зная величину оптической плотности, найдите по градуировочному графику концентрацию иона Cu2+ в миллиграммах на 1 мл раствора. Умножив ее на объем всего анализируемого раствора (50 мл), вычислите общую массу меди.

