
- •Абсорбционная спектроскопия в
- •Спектроскопия — разделы физики и аналитической химии, посвящённые изучению спектров взаимодействия излучения (в
- •Электромагнитный спектр
- •Закон Бера-Бугера-Ламберта
- •• Условия применения закона Бугера- Ламберта-
- ••Закон аддитивности
- •Схема энергетических состояний двухатомной молекулы
- •Способы изображения электронных спектров
- •Вид полосы поглощения
- •Характеристики спектра поглощения
- •Энергия
- •Типы молекулярных
- •Классификация полос поглощения.
- •Взаимосвязь электронных спектров и
- •Основные хромофорные группы
- •Взаимосвязь электронных спектров и структуры органических молекул
- •Типы смещений полосы поглощения в УФ-спектре
- •Изменение спектральных характеристик систем с сопряженными связями
- •Механизм возникновения гипсо- и батохромных сдвигов в электронных спектрах
- •Синее смещение полосы поглощения (n → π* переход) карбонильной группы в следующем ряду
- •Гипсохромный и батохромный сдвиги для n → π*
- •Электронные спектры поглощения основных классов органических
- •Электронные спектры поглощения основных классов органических
- •Электронные спектры поглощения основных классов органических
- •Электронные спектры поглощения основных классов органических
- •Вид спектра монозамещенных бензола
- ••Количественный спектральный анализ
- •Нефелометрический и турбидиметрический анализ
- •В нефелометрическом и турбидиметрическом анализе используется явление рассеяния света твердыми частицами, находящимися в
- ••Метод с измерением интенсивности рассеянного света под углом 90о (или каким- либо другим)
- •Применение методов, основанных на
Характеристики спектра поглощения
Положение максимума по шкале длин волн –
характеризуется типом электронных переходов и их энергией. Это качественная характеристика
спектра E= hc/ max
Высота максимума – соответствует вероятности электронного перехода. Чем больше вероятность
перехода, тем выше максимум, тем больше величины А, . Это количественная характеристика спектра.
Характер, форма максимума –определяется расстоянием между половинными значениями max .
Зависит и определяется глубиной расположения орбиты на которую осуществляются переходы , температурой и окружением молекулами растворителя.
Число полос поглощения (число максимумов) в спектре поглощения –определяется числом разрешенных переходов.
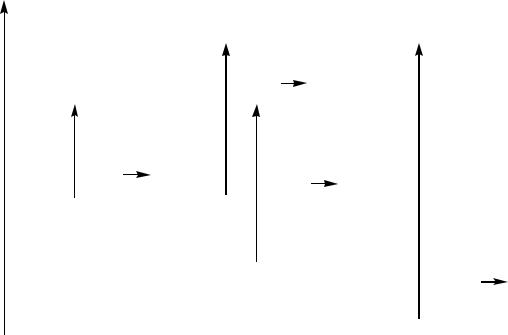
Энергия
Относительные энергии электронных переходов
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
----------------------------------------------- |
|
|
|||||||||||||||||
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
n |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
------------------------ |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
n |
|
|
|
n |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
-------------------- |
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
------------------------ |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
---------------------------------------------- |
|
|
|||||||||||||||||
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
||||||||||||||||||
•-связи характерны для молекул с одинарными связями (метан, этан)
•-связи преимущественны для молекул с двойными и кратными связями (ароматические соединения)
•n-орбитали имеют спирты, органические
сульфиды,эфиры и многие другие.
Типы молекулярных
орбиталей
• пять типов молекулярных орбиталей:-, -, *, * и n.
• переходы - *, *, n *, n *,
• -орбитали-электроны одинарных связей (C–C, C–H, C–O, C–N, C–S, C–Hlg)
• -орбитали-электроны кратных связей (С=С, С=N, C=O, и др.)
• n-орбитали -молекулы, содержащие гетероатомы с неподелёнными электронными парами (O: , N: , S: , Hlg:
и др.)
Классификация полос поглощения.
K-полосы (нем. konjugiert – сопряженный) – полосы высокой интенсивности, характерные для систем, содержащих сопряженные связи.
*-переходы 103
R-полосы (нем. radikalartig – радикальный) – полосы средней или низкой интенсивности характерные для систем, содержащих не поделенные электронные пары гетероатомных функциональных групп и радикалов. n *-переходы с 102 При переходе от неполярного растворителя к полярному или введении полярного заместителя K-полосы претерпевают
батохромный сдвиг, а R-полосы – гипсохромный сдвиг.
Полосы, обусловленные наличием в молекуле

Взаимосвязь электронных спектров и
структуры органических молекул
Хромофоры
Хромофор -простая функциональная группа, ответственная за поглощение с характеристическими
величинами и
X - - Y спектр соединения - сумма спектральных характеристик индивидуальных хромофоров X и Y
X - Y |
новый, хромофор с новыми спектральными |
|
характеристиками |
Ауксохром – функциональная группа, которая сама по себе не поглощает в близком ультрафиолете, но может влиять на поведение сопряженного с ней хромофора
Типичные ауксохромы: -SH, -NH2 , -OH
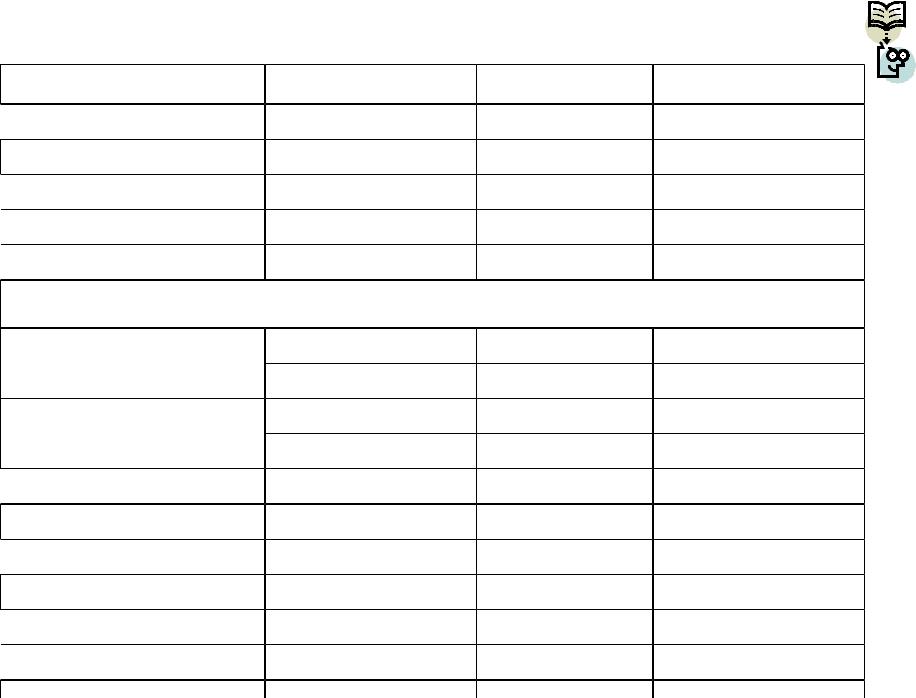
Основные хромофорные группы
Хромофор
 нитрилы
нитрилы
алкины
 алкены
алкены  спирты
спирты  простые эфиры
простые эфиры
кетоны
альдегиды
 амины
амины
кислоты
 сложные эфиры
сложные эфиры
амиды
 тиоспирты
тиоспирты  нитросоединения
нитросоединения
азосоединения
Тип перехода |
λmax |
log(ε) |
n → π* |
160 |
<1.0 |
π→ π* |
170 |
3.0 |
π→ π* |
175 |
3.0 |
n→σ* |
180 |
2.5 |
n→σ* |
180 |
3.5 |
π→ π* |
180 |
3.0 |
n → π* |
280 |
1.5 |
π→ π* |
190 |
2.0 |
n → π* |
290 |
1.0 |
n→σ* |
190 |
3.5 |
n → π* |
205 |
1.5 |
n → π* |
205 |
1.5 |
n → π* |
210 |
1.5 |
n → π* |
210 |
3.0 |
n → π* |
271 |
<1.0 |
n → π* |
340 |
<1.0 |
|
|
|
Взаимосвязь электронных спектров и структуры органических молекул
Для характеристики спектральных изменений, вызванных модификацией структуры, введены специальные термины:
гипсохромный сдвиг (синий сдвиг) – для смещения полос поглощения в коротковолновую область
спектра;
батохромный сдвиг (красный сдвиг) – для смещения полос
поглощения в область
длинных волн;
гиперхромный эффект – увеличение интенсивности поглощения;
гипохромный эффект – уменьшение интенсивности

Типы смещений полосы поглощения в УФ-спектре
Изменение спектральных характеристик систем с сопряженными связями
•Наличие системы сопряженных кратных связей вносит принципиальные изменения в спектры: в этих случаях наблюдается
изменение и максимума и интенсивности поглощения. В этих системах полосы поглощения невозможно приписать отдельным структурным элементам , ответственной за поглощение становится вся система сопряженных связей.
•в сопряженных системах полосы поглощения обладают гораздо большей интенсивностью (К-полосы, lgε > 4), чем в несопряженных, причем коэффициент экстинкции возрастает с увеличением цепи сопряжения . CH2=CH–CH=CH2 λмакс., нм = 218 ;ε (л/моль•см)=23000
CH3CH=CH–CH=CH2 λмакс., нм =223 |
ε(л /моль•см) = 25000 |
• |
242 ε (л/моль•см)= 26000 |
(CH3)2C=CH–CH=C(CH3)2 λмакс., нм = |
|
• |
|
•Сопряжение ненасыщенных хромофоров приводит к батохромному смещению соответствующих полос поглощения.
•смещение полосы поглощения закономерно зависит от протяженности системы сопряженных связей.
•для сопряженных систем характерно увеличение интенсивности поглощения.
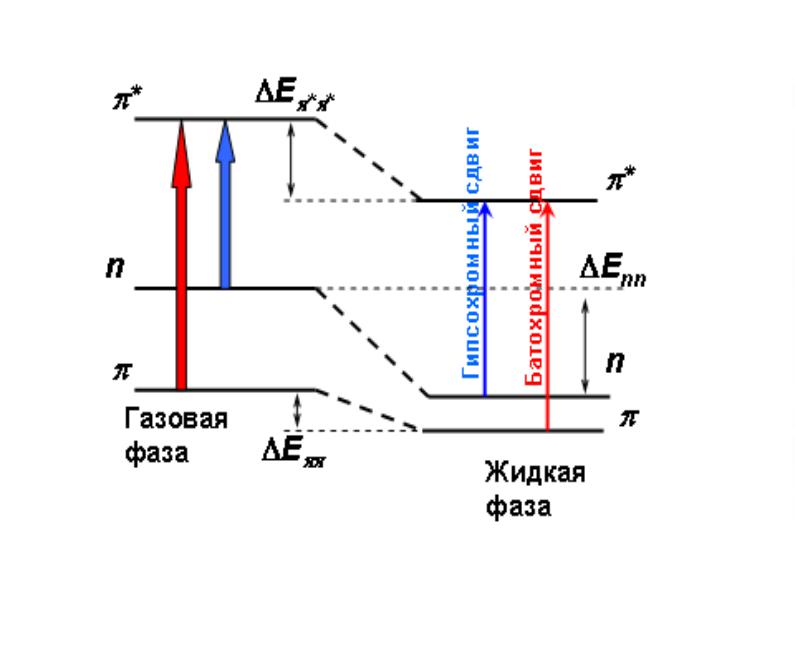
Механизм возникновения гипсо- и батохромных сдвигов в электронных спектрах
поглощения под влиянием растворителя.
