
- •0. Элементы волновой оптики
- •1. Развитие взглядов на природу света — корпускулярная теория Ньютона, волновая — Гюйгенса-Френеля. Законы геометрической оптики.
- •2. Интерференция света. Когерентность. Условия максимумов и минимумов интенсивности в общем виде.
- •3. Интерференция света при отражении от тонких пленок. Оптическая длина пути.
- •4. Дифракция света. Метод зон Френеля. Дифракция Френеля на круглом отверстии, диске. Зонная пластинка. Дифракция Фраунгофера на щели. Дифракционная решетка.
- •5. Поляризация света. Закон Малюса. Поляризация света при отражении. Закон Брюстера.
- •7. Основные положения атомной физики. Постулаты Бора. Опыт Франка и Герца. Недостатки теории Бора.
- •8. Гипотеза де Бройля. Опыты по дифракции электронов (Дэвиссона и Джермера, Тартаковского). Соотношения неопределённости Гейзенберга.
- •9. Волновая функция. Уравнение Шредингера. Стационарное уравнение Шредингера. Физический смысл и свойства волновой функции. Волновая функция свободно движущейся частицы. Микрочастица в бесконечно глубокой одномерной потенциальной яме.
- •10. Излучение и поглощение света атомами. Инверсная населенность уровней. Принцип действия и устройство лазера.
- •11. Элементы зонной теории твёрдого тела. Металлы, полупроводники и диэлектрики в зонной теории.
света, а зависит только от его частоты;
• фототок выходит на насыщение. |
|
|
|
Вольтамперная характеристика. |
|
|
|
U0 - потенциал задержки (ток прекращается). eU 0= |
mV max2 |
, V max2 |
- max скорость |
|
|||
2 |
|
|
|
выбитых электронов. |
|
|
|
Уравнение Эйнштейна.
По Эйнштейну энергия не только излучается дискретно, но и распространяется и взаимодействует тоже дискретно. При фотоэффекте электрон проводимости металла, поглощая фотон, получает его энергию hν . Для высвобождения из металла электрон должен совершить работу выхода A . Поэтому уравнение Эйнштейна для фотоэффекта, выражающее закон сохранения энергии, имеет вид:
hv= A+ |
mV max2 |
, |
m |
— масса электрона, υmax – максимальная начальная скорость |
|||
|
|||||||
|
|
2 |
|
|
|
|
|
фотоэлектронов, связанная с так называемым задерживающим потенциалом U0 |
|||||||
соотношением |
mV max2 |
=eU 0 |
; e — абсолютная величина заряда электрона. hν 0 = A , v0 |
||||
2 |
|
||||||
|
|
|
|
|
|
|
|
— min частота, |
hc = A |
|
, |
λ0 |
— max длина волны. |
||
|
|
λ0 |
|
|
|
|
|
7. Основные положения атомной физики. Постулаты Бора. Опыт Франка и Герца. Недостатки теории Бора.
Основные положения атомной физики.
Ядро атома состоит из:
•нуклонов
• протонов ( p или 11 H )
•нейтронов ( 10 p )
Любой элемент таблицы Менделеева можно представить: AZ X
Z — это
•порядковый номер элемента в таблице Менделеева;
•число протонов в ядре (заряд ядра атома равен произведению элементарного
электрического заряда е на его порядковый номер Z: q=eZ ;
•число электронов в атоме (атом в целом электрически нейтрален)
A — это
•массовое число (в таблице Менделеева);
• общее число нуклонов в ядре: A=Z +N , где N — число нейтронов в ядре
Ядерные реакции — превращения одних атомных ядер в другие при взаимодействии их с элементарными частицами или друг с другом.
Радиоактивность — способность атомных ядер некоторых элементов спонтанно распадаться, превращаясь в ядра другого элемента.
Закон сохранения зарядового числа (закон сохранения заряда): сумма нижних индексов частиц, вступивших в ядерную реакцию, равна сумме нижних индексов частиц, полученных в результате реакции.
Закон сохранения массового числа (закон сохранения массы): сумма верхних индексов частиц, вступивших в реакцию, равна сумме верхних индексов частиц, полученных в результате реакции.
Дефект массы ядра
m=Zmp+( A−Z )mn −mя
Энергия связи атомного ядра
ECB=Δ mc2
Энергия ядерной реакции
E=Δ m=931,5 МэВ
Альфа-частицы ( α ) — это ядра атома гелия: 42 He .
Бета-частицы ( β ) — это электроны, летящие со скоростью, близкой к скорости света.
Гамма-кванты ( γ ) - жесткое электромагнитное излучение мяпой длины волны ( 10−11 :10−12 м )
Правило смещения при α -распаде
AZ X →42 He+AZ−−42Y
Правило смещения при β -распаде
AZ X →−01e +Z +A1Y
Закон радиоактивного распада
−1
N=N 0 2 T или N=N 0 e−λ t
λ=2,71828
Период полураспада Т- время, в течение которого распадается половина наличного числа радиоактивных атомов.
Постулаты Бора.
Первый постулат Бора – постоянство орбит — электроны в атоме движутся по стационарным орбитам не излучая при этом энергию. Орбиты должны удовлетворять двум критериям:
• |
Классический: F =ma |
n |
— нормальное ускорение, |
1 |
|
ze2 |
=mV 2 |
— закон |
|
|
|||||||
|
Кулона. |
|
4 π E0 rn2 |
rn |
|
|||
|
|
|
|
|
|
|
|
|
• |
Квантовый: mVrn =n η |
|
mVrn — момент импульса, может принимать |
pr n |
||||
|
устойчивых значений (квантуется), n — главное квантовое число. |
|
||||||
rn= 4 π E0 η2 n2 — радиусы электронных орбит. mze2
Wпот= |
−mz2 e4 |
Wкин= |
mz2 e4 |
|
16 π2 E02 η2 n2 |
32 π2 E02 η2 n2 |
|||
|
|
Энергия электрона может принимать только определенные дискретные значения (квантуется). Электрон находится в определенном энергетическом состоянии или на определенном энергетическом уровне.
Второй постулат — постулат частот — электрон излучает энергию в виде кванта при переходе с более высокого уровня на более низкий, причем hv=En−Em , где En и Em
— соответственно энергии стационарных состояний атома до и после излучения (поглощения).
Опыт Франка и Герца.
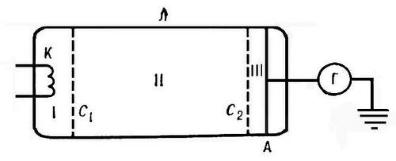
Опыт Франка-Герца — опыт, явившийся экспериментальным доказательством дискретности внутренней энергии атома. Поставлен в 1913 Дж. Франком и Г. Герцем.
На рисунке приведена схема |
|
|
|
|
|
|
|
|||
опыта. К катоду К |
и сетке |
C1 |
|
|
|
|
|
|
|
|
электровакуумной трубки, |
|
|
|
|
|
|
|
|
||
наполненной парами |
Hg (ртути), прикладывается разность потенциалов |
V |
, |
|
||||||
ускоряющая электроны, и снимается вольт-амперная характеристика. К сетке |
C2 |
и аноду |
||||||||
А прикладывается замедляющая разность потенциалов. Ускоренные в области |
I |
|||||||||
электроны испытывают соударения с атомами Hg |
в области |
II |
. Если энергия |
|
||||||
электронов после соударения достаточна для преодоления замедляющего потенциала в |
||||||||||
области |
III , то они попадут на анод. Следовательно, показания гальванометра |
Г |
||||||||
зависят от потери электронами энергии при ударе. |
|
|
|
|
|
|
|
|||
В опыте наблюдался монотонный рост тока |
I |
при увеличении ускоряющего |
||||||||
напряжения вплоть до 4,9 В |
, то есть электроны с энергией |
Е<4,9 эВ испытывали |
||||||||
упругие соударения с атомами |
Hg , и внутренняя энергия атомов не менялась. При |
|||||||||
значении |
V =4,9 В |
(и кратных ему значениях |
9,8 В , 14,7 В |
) появлялись резкие спады |
||||||
тока. Это определённым образом указывало на то, что при этих значениях |
V |
соударения |
||||||||
электронов с атомами носят неупругий характер, то есть энергия электронов достаточна для возбуждения атомов Hg . При кратных 4,9 эВ значениях энергии электроны могут испытывать неупругие столкновения несколько раз.
Таким образом, опыт Франка — Герца показал, что спектр поглощаемой атомом энергии не непрерывен, а дискретен, минимальная порция (квант электромагнитного поля),
которую может поглотить атом |
Hg |
, равна 4,9 эВ . Значение длины волны |
|||||||
λ=253,7 нм |
свечения паров |
Hg |
, возникавшее при V >4,9 В , оказалось в |
||||||
соответствии со вторым постулатом Бора |
|||||||||
E |
−E |
= hc |
, где |
E |
0 |
и |
E |
1 |
— энергии основного и возбужденного уровней |
1 |
0 |
λ |
|
|
|
|
|
||
энергии. В опыте Франка — Герца |
E0−E1=4,9 эВ . |
||||||||
Недостатки теории Бора.
•Не смогла объяснить интенсивность спектральных линий.
•Справедлива только для водородоподобных атомов и не работает для атомов, следующих за ним в таблице Менделеева.
•Теория Бора логически противоречива: не является ни классической, ни квантовой. В
системе двух уравнений, лежащих в её основе, одно — уравнение движения электрона
— классическое, другое — уравнение квантования орбит — квантовое.
8.Гипотеза де Бройля. Опыты по дифракции электронов (Дэвиссона и Джермера, Тартаковского). Соотношения неопределённости Гейзенберга.
Гипотеза де Бройля.
Бройль предположил, что движение частиц можно связать с распространением волн, описать движение частиц на волновом языке. Движущейся со скоростью v частице
соответствует так называемая волна де Бройля длиной |
|
λ= |
h |
– формула де Бройля , где |
|||||||||
p |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
12.65 |
|
|
̊ |
|
|||||
p – импульс частицы p=√2 me Δϕ , |
λ= |
|
A |
|
|
||||||||
|
|
|
|
|
|||||||||
|
|
|
|
√Δϕ |
B |
|
|||||||
Опыты по дифракции электронов
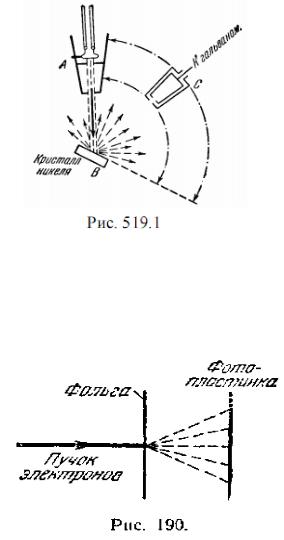
Опыты Дэвиссона и Джермера - исследование отражения электронов от монокристалла никеля. Установка включала в себя монокристалл никеля, сошлифованный под углом и установленный на держателе. На плоскость шлифа направлялся перпендикулярно пучок монохроматических электронов.
Под углом ψ к падающему пучку электронов устанавливался цилиндр Фарадея, соединённый с чувствительным гальванометром. По показаниям гальванометра определялась интенсивность отражённого от кристалла электронного пучка.
При различных значениях углов и скоростей, в отражённых лучах наблюдаются максимумы и минимумы интенсивности. Условие максимума:
Δ=2dsin θ=λ n , n=1,2, ...
Здесь d — межплоскостное расстояние.
Опыт Тартаковского - получение дифракционной картины при прохождении электронного пучка через металлическую фольгу. Пучок электронов, ускоренных разностью потенциалов порядка нескольких десятков киловольт, проходил через тонкую металлическую фольгу и попадал на фотопластинку. Электрон при ударе о фотопластинку оказывает на нее такое же действие, как и фотон.
