- •Введение
- •1. Растворы электролитов
- •1.1. Основные положения теории электролитической диссоциации с.Аррениуса
- •1.2. Механизмы образования растворов электролитов
- •1.3. Электропроводность растворов электролита
- •1.4. Электродный потенциал и его возникновение
- •Контрольные вопросы
- •Примеры решения задач
- •Задачи для самостоятельной работы:
- •2. Гальванический элемент
- •2.1. Общие понятия о работе гальванического элемента
- •2.2. Стандартный электродный потенциал
- •2.3. Ряд стандартных электродных потенциалов металлов
- •2.4. Поляризация и перенапряжение
- •2.5. Термодинамика обратимых электрохимических систем
- •2.6. Классификация электродов
- •2.7. Электрохимические цепи
- •Контрольные вопросы
- •Примеры решения задач
- •Задачи для самостоятельной работы:
- •3. Электролиз
- •3.1. Сущность электролиза
- •3.2. Электрохимическая система (ячейка)
- •3.3. Электролиз водных растворов
- •3.4. Поляризация электродов в процессе электролиза
- •3.5. Напряжение разложения. Явление перенапряжения
- •3.6. Электролиз органических соединений
- •3.7. Законы электролиза. Выход по току
- •3.8. Применение электролиза
- •Контрольные вопросы
- •Примеры решения задач
- •Задачи для самостоятельной работы:
- •4. Коррозия металлов
- •4.1. Классификации коррозионных процессов
- •4.2. Химическая коррозия
- •4.2.1. Взаимодействие с кислородом
- •4.2.2. Факторы, влияющие на скорость химической коррозии
- •4.2.3. Коррозия металлов в жидкостях – неэлектролитах
- •4.2.4. Сероводородная коррозия
- •Водородное охрупчивание металла
- •4.3. Электрохимическая коррозия (микрогальванокоррозия)
- •4.3.1. Условия протекания электрохимической коррозии
- •4.3.2. Диаграмма Пурбэ
- •4.3.3. Атмосферная коррозия металлов
- •4.3.4. Коррозия в морской воде
- •4.3.5. Подземная коррозия трубопроводов
- •4.4. Биохимическая коррозия
- •4.5. Коррозия блуждающими токами
- •4.6. Поляризация электродных процессов при коррозии
- •4.7. Защита металлов от коррозии
- •4.7.1. Легирование
- •4.7.2. Защитные покрытия
- •Методы борьбы с подземной коррозией
- •4.7.3. Металлические защитные покрытия
- •4.7.4. Электрохимическая защита
- •Методы борьбы с блуждающими токами
- •4.7.5. Ингибиторы коррозии металлов
- •4.7.6. Способы защиты от коррозии в морской воде
- •Контрольные вопросы
- •Примеры решения задач
- •Задачи для самостоятельной работы:
- •Тесты для самостоятельного решения
- •Перенапряжение катодного восстановления водорода и некоторых металлов из водных растворов при 25 0с
- •Значения фактора Пиллинга-Бэдвордса для некоторых металлов
1.3. Электропроводность растворов электролита
Мерой способности веществ проводить электрический ток является электрическая проводимость L– величина, обратная электрическому сопротивлениюR. Так как
|
|
(1.31) |
то
|
|
(1.32) |
где ρ– удельное сопротивление, Ом.м;S– поперечное сечение, м2;l– длина проводника, м; æ – удельная электрическая проводимость, См/м.
Удельная электрическая проводимость раствора электролита – это электрическая проводимость объема раствора, заключенного между двумя параллельными электродами, имеющими площадь по 1 м2и расположенными на расстоянии 1 м друг от друга. Удельная электрическая проводимость раствора электролита определяется количеством ионов, переносящих электричество, и скоростью их миграции.
Зависимость удельной электрической проводимости растворов некоторых электролитов от концентрации представлена на рис. 2.
В разбавленных растворах сильных и слабых электролитов рост электрической проводимости с концентрацией обусловлен увеличением числа ионов, переносящих электричество. В области концентрированных растворов повышение концентрации сопровождается увеличением вязкости раствора, что снижает скорость движения ионов и электрическую проводимость. Кроме того, у слабых электролитов в концентрированных растворах заметно снижается степень диссоциации и, следовательно, число ионов, переносящих электричество.
|
|
|
Рис. 2. Зависимость удельной электрической проводимости растворов некоторых электролитов от концентрации |
Молярная электрическая проводимость раствора – мера электрической проводимости всех ионов, образующихся при диссоциации 1 моль электролита при данной концентрации. Она численно равна электрической проводимости объема V(м3) раствора, заключенного между двумя параллельными электродами, с расстоянием между электродами 1 м, причем каждый электрод имеет такую площадь, чтобы в этом объеме содержался 1 моль растворенного вещества. Между молярной и удельной электрической проводимостью имеется соотношение
|
|
(1.33) |
где λ– молярная электрическая проводимость, См.м2/моль; æ – удельная электрическая проводимость, См/м;V– разведение раствора, м3/моль;с– концентрация, моль/м3.
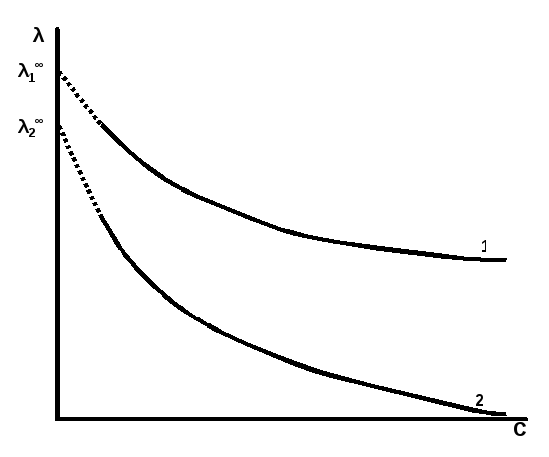
Общий характер изменения молярной электрической проводимости с концентрацией для сильных и слабых электролитов выражен кривыми, представленными на рис. 4. С увеличением разведения молярная электрическая проводимость возрастает и в области больших разведений стремится к предельному значению λ∞. Эта величина отвечает электрической проводимости бесконечно разбавленного раствора, характеризующегося полной диссоциацией электролита и отсутствием сил взаимодействия между ионами.
|
|
|
Рис. 3. Зависимость молярной электрической проводимости растворов сильных (1) и слабых (2) электролитов от концентрации |
В неравновесных условиях существование ионной атмосферы обусловливает два эффекта, тормозящих движение центрального иона, которые называются электрофоретическим и релаксационным эффектами торможения.
Электрофоретический эффект связан с тем, что ион под действием внешнего электрического поля перемещается не в неподвижной среде, а в потоке движущихся ему навстречу противоионов. Поскольку ионы гидратированы, то движение центрального иона происходит не в неподвижной среде, а в среде, перемещающейся ему навстречу. Поэтому движущийся ион находится под влиянием дополнительной тормозящей силы, что приводит к снижению его скорости.
Релаксационный эффект торможения обусловлен конечным временем разрушения ионной атмосферы. Согласно электростатической теории растворов сильных электролитов ионная атмосфера обладает центральной симметрией. При движении иона в электрическом поле симметрия ионной атмосферы нарушается. Это связано с тем, что перемещение иона сопровождается разрушением ионной атмосферы в одном положении иона и формированием ее в другом, новом. Этот процесс происходит с конечной скоростью в течение некоторого времени – времени релаксации. Вследствие этого ионная атмосфера теряет центральную симметрию, и позади движущегося иона всегда будет некоторый избыток заряда противоположного знака. Возникающие при этом силы электростатического притяжения будут тормозить движение иона.