
- •Оглавление
- •2.Термодинамическая система
- •3. Опытные законы идеального газа
- •4. Уравнение состояния идеального газа
- •1 Объём азота соединяется с 3 объёмами водорода с образованием 2 объёмов аммиака:
- •5. Основное уравнение молекулярно-кинетической теории идеальных газов
- •6. Закон Максвелла для распределения молекул идеального газа по скоростям и энергиям теплового движения
- •7. Барометрическая формула. Распределение Больцмана
- •8. Среднее число столкновений и средняя длина свободного пробега
- •10. Явления переноса
4. Уравнение состояния идеального газа
Уравнение состояния идеального газа (иногда уравнение Клапейрона или уравнение Менделеева — Клапейрона) — формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой идеального газа. Уравнение имеет вид:
![]()
где
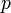 — давление,
— давление,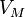 — молярный
объём,
— молярный
объём,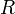 — универсальная
газовая постоянная
— универсальная
газовая постоянная — абсолютная
температура,К.
— абсолютная
температура,К.
Так
как ![]() ,
где
,
где![]() —количество
вещества,
а
—количество
вещества,
а ![]() ,
где
,
где![]() —
масса,
—
масса,![]() —молярная
масса,
уравнение состояния можно записать:
—молярная
масса,
уравнение состояния можно записать:
![]()
Эта форма записи носит имя уравнения (закона) Менделеева — Клапейрона.
В случае постоянной массы газа уравнение можно записать в виде:
![]()
![]()
Последнее уравнение называют объединённым газовым законом. Из него получаются законы Бойля — Мариотта, Шарля и Гей-Люссака:
![]() — закон
Бойля — Мариотта.
— закон
Бойля — Мариотта.
![]() — Закон
Гей-Люссака.
— Закон
Гей-Люссака.
![]() — закон Шарля (второй
закон Гей-Люссака, 1808 г.).А
в форме пропорции
— закон Шарля (второй
закон Гей-Люссака, 1808 г.).А
в форме пропорции ![]() этот
закон удобен для расчёта перевода газа
из одного состояния в другое. С точки
зрения химика этот закон может звучать
несколько иначе: Объёмы вступающих в
реакцию газов при одинаковых условиях
(температуре, давлении) относятся друг
к другу и к объёмам образующихся
газообразных соединений как простые
целые числа. Например, 1 объёмводородасоединяется
с 1 объёмом хлора,
при этом образуются 2 объёма хлороводорода:
этот
закон удобен для расчёта перевода газа
из одного состояния в другое. С точки
зрения химика этот закон может звучать
несколько иначе: Объёмы вступающих в
реакцию газов при одинаковых условиях
(температуре, давлении) относятся друг
к другу и к объёмам образующихся
газообразных соединений как простые
целые числа. Например, 1 объёмводородасоединяется
с 1 объёмом хлора,
при этом образуются 2 объёма хлороводорода:
![]()
1 Объём азота соединяется с 3 объёмами водорода с образованием 2 объёмов аммиака:
![]()
![]() — закон
Бойля — Мариотта.
Закон Бойля — Мариотта назван в честь
ирландского физика, химика и философа Роберта
Бойля (1627—1691),
открывшего его в 1662 г., а также в честь
французского физика Эдма
Мариотта (1620—1684),
который открыл этот закон независимо
от Бойля в 1677 году. В некоторых случаях
(в газовой
динамике)
уравнение состояния идеального газа
удобно записывать в форме
— закон
Бойля — Мариотта.
Закон Бойля — Мариотта назван в честь
ирландского физика, химика и философа Роберта
Бойля (1627—1691),
открывшего его в 1662 г., а также в честь
французского физика Эдма
Мариотта (1620—1684),
который открыл этот закон независимо
от Бойля в 1677 году. В некоторых случаях
(в газовой
динамике)
уравнение состояния идеального газа
удобно записывать в форме
![]()
где ![]() —показатель
адиабаты,
—показатель
адиабаты, ![]() —
внутренняя энергия единицы массы
вещества.Эмиль
Амага обнаружил,
что при высоких давлениях поведение газов отклоняется
от закона Бойля — Мариотта. И это
обстоятельство может быть прояснено
на основании молекулярных представлений.
—
внутренняя энергия единицы массы
вещества.Эмиль
Амага обнаружил,
что при высоких давлениях поведение газов отклоняется
от закона Бойля — Мариотта. И это
обстоятельство может быть прояснено
на основании молекулярных представлений.
С
одной стороны, в сильно сжатых газах
размеры самих молекул являются сравнимыми
с расстояниями между молекулами. Таким
образом, свободное пространство, в
котором движутся молекулы, меньше, чем
полный объём газа. Это обстоятельство
увеличивает число ударов молекул в
стенку, так как благодаря ему сокращается
расстояние, которое должна пролететь
молекула, чтобы достигнуть стенки. С
другой стороны, в сильно сжатом и,
следовательно, более плотном газе
молекулы заметно притягиваются к другим
молекулам гораздо большую часть времени,
чем молекулы в разреженном газе. Это,
наоборот, уменьшает число ударов молекул
в стенку, так как при наличии притяжения
к другим молекулам молекулы газа движутся
по направлению к стенке с меньшей
скоростью, чем при отсутствии притяжения.
При не слишком больших давлениях более
существенным является второе обстоятельство
и произведение ![]() немного
уменьшается. При очень высоких давлениях
большую роль играет первое обстоятельство
и произведение
немного
уменьшается. При очень высоких давлениях
большую роль играет первое обстоятельство
и произведение![]() увеличивается.
увеличивается.
5. Основное уравнение молекулярно-кинетической теории идеальных газов
Для вывода основного уравнения молекулярно-кинетической теории рассмотрим одноатомный идеальный газ. Предположим, что молекулы газа движутся хаотически, число взаимных столкновений между молекулами газа пренебрежимо мало по сравнению с числом ударов о стенки сосуда, а соударения молекул со стенками сосуда абсолютно упругие. Выделим на стенке сосуда некоторую элементарную площадку DS и вычислим давление, оказываемое на эту площадку. При каждом соударении молекула, движущаяся перпендикулярно площадке, передает ей импульс m0v-(-m0v)=2m0v, где т0 — масса молекулы, v — ее скорость.
За время Dt площадки DS достигнут только те молекулы, которые заключены в объеме цилиндра с основанием DS и высотой vDt .Число этих молекул равно nDSvDt (n—концентрация молекул).
Необходимо, однако, учитывать, что реально молекулы движутся к площадке
DS под разными углами и имеют различные скорости, причем скорость молекул при каждом соударении меняется. Для упрощения расчетов хаотическое движение молекул заменяют движением вдоль трех взаимно перпендикулярных направлений, так что в любой момент времени вдоль каждого из них движется 1/3 молекул, причем половина молекул (1/6) движется вдоль данного направления в одну сторону, половина — в противоположную. Тогда число ударов молекул, движущихся в заданном направлении, о площадку DS будет 1/6nDSvDt. При столкновении с площадкой эти молекулы передадут ей импульс
DР = 2m0v•1/6nDSvDt=1/3nm0v2DSDt.
Тогда давление газа, оказываемое им на стенку сосуда,
p=DP/(DtDS)=1/3nm0v2. (3.1)
Если газ в объеме V содержит N молекул,
движущихся со скоростями v1, v2, ..., vN, то
целесообразно рассматривать среднюю квадратичную скорость
характеризующую всю совокупность молекул газа.
Уравнение (3.1) с учетом (3.2) примет вид
р = 1/3пт0 <vкв>2. (3.3)
Выражение (3.3) называется основным уравнением молекулярно-кинетической теории идеальных газов. Точный расчет с учетом движения молекул по все-
возможным направлениям дает ту же формулу.
Учитывая, что n = N/V, получим
где Е — суммарная кинетическая энергия поступательного движения всех молекул газа.
Так как масса газа m =Nm0, то уравнение (3.4) можно переписать в виде
pV=1/3m<vкв>2.
Для одного моля газа т = М (М — молярная масса), поэтому
pVm=1/3M<vкв>2,
где Vm — молярный объем. С другой стороны, по уравнению Клапейрона — Менделеева, pVm=RT. Таким образом,
RT=1/3М <vкв>2, откуда
Так как М = m0NA, где m0—масса одной молекулы, а NА — постоянная Авогадро, то из уравнения (3.6) следует, что
где k = R/NA—постоянная Больцмана. Отсюда найдем, что при комнатной температуре молекулы кислорода имеют среднюю квадратичную скорость 480 м/с, водорода — 1900 м/с. При температуре жидкого гелия те же скорости будут соответственно 40 и 160 м/с.
Средняя кинетическая энергия поступательного движения одной молекулы идеального газа
<e0) =E/N = m0 <vкв>)2/2 = 3/2kT(43.8)
(использовали формулы (3.5) и (3.7)) пропорциональна термодинамической температуре и зависит только от нее. Из этого уравнения следует, что при T=0 <e0> =0,,т. е. при 0 К прекращается поступательное движение молекул газа, а следовательно, его давление равно нулю. Таким образом, термодинамическая температура является мерой средней кинетической энергии поступательного движения молекул идеального газа и формула (3.8) раскрывает молекулярно-кинетическое толкование температуры.
