
Лысак Микробиология
.pdfэнергии и углерода самый широкий набор органических и неорганических соединений. Такая способность обусловлена различиями в наборе клеточных периферических ферментов или экзоферментов, которые выделяются наружу и разрушают макромолекулы исходных субстратов на более низкомолекулярные вещества. Эти ферменты относятся к классу гидролаз. Образующиеся в результате действия таких ферментов вещества поступают в клетку бактерий и подвергаются действию ферментов промежуточного метаболизма. Эти ферменты называются эндоферментами, так как они локализуются внутри клетки. Эндоферменты, синтезируемые микроорганизмами, относятся ко всем известным классам ферментов – оксидоредуктазы, трансферазы, гидролазы, лиазы, лигазы, изомеразы и др. Многие из эндоферментов локализованы на мембранах или на рибосомах. Они называются связанными ферментами. Другие ферменты находятся в свободном, растворённом состоянии в цитоплазме.
Набор ферментов в клетке может изменяться в зависимости от условий, в которых находятся бактерии. По этому свойству все ферменты подразделяют на 2 группы: конститутивные и индуцибельные. Конститутивные ферменты синтезируются постоянно, независимо от веществ субстрата. В клетке они находятся в более или менее постоянной концентрации. Примером конститутивных ферментов является ДНК-полимераза. Индуцибельные ферменты синтезируются в ответ на появление в среде субстрата-индуктора. К индуцибельным ферментам относится большинство гидролаз. Наличие индуцибельных ферментов обеспечивает быструю приспособляемость бактерий к конкретным условиям.
Таким образом, назначение метаболизма состоит в следующем:
- генерация энергии в молекулах АТФ или других богатых энергией соединениях;
- образование субъединиц, из которых синтезируются макромолекулы основных биополимеров клетки (белков, нуклеиновых кислот, полисахаридов, липидов);
-активация образованных субъединиц – перенос фосфатной группы с АТФ на субъединицы. При этом происходит затрата энергии. Однако, этот процесс необходим, потому что только активированные субъединицы способны вступать в реакции полимеризации;
-синтез специфических макромолекул из активированных субъединиц, т.е. их полимеризация. Полимеризация активированных субъединиц может происходить двумя способами:
119
а) реакции матричного синтеза (так синтезируются белки и нуклеиновые кислоты);
б) простая конденсация одинаковых активированных субъединиц (например, образование молекул крахмала из остатков глюкозы).
Теперь разберем как осуществляются основные типы энергетического и конструктивного метаболизма у бактерий.
6.1. Энергетический метаболизм
Мы уже установили, что все микроорганизмы по отношению к энергетическим источникам подразделяются на две группы: фототрофы и хемотрофы.
Хемотрофные микроорганизмы используют для синтеза молекул АТФ энергию, освобождаемую при химических реакциях, фототрофные – световую энергию в процессе фотосинтеза.
Образование молекул АТФ из АДФ может происходить двумя способами:
- фосфорилирование в дыхательной или фотосинтетической электронтранспортной цепи. Этот процесс у прокариот связан с мембранами или их производными, поэтому его называют мембранным фосфорилированием. Синтез АТФ в данном случае происходит при участии фермента АТФ-синтазы:
АДФ + Фн АТФ; - фосфорилирование на уровне субстрата. При этом фосфатная
АТФ; - фосфорилирование на уровне субстрата. При этом фосфатная
группа переносится на АДФ от вещества (субстрата), более богатого энергией, чем АТФ:
R ~ Ф + АДФ R + АТФ.
R + АТФ.
Такой способ синтеза АТФ получил название субстратного фосфорилирования. В клетке реакции субстратного фосфорилирования не связаны с мембранными структурами и катализируются растворимыми ферментами промежуточного метаболизма.
У хемотрофных бактерий генерация энергии в молекулах АТФ сводится к двум типам биохимических реакций: окисления и восстановления. Окисляться микроорганизмами могут самые разнообразные органические и неорганические вещества. Эти вещества являются донорами электронов. Поскольку электроны не могут самостоятельно существовать, они обязательно должны быть перенесены на молекулы, способные их воспринимать, т.е. восстанавливаться. Такие молекулы называются акцепторами электронов. Донором электронов не может быть предельно окисленное вещество, а их акцептором – предельно восстановленное.
120
дельно восстановленное. Таким образом, окисление субстратов происходит путём переноса электронов от донора к акцептору. При биологическом окислении чаще всего происходит одновременный перенос двух электронов; при этом от субстрата отщепляются также два протона (Н+). Такое окисление субстрата, происходящее с отщеплением двух протонов и двух электронов, называется дегидрированием. Поэтому нередко термины донор водорода и донор электронов употребляются как синонимы.
Все окислительно-восстановительные реакции энергетического метаболизма у хемотрофных микроорганизмов можно разделить на 3 типа, т.е. различают три типа энергетического метаболизма:
-аэробное дыхание или аэробное окисление,
-анаэробное дыхание,
-брожение.
Основным процессом энергетического метаболизма многих прокариот является аэробное дыхание, при котором донором водорода или электронов являются органические (реже неорганические) вещества, а конечным акцептором – молекулярный кислород. Основное количество энергии при аэробном дыхании образуется в электронтранспортной цепи, т.е. в результате мембранного фосфорилирования.
Анаэробное дыхание – цепь анаэробных окислительно-восстано- вительных реакций, которые сводятся к окислению органического или неорганического субстрата с использованием в качестве конечного акцептора электронов не молекулярного кислорода, а других неорганических веществ (нитрата – NO3-, нитрита – NO2- , сульфата – SO42-, сульфита – SO32-, CO2 и др.), а также органических веществ (фумарата и др.). Молекулы АТФ в процессе анаэробного дыхания образуется в основном в электронтранспортной цепи, т.е. в результате реакций мембранного фосфорилирования, но в количестве меньшем, чем при аэробном дыхании.
Брожение – совокупность анаэробных окислительно-восстанови- тельных реакций, при которых органические соединения служат как донорами, так и акцепторами электронов. Как правило, доноры и акцепторы электронов образуются из одного и того же субстрата, подвергающегося брожению (например, из углевода). Сбраживанию могут подвергаться различные субстраты, но лучше других используются углеводы. АТФ при брожении синтезируется в результате реакций субстратного фосфорилирования.
121
Наиболее выгодным типом окислительно-восстановительных реакций у бактерий, в результате которых генерируется энергия в молекулах АТФ, является аэробное дыхание, так как здесь происходит больший выход молекул АТФ. Наименее выгодным типом таких реакций является брожение, сопровождающееся минимальным энергетическим выходом.
Поскольку большинство микроорганизмов используют в качестве источника энергии углеводы, и в первую очередь глюкозу, рассмотрим основные пути её расщепления или катаболизма.
У бактерий возможны три пути катаболизма глюкозы:
1)гликолиз или фруктозодифосфатный путь или путь Эмбдена- Мейергофа-Парнаса (по имени исследователей, внесших большой вклад в изучение этого процесса);
2)окислительный пентозофосфатный путь или гексозомонофосфатный путь или путь Варбурга-Диккенса-Хореккера;
3)2-кето-3-дезокси-6-фосфоглюконатный путь (КДФГ-путь) или путь Энтнера-Дудорова.
Следует отметить, что все перечисленные пути катаболизма глюкозы у микроорганизмов могут протекать при разных типах энергетического метаболизма (аэробное дыхание, анаэробное дыхание, брожение).
Все пути катаболизма начинаются с того, что глюкоза в клетке сначала фосфорилируется при участии фермента гексокиназы и АТФ как донора фосфата. Образуется глюкозо-6-фосфат, который представляет метаболически активную форму глюкозы в клетке и служит исходным пунктом для любого из трёх путей катаболизма.
Пути расщепления глюкозы состоят из многих биохимических реакций, каждая из которых катализируется специфическим ферментом.
Наиболее распространённым путём катаболизма глюкозы у многих микроорганизмов является гликолиз. При этом глюкозо-6-фосфат изомеризуется с помощью глюкозофасфатизомеразы и фосфорилируется далее в фруктозо-1,6-дифосфат, который затем расщепляется на 3-фосфоглицериновый альдегид (3-ФГА) и фосфодиоксиацетон. Фосфодиоксиацетон под действием фермента триозофосфатизомеразы превращается в 3-ФГА. Таким образом, из одной молекулы глюкозы образуется 2 молекулы 3-ФГА. На эти реакции превращения глюкозы в 3-ФГА затрачивается энергия двух молекул АТФ. Далее происходит окисление каждой молекулы 3-ФГА до 1,3-дифосфоглицери- новой кислоты (1,3-ФГК) (рис. 32).
122
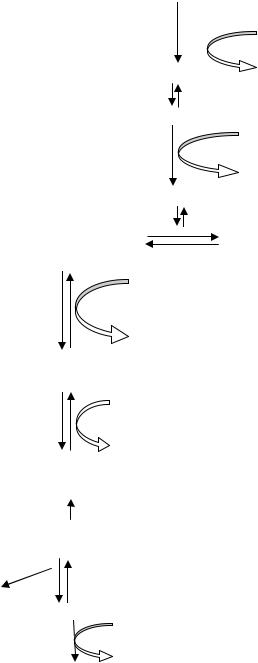
1,3-ФГК – высокоэнергетическое соединение, содержащее макроэргическую фосфатную связь, – реагирует с АДФ (фермент фосфоглицераткиназа), отдавая высокоэнергетическую фосфатную группу, в результате чего синтезируется молекула АТФ. Таким образом, энергия, освободившаяся при окислении 3-ФГА, путём субстратного фосфорилирования оказывается аккумулированной в молекуле АТФ. Образуется 3-ФГК.
Глюкоза
АТФ
гексокиназа
АДФ глюкозо-6-фосфат
глюкозофосфатизомераза
фруктозо-6-фосфат АТФ
6-фосфофруктокиназа
АДФ фруктозо-1,6-дифосфат
фруктозодифосфатальдолаза |
|
|
3-фосфоглицериновый |
диоксиацетонфосфат |
|
альдегид (3-ФГА) |
триозофосфатизомераза |
|
НАД
глицеральдегидфосфатдегидрогеназа
Фн НАД.Н2 1,3-дифосфоглицериновая
НАД.Н2 1,3-дифосфоглицериновая
кислота
фосфоглицераткиназа  АДФ
АДФ
АТФ 3-фосфоглицериновая
кислота
фосфоглицеромутаза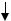
2-фосфоглицериновая кислота
енолаза
Н2О фосфоенолпируват
пируваткиназа |
АДФ |
Рис. 32. Гликолитический путь |
|
АТФ |
расщепления глюкозы. |
Пируват
123

O |
|
O |
׀׀ |
|
׀׀ |
C – O ~Ф |
фосфоглице- |
C – OН |
׀ |
раткиназа |
׀ |
Н- С – ОН + АДФ |
|
Н- С – ОН + АТФ. |
׀ |
|
׀ |
СН2О-Ф |
|
СН2О-Ф |
______________ |
|
______________ |
1,3-ФГК |
|
3-ФГК |
Далее 3-ФГК под действием фермента фосфоглицеромутазы превращается в 2-ФГК, из которой в результате отщепления воды образуется фосфоенолпировиноградная кислота (ФЕП). Это также высокоэнергетический фосфат, с которого богатая энергией фосфатная группа переносится пируваткиназой на АДФ, образуется молекула АТФ и пировиноградная кислота (ПВК). Это второе фосфорилирование на уровне субстрата:
СOОН |
|
|
СОOН |
|
׀ |
|
|
׀ |
|
C – O ~Ф |
|
|
C = O |
|
׀׀ |
+ АДФ |
пируваткиназа |
׀ |
+ АТФ. |
СН2 |
|
С Н3 |
||
____________ |
|
|
___________ |
|
ФЕП |
|
|
ПВК |
|
Таким образом, при распаде одной молекулы глюкозы образуется четыре молекулы АТФ, в которых аккумулируется освободившаяся при гликолизе энергия. Поскольку в самом начале процесса на активирование глюкозы были израсходованы две молекулы АТФ, чистый выход АТФ на одну молекулу глюкозы составляет 2 молекулы. Суммарное уравнение гликолиза можно записать следующим образом:
С6Н12О6 + 2 АДФ + 2Фн + 2 НАД  2С3Н4О3 + 2 АТФ + 2 НАД.Н2.
2С3Н4О3 + 2 АТФ + 2 НАД.Н2.
Второй, пентозофосфатный путь расщепления углеводов, характерен для некоторых представителей семейства Enterobacteriaceae, а также для гетероферментативных молочнокислых бактерий и некоторых маслянокислых бактерий.
124
В этом цикле глюкозо-6-фосфат, образующийся путём активирования глюкозы молекулой АТФ, превращается через ряд промежуточных реакций в 6-фосфоглюконовую кислоту, которая подвергается окислению и декарбоксилированию с образованием рибулозо-5- фосфата, СО2 и НАДФ.Н2 . Рибулозо-5-фосфат включается в сложный цикл, приводящий к образованию из его трёх молекул двух молекул глюкозо-6-фосфата и одной молекулы 3-фосфоглицеринового альдегида. Глюкозо-6-фосфат может снова включаться в цикл. А 3-ФГА превращается гликолитическим путём в пировиноградную кислоту.
С энергетической точки зрения этот путь катаболизма углеводов в два раза менее эффективен, чем гликолитический, так как на 1 молекулу глюкозы образуется только 1 молекула АТФ. Однако большое значение этого пути в том, что он обеспечивает клетки бактерий пентозами (рибулозо-5-фосфат), которые являются предшественниками нуклеотидов и нуклеиновых кислот. Кроме того, в этом цикле образуются 2 молекулы НАДФ.Н2, которые необходимы клетке для восстановительных реакций биосинтеза.
Путь Энтнера-Дудорова встречается у прокариот реже, чем другие. Он характерен в основном для псевдомонад и уксуснокислых бактерий. От пентозофосфатного пути он отличается тем, что 6- фосфо-глюконовая кислота превращается в пировиноградную кислоту и 3-ФГА. 3-ФГА гликолитическим путём также превращается в пировиноградную кислоту. Из 1 молекулы глюкозы в этом пути синтезируется 1 молекула АТФ, 1 молекула НАДФ.Н2 и 1 молекула НАД.Н2.
Следует подчеркнуть, что путь Энтнера-Дудорова является самым кратчайшим механизмом расщепления углеводов до пировиноградной кислоты.
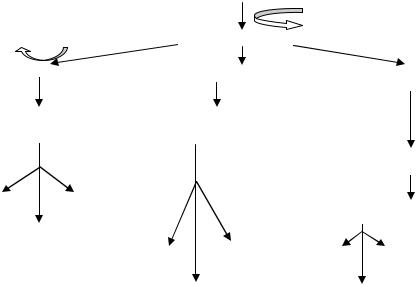
Энергетическую значимость различных путей катаболизма глюкозы можно представить из схемы (рис. 33).
Таким образом, рассмотрев пути катаболизма глюкозы, мы можем заключить, что важнейшим продуктом, образующимся в них, является пировиноградная кислота, которая подвергается дальнейшим превращениям. Пируват занимает центральное положение в промежуточном метаболизме и может служить предшественником многих продуктов.
Что же происходит с пировиноградной кислотой при различных типах энергетического метаболизма: аэробном дыхании, анаэробном дыхании и брожении?
125
|
|
|
|
|
ГЛЮКОЗА |
АТФ |
|
|
|||
|
|
|
|
|
|
|
|
|
|
||
|
АДФ |
АТФ |
|
глюкозо-6-фосфат |
АДФ |
|
|
||||
|
|
|
|
|
|
||||||
фруктозо-1,6-дифосфат |
6-фосфоглюконовая |
|
|
6-фосфоглюконовая |
|||||||
|
|
|
|
кислота |
|
|
кислота |
||||
|
|
|
|
|
|
||||||
3-фосфоглицериновый |
3-ФГА + |
пировиног- |
|
|
|
|
|||||
|
альдегид (3-ФГА) |
|
|
радная кислота |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
рибулозо-5-фосфат + СО2 |
|
|
|
|
|
|
|
|
|
|
|
||
2 АТФ |
2НАД . Н2 |
|
|
|
|
|
3-ФГА +2 глюкозо-6-фосфат |
||||
2 |
|
|
|
|
|
|
|
|
|
|
|
пировиноградная кислота |
АТФ |
НАД . Н2 |
АТФ |
2НАДФ . Н2 |
|||||||
|
|
|
|
||||||||
|
|
|
|
|
НАДФ . Н2 |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|||
|
|
|
пировиноградная кислота |
пировиноградная кислота |
|||||||
|
|
А |
|
Б |
|
|
В |
||||
Рис. 33 . Схема путей катаболизма глюкозы в клетках прокариот:
А– гликолиз; Б – путь Энтнера-Дудорова; В – пентозофосфатный путь.
6.1.1.Аэробное дыхание
Пировиноградная кислота, образующаяся одним из трех вышеперечисленных путей катаболизма глюкозы, окисляется до ацетил-КоА. В данном процессе работают ферменты пируватдегидрогеназы:
CH3-CO-COOH + KoA-SH + HAД+ 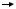 CH3-CO~KoA + НАД.Н2 + CO2.
CH3-CO~KoA + НАД.Н2 + CO2.
Ацетил-КоА является исходным субстратом цикла трикарбоновых кислот (цикла Кребса).
В цикл Кребса включается одна молекула ацетил-КоА, которая соединяется с оксалоацетатом. Этот процесс катализируется цитратсинтетазой. Продуктами реакции являются лимонная кислота и свободный коэнзим А. Лимонная кислота с помощью фермента аконитазы превращается в цис-акотиновую и изолимонную кислоты. Изолимонная кислота через щавелевоянтарную кислоту превращается в α-кетоглутаровую кислоту, которая подвергается дальнейшему декарбоксилированию.
126
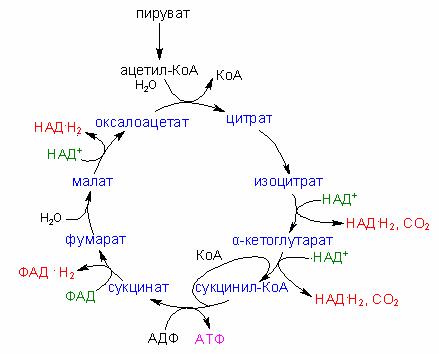
В конечном счете окисление ацетил-КоА в цикле трикарбоновых кислот (ЦТК) даёт: 2 молекулы СО2, 1 молекулу АТФ и 8 атомов водорода, из них 6 атомов водорода на уровне пиридиннуклеотидов и 2 атома – на уровне флавопротеинов (рис. 34).
Рис. 34. Цикл Кребса.
Таким образом, цикл трикарбоновых кислот выполняет функцию конечного окисления органических веществ. Но, кроме этого, цикл трикарбоновых кислот обеспечивает биосинтетические процессы клетки различными предшественниками, такими как оксалоацетат, сукцинат, α-кетоглутарат и др.
У некоторых бактерий цикл трикарбоновых кислот «разорван». Наиболее часто отсутствует ферментативный этап превращения α-кетоглутаровой кислоты в янтарную. В таком виде ЦТК не может функционировать в системе энергодающих механизмов клетки. Основная функция «разорванного» ЦТК – биосинтетическая.
НАД.Н2 и ФАД.Н2, образовавшиеся на разных этапах окисления органических веществ, поступают в дыхательную цепь, которая у бактерий находится в цитоплазматической мембране, а у эукариот в мембране митохондрий. В дыхательной цепи НАД.Н2 и ФАД.Н2 вновь окисляются до НАД и ФАД, а отщепившийся от них водород передаётся не менее через пять переносчиков к концу цепи, где соединяется с молекулярным кислородом, образуя воду (рис. 35).
127
ГЛЮКОЗА |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
АТФ + пировиноградная кислота + |
|
НАД . Н2 |
|
|
|
|
|
||||||||
|
|
|
|
||||||||||||
|
|
|
НАД |
|
|
||||||||||
СО2 |
|
НАД . Н2 |
|
|
|
|
|
|
|
||||||
|
|
|
|
||||||||||||
Ацетил-КоА |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
цикл |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Кребса |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
||||||||
2 СО2 + 1 АТФ + |
3 НАД . Н2 |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
1 ФАД . Н2 |
Дыхательная цепь |
|
АТФ |
|||||||||||
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
О2 |
Н2О |
||
Рис. 35 Схема аэробного дыхания. |
|
|
|||||||||||||
Переход водорода по дыхательной цепи состоит из ряда окисли- тельно-восстановительных реакций. В некоторых из этих реакций выделяется достаточно энергии для образования АТФ, и такой процесс носит название окислительного фосфорилирования. В реакциях окислительного фосфорилирования принимает участие специальный фермент АТФ-синтаза, который катализирует превращение АДФ в АТФ.
Дыхательные цепи микроорганизмов состоят из следующих важнейших локализованных в мембране переносчиков атомов водорода или электронов: флавопротеины, железосерные белки, хиноны и цитохромы.
Флавопротеины – коферменты, в состав которых входит витамин В2. В качестве простетических групп в них выступают флавинмононуклеотид (ФМН) или флавинадениндинуклеотид (ФАД). Флавопротеины осуществляют перенос атомов водорода, т.е. являются дегидрогеназами. Дегидрогеназа, содержащая в качестве простетической группы ФМН, является НАДФ.Н2-дегидрогеназой. Это стартовый переносчик дыхательной цепи, она осуществляет перенос водорода с НАДФ.Н2 на последующие компоненты дыхательной цепи. Дегидрогеназа, содержащая в качестве простетической группы ФАД, действует как сукцинатдегидрогеназа. Она катализирует окисление янтарной
128
