
- •Основные правила при работе в химической лаборатории.
- •Требования к технике безопасности при работе в химической лаборатории.
- •Оформление лабораторного журнала.
- •Лабораторная работа №1.
- •Посуда общего назначения
- •Посуда специального назначения
- •Мерная посуда.
- •Лабораторная работа №2.
- •Лабораторная работа №3.
- •Лабораторная работа №4.
- •Лабораторная работа №5.
- •Лабораторная работа № 6.
- •Лабораторная работа № 7.
- •Лабораторная работа №8.
- •Лабораторная работа №9.
- •Ю.И. Сухарев, и.Ю. Апаликова, н.В. Пыхова, и.Ю.Лебедева. Химия коллоидных систем; Учеб. Пособие по лабораторным работам - Челябинск: Изд-во ЧелГу, 2008. - 45 с.
- •Содержание
Лабораторная работа №9.
Определение жесткости воды
Цель работы: определить общую, карбонатную, некарбонатную и остаточную жесткость водопроводной воды.
Оборудование и реактивы:
1. Раствор ЭДТА (комплексона III, трилона Б), 0,05М;
2. Аммиачный буферный раствор;
3. Соляная кислота, 0,1н.;
4. Эриохром черный Т, сух.;
5. Метиловый оранжевый, 0,5% р-р.;
6. Бюретка, 25 мл.;
7. Колбы конические, 250 мл;
8. Пипетки, 5, 100мл;
9.Мерные колбы, 50 мл.
Ход работы:
1. Определение общей жесткости воды.
В коническую колбу на 250 мл пипеткой отбирают 100 мл водопроводной воды, затем добавляют 5 мл аммиачного буферного раствора, насыпают на кончике шпателя индикатор эриохром черный Т. Пробу титруют при интенсивном перемешивании 0,05М раствором ЭДТА до изменения окраски из розовой в голубую.
Общую жесткость воды Х в мг-экв/л определяют по формуле:

Где v– объем ЭДТА в мл пошедший на титрование;
V– объем воды, взятый для определения, мл.
2. Определение карбонатной жесткости воды.
В коническую колбу отбирают 100 мл исследуемой воды, добавляют 2-3 капли метилового оранжевого и титруют 0,1н раствором соляной кислоты до перехода желтой окраски в устойчивую оранжевую.
Карбонатную жесткость Х1 в мг-экв/л рассчитывают по формуле:

Где, v– объемHCl, израсходованный на титрование пробы, мл;
V– объем воды, взятый для определения, мл.
3. Определение остаточной жесткости воды.
Приготовление раствора 0,01н HCl: в мерную колбу на 50 мл пипеткой отбираю 5 мл 0,1нHCl, доводят до метки.
В коническую колбу отбирают 100 мл дистиллированной воды, добавляют 2-3 капли метилового оранжевого и титруют приготовленным 0,01н раствором соляной кислоты.
Остаточную жесткость Х2 мг-экв/л рассчитывают по формуле:

Где, v – объем 0,01н HCl, пошедший на титрование пробы, мл;
V – объем воды, взятый для определения, мл.
4. По разнице карбонатной и остаточной жесткости определяют устранимую жесткость Х3 мг-экв/л. По разнице общей и карбонатной жесткости определяют некарбонатную жесткость Х4 мг-экв/л.
5. Все результаты представляют в виде Х=(Хср ± ΔХ) мг-экв/л. Оформляют выводы по работе.
Статистическая обработка результатов.
Среднее значение вычисляют по формуле:

Затем рассчитывают стандартное отклонение от среднего:
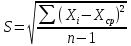
Для удобства расчетов S можно для каждой группы расчетов построить таблицу:
|
№ опыта |
Хi |
Xi - Xср |
(Xi - Xср)2 |
|
1 … |
|
|
|
|
∑ |
|
- |
|
Рассчитав S можно посчитать ΔХ – доверительный интервал:

Значения t – коэффициент Стьюдента приведены в таблице:
|
n |
Уровень доверительной вероятности | ||
|
0,90 |
0,95 |
0,99 | |
|
2 |
6,31 |
12,7 |
63,6 |
|
3 |
2,92 |
4,30 |
9,93 |
|
4 |
2,35 |
3,18 |
5,34 |
|
5 |
2,13 |
2,78 |
4,60 |
|
6 |
2,02 |
2,57 |
4,03 |
|
7 |
1,94 |
2,45 |
3,71 |
|
8 |
1,86 |
2,37 |
3,50 |
|
9 |
1,83 |
2,31 |
3,35 |
|
10 |
1,83 |
2,26 |
3,25 |
Рекомендуемая литература
