
Лабораторная работа №6
.docЛабораторная работа № 6. Модульная единица № 2.9
Определение удельной теплоёмкости твёрдого тела
Теоретическая часть
Теплоёмкостью называется способность тел накапливать тепловую энергию при их нагревании. Количество теплоты Q, необходимое для нагревания тела массы m от температуры t0 до t1, выражается соотношением
|
|
(1) |
где C – коэффициент пропорциональности, называемый удельной теплоёмкостью.
Удельной теплоёмкостью C называется количество теплоты, необходимое для нагревания единицы массы вещества на один градус; размерность C выражается в Дж/кг · град.
Мольной теплоёмкостью CM называется количество теплоты , необходимое для нагревания одного моля вещества на 1 градус. Если M – масса одного моля вещества, то справедливо соотношение CM = M · C [Дж/моль · град].
Процесс нагревания твёрдых тел отличается от нагревания газообразных веществ (см. работу 12) тем, что у них коэффициент объёмного расширения значительно меньше, поэтому затрачиваемая теплота идёт в основном на увеличение внутренней энергии тела, а совершение работы за счёт расширения пренебрежимо мало, следовательно в этом случае можно говорить просто о теплоёмкости твёрдого тела (аналогично CV для газов).
В отличие от газов в твёрдых телах атомы связаны упруго с положениями равновесия, которыми являются узлы кристаллической решётки. Поступательных и вращательных степеней свободы у атомов твёрдого тела нет. Внутренняя энергия твёрдых тел возрастает при нагревании за счёт возбуждения колебательных степеней свободы – колеблющиеся атомы в некотором приближении можно рассматривать как гармонические осцилляторы.
Согласно представлением классической статической физики на каждую колебательную степень свободы приходится в среднем энергия E = kT, а на каждую поступательную и вращательную степень свободы приходится в среднем кинетическая энергия, равная кТ/2.
Это обусловливается тем, что при колебаниях атома у него есть и кинетическая, и потенциальная энергии, причем их средние значения равны.
Так как каждый атом колеблется по трем осям х, у, z, то полная энергия колебаний одного атома будет равна
Ek = 3kT.
Внутреннюю энергию одного моля простого вещества находим, умножая число Авогадро NA = 6,02 · 1023 1/моль на Eк, тогда имеем ЕМ = ЕкNА = 3kTNA = 3RT, где R - универсальная газовая постоянная..
При изменении температуры нагреваемого тела на ΔT = T1 – T0 градусов приращение внутренней энергии равно ΔЕМ = 3RΔT, а мольная теплоёмкость
|
|
(2) |
Поскольку R ≈ 8,31 Дж/моль · К, то мольная теплоёмкость простых веществ равна 3R≈ 25 Дж/моль · К, что составляет правило Дюлонга–Пти.
Эксперимент показывает достаточно хорошее соответствие этого правила для многих веществ: для серебра и алюминия CM = 3,1R, для золота и железа CM = 3,22R. Поскольку в ионных решётках двухатомных соединений типа солей на один моль приходится 2NA атомов, то мольная теплоёмкость таких веществ равна CM = 2 CM. Например, для поваренной соли (NaCl) CM2 = 6,1R, что также хорошо согласуется с теорией.
Правило Дюлонга–Пти выполняется в том случае, когда теплоёмкость не зависит от температуры. Этот диапазон температур для многих веществ достаточно широк, но при очень низких температурах теплоёмкость уменьшается, а при весьма высоких – возрастает. Скачки величины теплоёмкости при увеличении температуры связаны с появлением новых степеней свободы, возбуждаемых при подводе энергии в процессе нагревания тел.
Общая постановка задачи:
Определить удельную теплоёмкость твёрдых тел калориметрическим методом, вычислить величины мольной теплоёмкости этих тел. Объяснить полученные результаты на основе молекулярно-кинетической теории.
Список индивидуальных данных:
1) нагреватель, 2) калориметр, 3) термометр, 4) мерная мензурка, 5) исследуемые тела, 6) инженерный калькулятор.
Пример выполнения работы
Один из методов определения теплоёмкости твёрдых тел основан на теплообмене исследуемого тела с веществом, теплоёмкость которого известна. Для этого удобно пользоваться жидкостью, удельная теплоёмкость которой в данном интервале температур постоянна и известна.
Если температура тела и жидкости различна, то при контакте между ними начинается теплообмен, и идёт до тех пор, пока температура системы «тело – жидкость» не выровняется. Уравнение теплового баланса очевидно:
Q1 = Q2,
где Q1 – тепло, отданное телом, и Q2 – тепло полученное жидкостью. Уравнение баланса справедливо в условиях изолированной системы.
Контролируемый теплообмен осуществляется с помощью калориметров, – в этом случае в уравнение теплового баланса нужно добавить члены, учитывающие вклад материала калориметра и сопутствующих принадлежностей.
Простейший калориметр состоит из (рисунок) металлического стакана 1, помещённого в другой 2 на теплоизолирующих пробках 3. Воздушный зазор 4 уменьшает теплообмен с внешней средой. В малый стакан наливают воду известного объёма 5, а для измерения температуры применяют термометр 6. Для лучшего теплообмена между водой и изучаемым телом 7 служит мешалка 8.
Уравнение теплового баланса запишем в виде
|
|
(3) |
где Q1 и Q2 (см. выше), а Q3 – количество теплоты, полученное корпусом калориметра и мешалкой, Q4<<Q3 – тепло, полученное термометром. С учётом уравнения (1) перепишем (3) в виде
|
|
(4) |
где m1 – масса исследуемого тела, C1 – его удельная теплоёмкость, t2 – температура тела в начале опыта, равная в данном случае температуре кипения воды, t1 – конечная температура системы «тело-калориметр», m2 – масса воды, m3 – масса деталей калориметра, С2 – удельная теплоёмкость воды, С3 – удельная теплоёмкость материала калориметра; С2 = 4,2 · 103, С3 = 3,8 · 102 Дж/кг · град; t0 – температура воды в начале опыта.
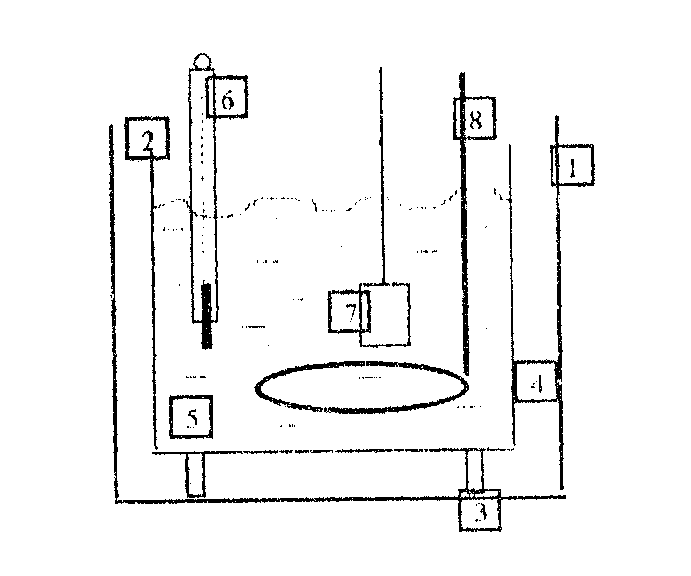
Рис. Схематическое изображение калориметра
Тогда искомая величина С1 равна
|
|
(5) |
где k = m2C2 +m3C3 – константа прибора
Определение удельной теплоёмкости твёрдых тел
1) Исследуемое тело опускают в нагреватель с кипящей водой и прогревают около 10 минут.
2) Мерной мензуркой отмеривают 300мл воды и вливают её в малый стакан калориметра; погрешность измерения ΔV = 0,5мл.
3) Измеряют температуру воды t0 термометром; погрешность измерения Δt1 = 0,5˚С. Будем считать t2 = 100ºC, Δt2 = 1ºC
4) Быстро вынимают исследуемое тело из нагревателя и переносят в калориметр. Постоянно перемешивая мешалкой воду, наблюдают за установлением температуры, и при достижении её постоянства снимают данные t1 и заносят в таблицу.
5) Вычисляют аппаратурный параметр k, согласно данным, написанным на стакане калориметра (масса) и величинам С2 и С3 (см. формулу (4)):
|
k = m2C2 + m3C3; m2 = 0,3 кг |
(6) |
6) Величину абсолютной погрешности Δk вычисляют по формуле
|
|
(7) |
считая Δm3 = 0,1г или Δm3 = 0,1 × 10-3 кг; Δm = 0,5 × 10-3 кг.
7) Определяют величину С1 по формуле (5)
8)величину относительной погрешности вычисляют по формуле
δс1 = √δк2+ δm12 + δ2t1+ δt22 (8)
где δк = Δk/k, δm1 = Δm1/m; Δm1 = 10-4 кг.
δt1 = Δt1/(t1 – t0), δt2 = Δt2/(t2 – t1) (9)
9) Абсолютную ошибку ΔС определения удельной теплоёмкости первого образца находят по формуле ΔС1 = δС1×С1. Все результаты записывают в таблицу.
10) Аналогичные операции и измерения проделывают со вторым образцом и результаты также вносят в таблицу.
11) Окончательный результат представляют в виде (удельная теплоёмкость)
|
С1±ΔC1 и С2±ΔC2, |
(10) |
а также пересчитывают по формуле СМi = Мi · Сi и выражают в виде (мольные теплоёмкости)
|
СM1±ΔCM1 и CM2±ΔCM2 . |
(11) |
12) Полученные данные сравнивают с теоретической величиной мольной теплоёмкости твёрдых тел СМ ≈ 25 Дж/моль · град и делают соответствующие выводы.
Определение теплоёмкости твёрдых тел
Таблица
|
№ |
t0, ˚С |
t1, ˚С |
t2, ˚С |
k |
Δk |
C, Дж/кг · град |
ΔC, Дж/кг · град |
М, кг/ моль |
См |
|
Металл 1 (Fe) |
|
|
|
|
|
|
|
|
|
|
Металл 2 (Al) |
|
|
|
|
|
|
|
|
|
Контрольные вопросы к защите
-
Какая физическая величина измеряется в данной работе и какова единица ее измерения?
-
Какому типу измерений относиться измерение температуры?
-
Оцените точность измерения температуры?
-
Что называется удельной и мольной теплоёмкостью?
-
Почему при изучении теплообмена используется колориметр?
-
Описать устройство калориметра, записать условие теплового баланса.
-
Между какими частями системы вода – калориметр – нагретое тело происходит теплообмен?
-
Что утверждает правило Дюлонга–Пти, раскрыть его физический смысл.
-
Как определяется мольная теплоёмкость для двухатомных кристаллических веществ?
-
Чем определяется погрешность окончательного результата при определении удельной теплоёмкости?
Способ оценки результатов
Полный ответ на каждый вопрос оценивается в один балл.

 ,
,