
- •Кафедра «Моделирование систем и информационные технологии»
- •Москва 2005
- •Введение
- •Электродные потенциалы
- •2. Гальванические элементы
- •3. Электролиз. Различие гальванического элемента и электролизера
- •4. Электролиз в водном растворе
- •5. Экспериментальная часть
- •5.1. Сравнение химической активности различных металлов
- •5.2. Гальванический элемент. Электролизер
- •Поместить в 2 пробирки по грануле металла
- •Литература
3. Электролиз. Различие гальванического элемента и электролизера
При прохождении электрического тока через металлы (проводники 1-го рода) они остаются неизменными, тогда как при прохождении электрического тока через расплавы или растворы электролитов (проводники 2-го рода) на электродах протекают процессы превращения одних веществ в другие.
При прохождении постоянного тока через расплав электролита катионы перемещаются к отрицательному электроду (катоду) и разряжаются на электроде, анионы перемещаются к положительному электроду (аноду) и разряжаются на электроде.
В результате электролит разлагается. Такой процесс называется электролизом.
Электролиз – разложение химического соединения под действием электрического тока, сопровождающееся разрядом ионов.
При электролизе протекают два параллельных полупроцесса: на катоде происходит прием электронов ионами, т.е. их восстановление, на аноде происходит отдача электронов ионами, т.е. их окисление.
Пример. В расплаве хлорида натрия при прохождении через него постоянного тока протекают следующие процессы. На катоде разряжаются ионыNa+, а на аноде разряжаются ионыCl-:
NaCl=Na++Cl-
на катоде Na++e-=Na0(восстановление)
на аноде Cl--e-=Cl0(окисление) 2Cl0 =Cl2(образование молекул)
Общее уравнение процесса, протекающего в расплаве NaClпод действием электрического тока:
электролиз
2NaCl-------2Na+Cl2
Электролиз – это окислительно-восстановительный процесс, при котором полупроцессы окисления и восстановления отделены друг от друга в пространстве. Полупроцессы при электролизе называются: анодным окислением и катодным восстановлением.
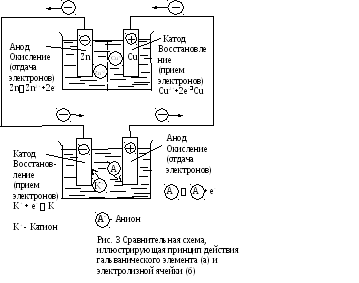
Принципиальное различие в действии гальванического элемента и электролизной ячейки (электролизера) заключается в том, что процессы, протекающие в них, имеют противоположные направления (рис. 3):
гальванический элемент – это источникэлектрического тока, а электролизер –потребительэлектрического тока;
в гальваническом элементе химическаяэнергия превращается вэлектрическую, в электролизере –электрическаяэнергия превращается вхимическую;
 в
замкнутой гальванической цепи
электрохимические процессы окисления
и восстановления протекают самопроизвольно,
в электролизере электрохимические
процессы окисления и восстановления
идут только под внешнимвоздействием
электрического тока;
в
замкнутой гальванической цепи
электрохимические процессы окисления
и восстановления протекают самопроизвольно,
в электролизере электрохимические
процессы окисления и восстановления
идут только под внешнимвоздействием
электрического тока;в гальваническом элементе отрицательный электрод – анод, аположительный электрод – катод;
в электролизере, наоборот, отрицательный электрод – катод, аположительный электрод – анод.
Обозначение «отрицательный» и «положительный» всегда относится к полюсам источника тока: применительно к электролизеру под положительным и отрицательным электродами также подразумеваются соответствующие полюса источника тока, к которым подключена ячейка.
Как в гальваническом элементе, так и в электролизере на отрицательном электроде создается избыток электронов, на положительном электроде – недостаток электронов.
Термины «катод» и «анод» связаны только с направлением потока электронов через электроды.
Катод – это электрод, через который поток электронов входит в гальванический элемент или электролизер и на котором реагирующие частицы восстанавливаются из-за наличия избытка электронов.
Анод - это электрод, через который поток электронов выходит из гальванического элемента или электролизера и на котором реагирующие частицы окисляются вследствие недостатка электронов.
В электролизной ячейке на отрицательном электроде – катодепротекаетвосстановление, а на положительном электроде –аноде – окисление, например:
Na+ + e- = Na0; 2Cl- - 2e- = Cl2.
В гальваническом элементе на положительном электроде – катодепротекаетвосстановление, а на отрицательном электроде –аноде–окисление, например:
Cu2+ + 2e- = Cu 0; Zn - 2e- = Zn2+.
