
- •1.Классификация и номенклатура органических соединений
- •2)Реакции окисления
- •3)Реакция восстановлениия
- •7.1) Качаственная реакция!!!концевая 3-ая связь
- •6.Галогенпроизводные ув
- •8.Заместители бензольного кольца и их влияние на направление и скорость реакции Se:
- •9.Кислородсодержащие соединения. Спирты
- •9.1Ненасыщенные спирты:
- •10.Многоатомные спирты: гликоли
- •11.Ароматические спирты и фенолы
- •12 Альдегиды и кетоны
- •13.Карбоновые кислоты.
- •14.Углеводы
- •Моносахариды
- •15.Нитросоединения
- •Способы получения нитросоединений
- •Химические свойства
- •16. Основные химические свойства аминов.
8.Заместители бензольного кольца и их влияние на направление и скорость реакции Se:

Заместители I рода орто- и пара-ориентанты, т. е. в SE-реакции образуются преимущественно два изомера, соответствующие орто- и пара-замещению.

Заместители II рода мета-ориентанты, т. е. в SE-реакции образуется преимущественно один изомер, соответствующий мета-замещению. Это электроноакцепторные (ЭА) заместители, снижающие скорость SE-реакции по сравнению с незамещенным бензолом.

Ориентация у дизамещенного бензола. При наличии двух заместителей в бензольном кольце возможны их согласованная и несогласованная ориентации.
Согласованная ориентация заместителей оба заместителя направляют вновь вступающую группу в одни и те же положения бензольного кольца


Несогласованная ориентация заместителей оба заместителя направляют вновь вступающую группу в разные положения бензольного кольца.

А Б
В этом случае руководствуются следующим принципом: место вступления электрофила определяет заместитель I рода (случай А) или заместитель, который является лучшим донором (случай Б).
9.Кислородсодержащие соединения. Спирты
Гидроксилсодержащие соединения (группа ОН)
К ним относятся: спирты и фенолы.
Классификация спиртов:
Жирноароматические: (ароматическое кольцо с алифатической цепью)
-первичные, -втроричные,-третичные
-одноатомные
-двухатомные
-трехатомные
-многоатомные
Получение спиртов:
Реакции гидролиза галогенопроизводных УВ.
СН3-СН(Cl)-СН2-СН3+ NaOH→CH2-CH(OH)-CH2-CH3+NaCl
Гидротация алкенов(+Н2О)
СH3-С(СH3)=СH-СH3
+ НОН СH3-(OH)С(СH3)-СH2-СH3
СH3-(OH)С(СH3)-СH2-СH3
Гидролиз сложных эфиров карбоновых кислот
R-C(=O)-OR1
 R1-OH+R-C(=O)-ONa
R1-OH+R-C(=O)-ONa
Восстановление альдегидов и кетонов:
А)
CH3-CH2-(H-)C(=O)
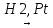 CH3-CH2-CH2-OH(первичн.спирт
CH3-CH2-CH2-OH(первичн.спирт
Б)
CH3-CH2(=О)-СН3 CH3-CH2(OH)-CH3вторичн.спирт.
CH3-CH2(OH)-CH3вторичн.спирт.
Окисление алкенов по Вагнеру, получение 2-мных спиртов.
CH3-C(CH3)=CH2+
KMnO4
CH3-(OH)C(CH3)-(OH)CH2+ MnO2↓
Физические свойства:
1)С1-С11 -жидкости 2)С12-и выше – тв.в-ва, Tкип. Выше, чем у алканов.
Высокие т кипения можно объяснить образованием между молекул водородных связей. Низшие спирты хорошо растворимы.
Химические свойства:
СН3-СН2-О←Н ↔ СН3-СН2-Оδ- + Нδ+
Разорвать связь ОН могут только щелочные и щелочноземельные Ме: Li,Na,K, Mg,Ca
Кислотность спиртов:
СН3-СН2-ОН
 СН3-СН2-ОNa
пропанолят Na
+ Н2
СН3-СН2-ОNa
пропанолят Na
+ Н2

Реакция нуклефильного замещения гидроксильной группы.
в качестве нуклеофилов выступают:
-галогеноводородные к-ты: HBr, HCl, HI
-галогениды фосфора: PCl3, PBr3, PCl5, PBr5
-спирты : R-OH
А) нуклефильного замещения галогеноводородами:
СH3-CH2-CH2→OH+HBr
 CH3-CH2-CH2→Br
CH3-CH2-CH2→Br
Б) нуклефильного замещения галогениды фосфора:
CH3-CH(OH)-CH2-CH3

CH3-CH(Cl)-CH2-CH3


В) нуклефильного замещения спиртами, с образование простых эфиров.
Катализаторы: H2SO4, H3PO4, Al2O3, P2O5
СH3-CH2-CH2-OH+HO-CH2-CH2-CH3
CH2-CH2-CH2-O-CH2-CH2-CH3 (дипропиловый эфир)
Внутримолекулярная дегидротаций(образуется алкен)
CH3-(OH→)C(CH3)-CH2-CH3

CH3-(CH3)C=CH-CH3
Окисление спиртов до альдекидов и кетонов:
А)CH3-CH2-CH2-OH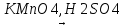 пропаналь
пропаналь
 CH3-CH2-COOH
CH3-CH2-COOH
Б)
CH3-CH2(OH)-CH3 CH3-CH2(=О)-СН3
пропанон
CH3-CH2(=О)-СН3
пропанон
Дегидрирование спиртов:
Первичные – альдегид, вторичные – кетон
А)
CH3-CH2-CH2-OH
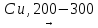 CH3-CH2-(H-)C(=O)
CH3-CH2-(H-)C(=O)
Б)тоже самое
Этерификация спиртов с органич, неорганич. кислотами –
образование сложных к-т.
R-C(=O)-OH+ R1OH ↔ R-C(=O)-O-R1 сложный эфир + H2O

Основные св-ва характеризуются способностью присоединять Н+
CH3-CH2-CH2-OH
 [CH3-CH2-CH2-OH2]HSO4
[CH3-CH2-CH2-OH2]HSO4
Представители:
СН3ОН – метанол, яд
С2Н5ОН – этанол, консервант анатомических препаратов.
