
- •Основы термодинамики процессов и циклов современных двигателей
- •5.2.Уравнения законов термодинамики
- •5.3.Энтропия
- •Уравнения для определения энтропии и её изменения
- •5.4. Термодинамические процессы
- •5.Термодинамические процессы изменения состояния идеального газа:
- •Изохорический процесс
- •Адиабитический процесс
- •Термодинамические характеристики адиабатного процесса
- •Политропический процесс
- •Термодинамические характеристики политропического процесса
- •Термодинамические процессфы в диаграммах p-V, t-s
- •5.5. Цикл карно
- •Круговые процессы
- •Обобщённый цикл Карно(оцк)
- •5.6. Эксергия
5.4. Термодинамические процессы
5.Термодинамические процессы изменения состояния идеального газа:
1. ИЗОХОРИЧЕСКИЙ
2. ИЗОБАРИЧЕСКИЙ
3. ИЗОТЕРМИЧЕСКИЙ
4. АДИАБАТИЧЕСКИЙ (ИЗОЭНТРОПИЧЕСКИ)
5. ПОЛИТРОПИЧЕСКИЙ
Все указанные процессы рассматриваются как обратимые и исследуются в соответствии с общим методом, включающим определение:
А.Графической зависимости процесса в p-v и T-s – координатах.
Б. Соотношения между основными параметрами состояния рабочего тела(идеального газа) в начале и конце термодинамического процесса.
В. Изменения
внутренней энергии: ∆u
= u2
– u1
=
![]() cvdT
= cv(t2
– t1).
cvdT
= cv(t2
– t1).
Г. Работы при
изменении объёма газа: l
=![]() pdv
pdv
Д. Удельного
количества теплоты: q1-2
=
![]() cxdT
= cx(t2
– t1)
cxdT
= cx(t2
– t1)
Е. Изменения
удельной энтальпии:
∆i
= i2
– i1
=
![]() cpdT
= cp(t2
– t1).
cpdT
= cp(t2
– t1).
Ж. Изменения удельной энтропии: s2 – s1 = cvln(T2/T1) + Rln(v2/v1);
s2 – s1 = cрln(T2/T1) – Rln(p2/p1);
Изохорический процесс
T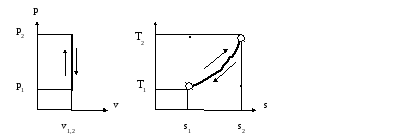
А. Уравнение процесса: v = const или dv = 0
Б. Соотношение параметров:
Для процесса 1-2 уравнение состояния в точках 1 и 2: p1v1,2 = RT1, p2v1,2 = RT2. Разделив первое уравнение на второе, получим закон Шарля p1/p2 = T1/T2.
В. Изменение внутренней энергии в соответствии с первым законом:
dqv
= duv
+ pdv
= duv
= cvdT,
откуда qv
=
![]() cvdT
= cv(T2
– T1)
= u2
– u1
cvdT
= cv(T2
– T1)
= u2
– u1
Г. Работа изменения объёма: lv = 0.
Д. Удельное
количество теплоты: uv
=
![]() cvdT
= cv(T2
– T1)
= u2
– u1.
cvdT
= cv(T2
– T1)
= u2
– u1.
Е. Изменение удельной энтальпии:
Ж. Изменение удельной энтропии:di = dq + vdp = dq = cpT2 – T1)
dqv = duv + pdv; dqv/T = (duv + pdv)/T = cvdT/T + pdv/T.
С учётом уравнений состояния: pv = RT и энтропии ds = dq/T получим
ds = cvdT/T + Rdv/v, откуда после интегрирования получим
∆s = s2 – s1 = cvln(T2/T1) + Rln(v2/v1) = cvln(T2/T1);
Адиабитический процесс
pvk = const
dq = du + dl = 0; du = - dl; dl = - du = u1 – u2;
l1,2 = cv(T2 – T1)
pv = RT; pdv + vdp = RdT; dT = (pdv + vdp)/R – в уравнение cvdT + pdv = 0(du + dl = 0), получим
cv(pdv + vdp)/R + pdv = 0 или (cv + R) pdv + cvvdp = 0, где cv + R = cp
Тогда cppdv + cvvdp = 0;
kpdv + vdp = 0,
kdv/v + dp/p = o,
где k = cp/cv
После интегрирования получим klnv + lnp = const или
pvk = const
Исключив из 2 р = RT/v, получим RTvk-1 = const или
Tvk-1 = const
Исключив из 2 v = RT/p, получим p(RT/p)k = const или
T/p (k-1)/k = const
Из 2, 3, 4 после их преобразований: p1v1k = p2v2k;
T1v1k = T2v2k; T1/p1 (k-1)/k = T2/p2 (k-1)/k получаем:
p1/p2 = (v2/v1)k-1
T1/T2 = (v2/v1)k-1
T1/T2 = (p1/p2)(k-1)/k
Для адиабатического процесса после деления уравнения Майера cp – cv = R на cv имеем
cp /cv -1 = R/cv или cv = R/(k-1).
После деления уравнения Майера cp – cv = R на cp имеем
(1 – 1/k) = R/cp или cp = kR/(k-1)
Термодинамические характеристики адиабатного процесса
Теплоёмкость:
с = 0
Удельная работа:
l1-2 = (p2v2 – p1v1)/(k-1) = p2v2/(k-1)(1 – (p1/ p2)(k-1)/k) =
R(T2 – T1)/(k-1)
Теплота:
q = 0
Изменение:
∆u = cv(T1 – T2)
∆i = cp(T1 – T2)
∆s = 0
Политропический процесс
pvn = const
1. dq = cdT = di – vdp = cpdT – vdp;
2. dq = cdT = du + pdv = cvdT + pdv;
Преобразовав и разделив 1 на 2, получим (c - cp)/ (c – cv) = - (vdp/pdv);
Принимая n = (c - cp)/(c – cv), получим n = - (vdp/pdv), откуда npdv = - vdp или n(dv/v) + dp/p = 0,
nlnv + lnp = 0
После интегрирования получаем ln(pvn) = const или
pvn = const.
Из n = (c - cp)/(c – cv) получаем n(c – cv) = c - cp,
с(n – 1) = cv(n – (cp/ cv)) = cv(n – k), откуда c = cv(n – k)/ (n – 1)
Соотношения между параметрами:
p1/p2 = (v2/v1)n
T1/T2 = (v2/v1)n
T1/T2 = (p1/p2)n-1
