
- •С.А. Сергеева, в.Е. Рябинин Практикум по химии
- •Рекомендовано
- •Оглавление
- •Введение
- •Тема: Тепловые эффекты химических реакций. Термодинамические характеристики химических и биохимических процессов
- •1. Практическая часть
- •1.3. Контрольные вопросы
- •2. Экспериментальная часть Лабораторная работа. Определение стандартной теплоты (энтальпии) реакции нейтрализации
- •Экспериментальные данные и результаты измерений
- •4. Вопросы по теме для самостоятельного изучения их студентами.
- •Тема: Кинетика химических и биохимических реакций. Химическое равновесие
- •1. Основные понятия химической кинетики:
- •1. Практическая часть
- •1.3. Контрольные вопросы
- •2. Экспериментальная часть
- •Зависимость скорости разложения от ее концентрации //
- •4. Вопросы по теме для самостоятельного изучения их студентами.
- •Приложения а
- •Значения теплоты сгорания некоторых органических веществ, применяемых в медицине
- •Список литературы Основная литература
- •Дополнительная литература
1. Практическая часть
1.1.Ситуационные задачи (№№ с 1 по 7)с алгоритмами их решений, эталонами ответов и с комментариями.
Вычисление значение внутренней энергии, теплоты и работы
Задача №1.Рассчитайте значение работы, проделанной реакцией открытия мышьяка в биологическом материале (слюне):
![]()
Решение.
В этой реакции на 1 моль
 выделяется
I
моль газообразного
выделяется
I
моль газообразного
 .
Газ оттесняет окружающую атмосферу и
производит работу, равную
.
Газ оттесняет окружающую атмосферу и
производит работу, равную
 .
Рассматривая этот газ как идеальный и
пренебрегая объемом исходных веществ,
можно
.
Рассматривая этот газ как идеальный и
пренебрегая объемом исходных веществ,
можно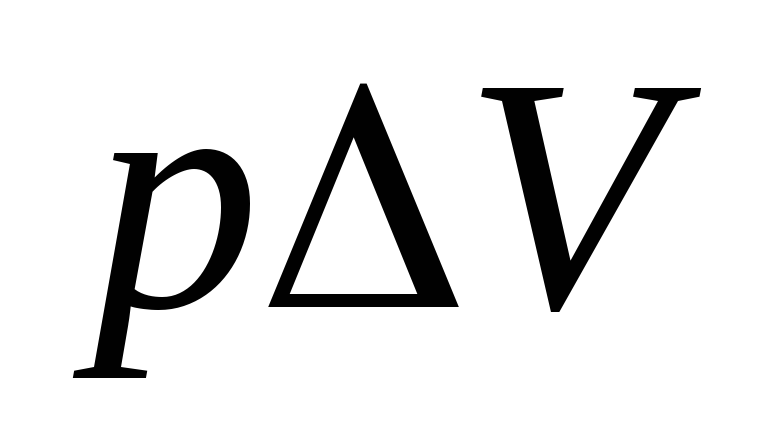 приравнять
приравнять ,
a
,
a
 =
= .
.Если прореагировал 1 моль
 ,
то работа, произведенная реакцией:
,
то работа, произведенная реакцией:
 =1
моль
=1
моль
 К=
2496,4 Дж или2,5 кДж.
К=
2496,4 Дж или2,5 кДж.Если реакцию проводят в плотно закрытой колбе, то W=0, так как объем не может увеличиваться. Работа производится только в том случае, когда изменяется объем системы.
Ответ.
![]() =
2496,4 Дж или 2,5 кДж.
=
2496,4 Дж или 2,5 кДж.
Задача
№2. Чему
равно изменение внутренней энергии
![]() при
испарении воды массой 100 г при 20°С, если
принять, что водяной пар подчиняется
законам идеальных газов, а объемом
жидкости, который незначителен по
сравнению с объемом пара, можно пренебречь.
Удельная теплота парообразования воды
при
испарении воды массой 100 г при 20°С, если
принять, что водяной пар подчиняется
законам идеальных газов, а объемом
жидкости, который незначителен по
сравнению с объемом пара, можно пренебречь.
Удельная теплота парообразования воды
![]() Дж/г.
Дж/г.
Решение.
Из формулы расчета внутренней энергии:
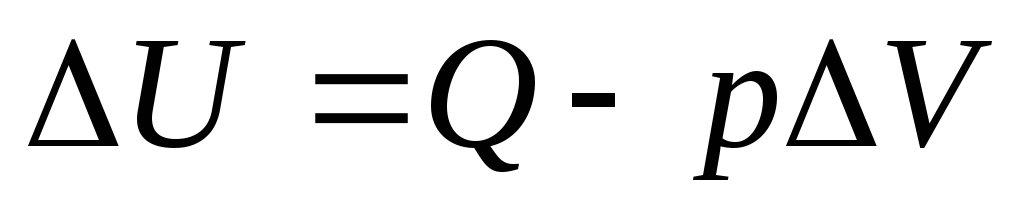 и с учетом того, что
и с учетом того, что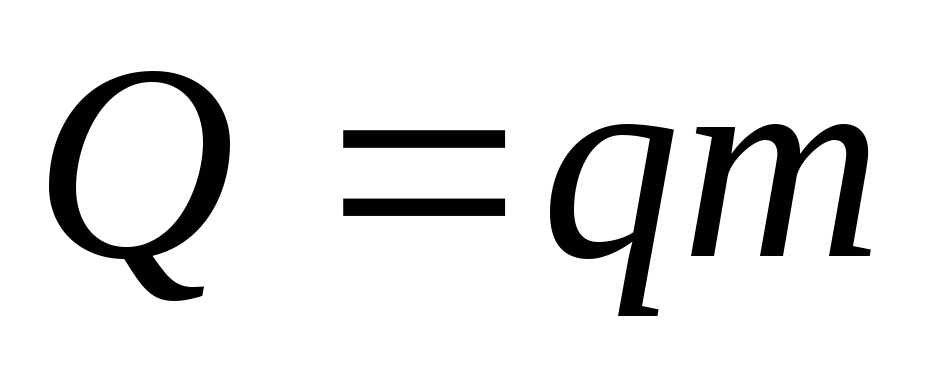 и
и ,
получаем:
,
получаем: кДж.
кДж.
Ответ. Внутренняя энергия увеличилась на 230,97 кДж.
Вычисление значение теплового эффекта и определение теплоты образования и сгорания
Задача
№3. Определите
тепловой
эффект
реакции образования воды:
![]() при постоянном давлении и температуре
298 К, если тепловой эффект при постоянном
объеме равен -284,2 кДж/моль.
при постоянном давлении и температуре
298 К, если тепловой эффект при постоянном
объеме равен -284,2 кДж/моль.
Решение.
В химических реакциях изменение числа молей равно разности стехиометрических коэффициентов /
 /
в уравнении, поэтому
/
в уравнении, поэтому ,
то
,
то =
= .Примечание!
Если в реакции участвуют твердые и
жидкие вещества, то при вычислении
.Примечание!
Если в реакции участвуют твердые и
жидкие вещества, то при вычислении
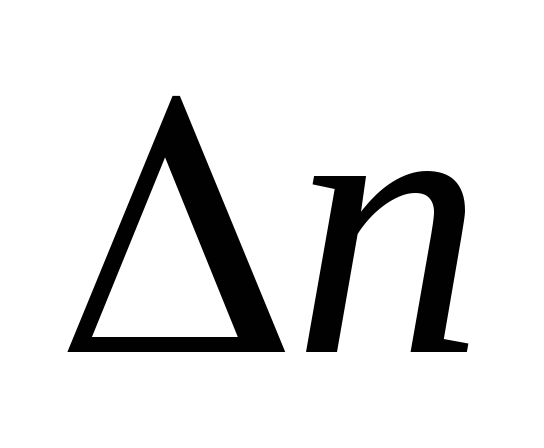 они во внимание не принимаются.
они во внимание не принимаются.Отсюда согласно формуле:
 =
=
 Дж/моль или 291,6 кДж/моль.
Дж/моль или 291,6 кДж/моль.
Ответ.
![]()
![]() Дж/моль или 291,6 кДж/моль.
Дж/моль или 291,6 кДж/моль.
Задача
№4. Определите
теплоту образования
![]() по реакции:
по реакции:![]()
![]()
Решение.
В основе термохимических расчетов лежит следствие из закона Гесса:
 .
Согласно данному уравнению, тепловой
эффект данной реакции является теплотой
образования
.
Согласно данному уравнению, тепловой
эффект данной реакции является теплотой
образования .
.Так как

 и
и равны
нулю, а
равны
нулю, а кДж/моль (табличные данные), то,
следовательно,
кДж/моль (табличные данные), то,
следовательно, кДж/моль.
кДж/моль.
Ответ.![]() кДж/моль.
кДж/моль.
Задача
№5. Рассчитайте стандартный тепловой
эффект реакции:![]() постандартным теплотам
сгорания.
постандартным теплотам
сгорания.
Решение.
В основе термохимических расчетов лежит следствие из закона Гесса:
 Тогда:
Тогда:
Из таблиц находят
 для каждого из участников реакции (в
кДж/моль):
для каждого из участников реакции (в
кДж/моль):
![]() =-802,32;
=-802,32;![]()
![]()
![]()
Подставляя данные, получим:
 кДж/моль (реакция эндотермическая).
кДж/моль (реакция эндотермическая).
Ответ.![]() кДж/моль.
кДж/моль.
Вычисление изменения стандартной энтропии и энергии Гиббса
Задача
№6.Предскажите
знак изменения энтропии /![]() /
в каждой из ниже предполагаемых реакций
и проверьте правильность сделанных
выводов расчетом
/
в каждой из ниже предполагаемых реакций
и проверьте правильность сделанных
выводов расчетом![]() соответствующих реакций, пользуясь
справочными данными.
соответствующих реакций, пользуясь
справочными данными.
|
|
Реакции |
Выводы |
|
1. |
|
|
|
2. |
|
|
|
3. |
|
|
|
4. |
|
Вероятно,
|
|
5 |
|
|
Решение.
Выпишем из таблицы (см. приложение) значения
 соответствующих
веществ и подпишем их под формулами в
уравнениях 1- 5 и для данных реакции
вычисляем
соответствующих
веществ и подпишем их под формулами в
уравнениях 1- 5 и для данных реакции
вычисляем
 по формуле:
по формуле: .
.
1)![]()
![]()
![]() .
.
2)
![]()
![]() =
=![]() .
.
3)
![]()
![]()
![]()
![]() =
=![]() .
.
4)
![]()
![]()
![]() =
=![]() .
.
5)
![]()
![]()
![]() =
=![]() .
.
Ответ.
Таким
образом,
результаты вычисления
![]() реакций подтвердили выводы, сделанные
ранее, т.е.:
реакций подтвердили выводы, сделанные
ранее, т.е.:
1)![]() =
=![]() ,т.е.
,т.е.![]() >0;
>0;
2)![]() =
=![]() ,
т.е.
,
т.е.![]() <0;
<0;
3)![]() =
=![]() ,т.е.
,т.е.![]() <0;
<0;
4)
![]() =
=![]() ,
т.е.
,
т.е.![]() >0;
>0;
5)![]() =
=![]() ,
т.е.
,
т.е.![]() <0.
<0.
Задача №7. Какие из реакций, перечисленных в задаче №6, протекают самопроизвольно при стандартных условиях?
Решение.
По выше найденным данным вычисляем изменения изобарно-изотермического потенциала или свободной энергии Гиббса /
 /:
/:
Из таблицы выпишем
 образования соединений и
подставляем эти данные
для выше соответствующих реакций:
образования соединений и
подставляем эти данные
для выше соответствующих реакций:
1)
![]()
![]() кДж.
кДж.
2)
![]()
![]() кДж.
кДж.
3)
![]()
![]() кДж.
кДж.
4)
![]()
![]() кДж.
кДж.
5)
![]()
![]() кДж.
кДж.
Ответ. Полученные результаты говорят о том, что реакции 1, 3 и 5 могут протекать в стандартных условиях самопроизвольно до установления равновесия, а реакции 2 и 4 в этих условиях протекать в указанном направлении не могут.
1.2. Ситуационные задачи №№ с 8 по 19 для закрепления материала (выполнить в протокольной тетради).
Задача
№ 8. Рассчитайте
изменение внутренней энергии при
испарении 20 г спирта при температуре
его кипения, если удельная теплота
парообразования спирта 858,95 Дж/г, а
удельный объем пара 607
![]() (объем жидкости пренебречь).
(объем жидкости пренебречь).
Задача
№9. Определите
работу изотермического обратимого
расширения 3 моль водяного пара от
![]() до
до![]() Па
при стерилизации ампул с раствором
глюкозыпри
330
К.
Па
при стерилизации ампул с раствором
глюкозыпри
330
К.
Задача № 10. Какая масса ядер грецких орехов может компенсировать половину суточной потребности человека в энергии, равной 6276 кДж, если известно, что в орехах массовая доля жира 64,4%, белка 15.6% и углеводов 12%?
Задача №11. Какое количество работы совершает человек весом 75 кг, взбираясь на памятник Вашингтону высотой 555 футов (1 фут=0,3048 м)? Сколько килокалорий необходимо для этого получить с пищей, если принять, что в механическую работу мышц может быть превращено 25% энергии, выделяющейся при окислении пищи в организме?
Задача №12. Энтальпия сгорания углеводов в организме человека составляет -17,55 кДж/г, белков – 16,72 кДж/г, жиров – 39,29 кДж/г. Среднесуточная потребность в белках, жирах и углеводах для студентов – мужчин составляет соответственно 113 г, 106 г, 451 г, для студентов – женщин 96 г, 90 г, 383 г. Какова среднесуточная потребность студентов в энергии?
Задача №13. Используя значение энтальпий сгорания белков, жиров и углеводов (см. задачу №12) рассчитать энергетическую ценность перловой каши (67 г крупы). В 100 г крупы содержится 9,3 г белков, 1,1 г жиров и 73,7 г углеводов.
Задача
№14.Вычислите
стандартную энтальпию биохимического
брожения глюкозы:
![]() ,
если стандартные энтальпии сгорания
глюкозы и этилового спирта равны
соответственно -2801,69 и -1366,6 кДж/моль.
Определить знак
,
если стандартные энтальпии сгорания
глюкозы и этилового спирта равны
соответственно -2801,69 и -1366,6 кДж/моль.
Определить знак![]() .
.
Задача №15. Рассчитайте тепловой эффект реакции получения этилового эфира аминобензойной кислоты (полупродукта при получении анестезина) при стандартных условиях по уравнению реакции:
![]() если
известны стандартные теплоты образования
участников реакции:
если
известны стандартные теплоты образования
участников реакции:![]()
-
Вещество
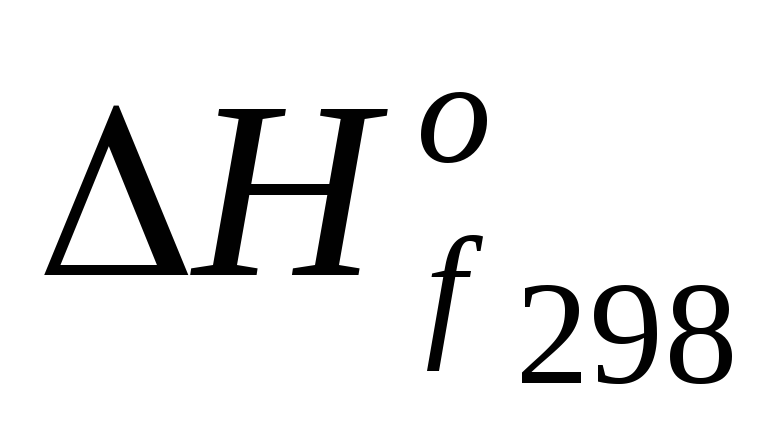 ,
кДж/моль
,
кДж/моль
-463,2

-273,2

-1759,0

-1068,0
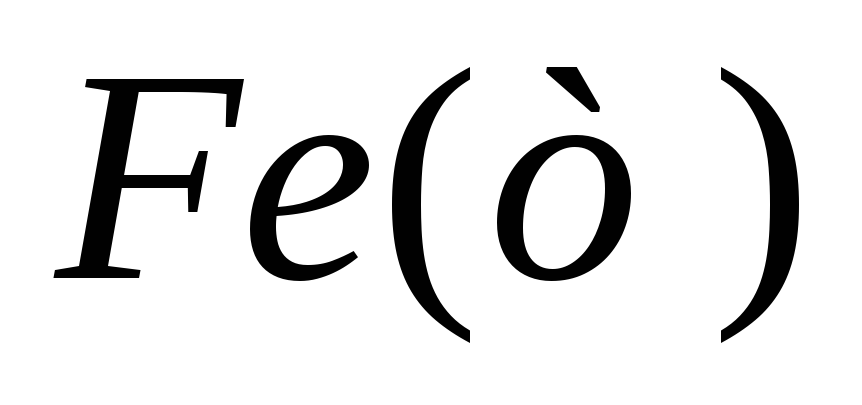
0
Задача
№16.
Рассчитайте тепловой эффект реакции
получения
газообразного диэтиламиноэтанола
(полупродукта при синтезе новокаина)
при
стандартных условиях
по реакции:![]() если
известны стандартные теплоты образования
участников реакции:
если
известны стандартные теплоты образования
участников реакции:
-
Вещество
 ,
кДж/моль
,
кДж/моль
-81,6

-48,8

-341,0
Задача
№17. Возможно
ли в стандартных условиях реакция:
![]() Рассчитайте
Рассчитайте![]() ,
,![]() ,
,![]() для
данной реакции.
для
данной реакции.
Задача
№18. Возможно
ли осуществление процесса восстановления
металлического железа из оксида
![]() действием водорода при стандартных
условиях:
действием водорода при стандартных
условиях:![]()
Задача № 19. Как влияет температура на направление реакций 1-5 (см. задачу №6)?
