
- •Государственное образовательное учреждение высшего профессионального образования
- •Введение
- •1. Краткие теоретические сведения
- •2. Указания по технике выполнения лабораторных работ
- •3. Лабораторный практикум Лабораторная работа №1. Действие групповых реагентов
- •Лабораторная работа №2. Качественные аналитические реакции катионов
- •Первая аналитическая группа катионов
- •Вторая аналитическая группа катионов
- •Третья аналитическая группа катионов
- •Четвертая аналитическая группа катионов
- •Пятая аналитическая группа катионов
- •Шестая аналитическая группа катионов
- •Лабораторная работа №3. Разделение ионов по аналитическим группам и внутри группы.
- •Катионы I и II аналитических групп.
- •Катионы III и IV аналитических групп.
- •Катионы V и VI аналитических групп
- •Лабораторная работа № 4. Анализ смеси катионовIиIIаналитических групп
- •Лабораторная работа № 5. Анализ смеси катионов третьей и четвертой аналитических групп
- •Лабораторная работа №6. Анализ смеси катионов пятой и шестой аналитических групп
- •Лабораторная работа №7. Анализ смеси катионов всех шести аналитических групп
- •4. Практические задания
- •Литература
- •Содержание
Лабораторная работа №2. Качественные аналитические реакции катионов
Оборудование и реактивы.В штативе: хлорид натрия, хлорид калия, хлорид аммония, дигидроантимонат натрия, нитрат свинца (II), йодид калия, хромат калия, сульфат натрия, сульфат цинка, хлорид бария, хлорид кальция, сульфат хрома (III), сульфат алюминия, сульфат цинка, ацетат натрия, сульфат магния, гидроортофосфат натрия, гидроксид аммония, сульфат марганца (II), хлорид железа (III), роданид (тиоцианат) калия, сульфат меди (II), сульфат кобальта (II), сульфат никеля (II), сульфат кадмия (II), гидроксид натрия, гидроксид калия – 5% растворы.В лаборатории: держатель для пробирок, воронка, фильтры.В вытяжном шкафу: соляная кислота, азотная кислота, серная кислота, уксусная кислота – 2 н. растворы, гидроксид калия, гидроксид натрия – 6 н. растворы, гидроксид аммония – концентрированный раствор, сульфид натрия – 5 % раствор, бромная вода.Получать в лаборантской: гексанитрокобальтат натрия, реактив Несслера, нитрат серебра, нитрат ртути (I), нитрат ртути (II) – 1 % растворы, ацетон, гексацианоферрат (II) калия, гексацианоферрат (III) калия, тетрароданомеркурат (II) аммония – 5 % растворы, спирт амиловый (изоамиловый), алюминон – 1% раствор, висмутат натрия, крист., хлорид аммония, крист., диметилглиоксим – 1 % спиртовой раствор, перекись водорода, индикаторная бумага, пробирки, стеклянные палочки.
Первая аналитическая группа катионов
1. Катион
![]() в водных растворах
бесцветен.
в водных растворах
бесцветен.
Определяется по обменной реакции с дигидроантимонатом калия KH2SbO4, образующим с водным раствором соли натрия в нейтральной среде (pH~7) белый кристаллический осадок дигидроантимоната натрия:
![]() .
.
Примечание: при рН < 7 выпадает белый аморфный осадок сурьмяной кислотыH3SbO4!
Ход анализа. В пробирку внести 2-3 капли раствора соли натрия и прибавить равный объем реактива. Для улучшения выпадения осадка можно потереть внутренние стенки пробирки стеклянной палочкой, охладить реакционную смесь.
2. Катион
![]() в водных растворах
бесцветен.
в водных растворах
бесцветен.
Определяется по реакции с гексанитрокобальтатом (III) натрия Na3[Co(NO2)6], образующим с водным раствором соли калия в слабокислой среде (рН=4-6) желтый осадок двойной комплексной солигексанитрокобальтата (III) натрия-калия:
![]() .
.
Ход анализа. В пробирку внести 2-3 капли соли калия и прибавить значительный избыток раствора реагента, энергично перемешать.
3. Катион
![]() в водных растворах
бесцветен.
в водных растворах
бесцветен.
Реактив Несслера, который является
щелочным раствором тетраиодомеркурата (II) калияK2[HgI4],
образует с растворами аммонийных солей
бурый осадок иодида основания Миллона,
имеющего химическую формулу [Hg2N]I∙H2O.
Это соединение можно рассматривать как
продукт замещения иодом гидроксильной
группы в гидратированном основании
Милона [HgI4]OH∙H2O.
Основание Миллона содержит катион
[Hg2N]+,
который можно рассматривать как ион![]() ,
в котором четыре атома водорода замещены
двумя атомами ртути.
,
в котором четыре атома водорода замещены
двумя атомами ртути.
Аналитическая реакция протекает по следующему уравнению:
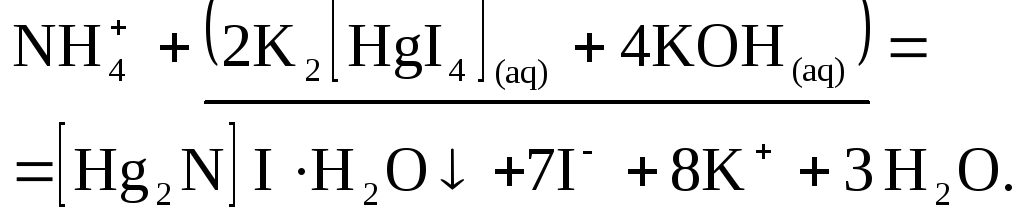
Ход анализа. К 2-3 каплям раствора соли аммония добавить 4-6 капель (избыток) реактива Несслера (2 K2[HgI4](aq)+4 KOH).
При малых количествах иона аммония («следы») осадок приобретает желтое окрашивание.
