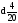2 Синтез заданного органического соединения
2.1 Основные реакции синтеза:
а) Диазотирование

б) Азосочетание

2.2 Свойства синтезируемого вещества по литературным данным:
молекулярная масса – 350 г/моль
2.3 Таблица - Свойства основных исходных соединений
|
Формула |
Молекулярная масса, г/моль |
tпл. С |
tкип С |
|
|
Растворимость | |
|
в воде |
в органических растворителях | ||||||
|
NH2C6H4SO2OH |
173,2 |
288 |
разл. |
1,4850 |
1,4850 |
6,7 |
М.р.,Эт,Раф |
|
NaNО2 |
68,99 |
271 |
разл. |
2,17 |
100 |
82,9 |
жид.NH2,Эт,Хлф |
|
C10H7OH |
144,17 |
23 |
286 |
1,2800 |
- |
0,074 |
Эт,Эф,Хлф,Р |
3 Расчет количеств исходных веществ, необходимых для синтеза
3.1 Расчет основных исходных веществ
Уравнения реакций получения 2-нафтолоранжевого красителя приведены выше. В соответствии с методическими указаниями в синтезе используется:
Сульфаниловая кислота 4,3 г
Азотистокислый натрий 2,1 г
2- нафтол 3,6 г
а)Исходя из этого, находим мольное соотношение реагирующих веществ.
Сульфаниловая кислота:
n=m/Mr=4,3г/173,2г/моль=0,0248 моль
Азотистокислый натрий:
n=m/Mr=2,1г/68,99г/моль=0,0304 моль
2- нафтол:
n=m/Mr=3,6г/144,17г/моль=0,0250 моль
б)Приводим к единице молей основное исходное вещество, по которому ведется расчет:
NH2C6H4SO2OH:NaNО2:C6H7OH=0,0248:0,0304:0,0250=1:1,2258:1,0081
в)Сохраняя это мольное соотношение, находим количества реагирующих веществ по основному веществу:
Сульфаниловая кислота
n1=m/Mr=4,5г/173,2г/моль=0,026 моль
m1=4,5г
Азотистокислый натрий:
n2=1,2258×n1=1,2258 ×0,026 моль=0,0319 моль
m2= Mr×n2=68,99 г/моль×0,0319 моль=2,2 г
2- нафтол:
n3=1,0081×n1=1,0081 г/моль×0,026 моль=0,0262 моль
m3= Mr×n2=144,17 г/моль×0,0319моль=4,6г
3.2 Расчет вспомогательных веществ
Рассчитываем количество вспомогательных веществ по пропорции, исходя из заданного количества исходного в-ва.
Из условия методики данного синтеза известно, что:
для 4,3 г сульфаниловой кислоты необходимо 12,5 см3 едкого натра,
а для 4,5 г––––– Х см3, тогда
V(NaOH) = (4,5х12,5)/4,3 = 13,08 см3
для 4,3 г сульфаниловой кислоты необходимо 12,5 см3 HCl,
а для 4,5 г––––– Х см3,тогда
V(HCl)= (4,5х12,5)/4,3 = 13,08 см3
для 4,3 г сульфаниловой кислоты необходимо 2 г NaOH(порошок),
а для 4,5 г––––– Х г,тогда
m(NaOH)= (4,5х2)/4,3 = 2,09 г
для 4,3 г сульфаниловой кислоты необходимо 25 г NaCl,
а для 4,5 г––––– Х г,тогда
m(NaCl)= (4,5х25)/4,3 = 26,2г
Таким образом, для синтеза сульфаниловой кислоты необходимо:
13,08 см3 едкого натра,
13,08 см3 соляной кислоты,
2,09 г едкого натра (порошок),
26,2г хлорида натрия.
Запишем новое мольное соотношение: NH2C6H4SO2OH : NaNО2 : C10H7OH =0,026: 0,0319: 0,0262
3.3 Таблица - Количества исходных веществ, применяемых в синтезе:
|
Реагент |
Число моль |
В граммах |
Объем, см 3
| |
|
Основные вещества | ||||
|
NH2C6H4SO2OH |
0,026 |
4,5г |
- | |
|
NaNО2 |
0,0319 |
2,2 г |
- | |
|
C10H7OH |
0,0262 |
4,6г |
- | |
|
Вспомогательные вещества | ||||
|
NaOH |
0,0349 |
- |
13,08 | |
|
HCl |
0,0349 |
- |
13,08 |
|
|
NaOH(порошок) |
0,0698 |
2,09г |
- | |
|
NaCl |
0,5962 |
26,2г |
- | |