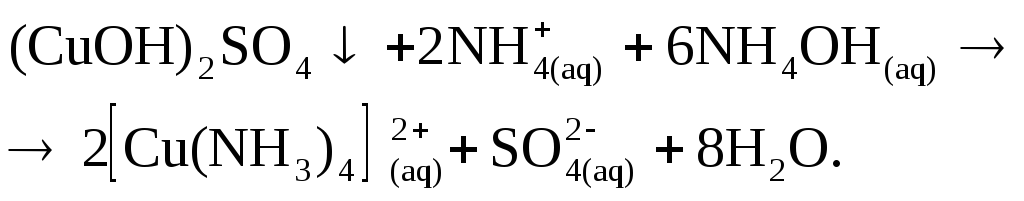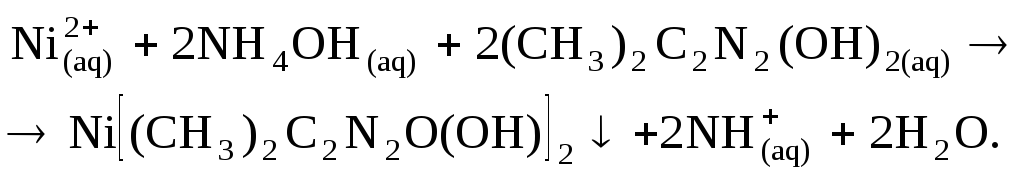- •Введение
- •Систематический анализ катионов кислотно-основным методом
- •Групповые реакции катионов по кислотно-основному методу
- •2. Качественные аналитические реакции катионов
- •2.1.Первая аналитическая группа катионов
- •2.3. Третья аналитическая группа катионов
- •2.4. Четвертая аналитическая группа катионов
- •2.5.Пятая аналитическая группа катионов
- •2.6. Шестая аналитическая группа катионов
- •3. Краткие указания по технике выполнения аналитических работ
- •4. Аналитическая работа №1 Анализ смеси катионов первой и второй аналитических групп
- •4.1. Анализ осадка 1
- •4.2. Анализ раствора 1
- •5. Аналитическая работа № 2 Анализ смеси катионов третьей и четвертой аналитических групп
- •5.1. Определение III аналитической группы
- •5.2. Анализ раствора 2
- •5.3. Анализ раствора 3
- •5.4. Анализ осадка 3
- •6. Аналитическая работа №3 Анализ смеси катионов пятой и шестой аналитических групп
- •6.1. Состав предварительных испытаний
- •6.2. Анализ осадка 1
- •6.3. Анализ аммиачного раствора 1
- •6.4. Анализ осадка 3
- •6.5. Анализ раствора 5
- •7. Аналитическая работа №4 Анализ смеси катионов всех шести аналитических групп
- •8. Пример решения задач на основании схем качественного анализа
- •9. Задачи для решения
2.5.Пятая аналитическая группа катионов
2.5.1. Катион
![]() в водных растворах
бесцветен.
в водных растворах
бесцветен.
Определяется по реакции с гидроортофосфатом натрия при рН9 в присутствии ионов аммония. Реакция идет с образованием белого кристаллического осадка двойной солиортофосфата аммония-магния:
|
|
(34) |
Назначение
добавки
![]() заключается в увеличении концентрации
ионов аммония в растворе для снижения
требуемого расхода гидроксида аммония
и предотвращения образования осадка
гидроксида магния.
заключается в увеличении концентрации
ионов аммония в растворе для снижения
требуемого расхода гидроксида аммония
и предотвращения образования осадка
гидроксида магния.
Ход анализа.К 2 каплям раствора
соли магния добавить раствор хлорида
аммония, 2 капли гидроортофосфата
натрия и гидроксид аммония (2 н.) до
рН9 (по каплям, при
перемешивании и измерении рН после
добавления каждой капли). Если белый
кристаллический осадок не образуется,
то необходимо добавить![]() и потереть внутренние стенки пробирки
стеклянной палочкой.
и потереть внутренние стенки пробирки
стеклянной палочкой.
2.5.2. Катион ![]() в относительно
концентрированных растворах соли имеют
бледно-розовый цвет, в разбавленных
растворахбесцветны.
в относительно
концентрированных растворах соли имеют
бледно-розовый цвет, в разбавленных
растворахбесцветны.
Определяется окислением до Mn (VII) висмутатом натрия в азотнокислой среде с образованием розового раствора марганцевой кислоты:
|
|
(35) |
Ход анализа.К 2-м каплям раствора соли марганца (II) прибавить 2 мл 6 н. раствора азотной кислоты и немного твердого висмутата натрия (на кончике шпателя). Смесь перемешать. При этом образуется раствор марганцевой кислоты розового цвета.
2.5.3. Катион ![]() растворы имеют
желтую окраску.
растворы имеют
желтую окраску.
А. Определяется реакцией комплексообразования с тиоцианатом (роданидом) с образованием кроваво-красного раствора тритиоцианатажелеза (III)
|
|
(36) |
Ход анализа.К нескольким каплям раствора соли железа (III) добавить по каплям раствор тиоцианата аммония или калия до образования кроваво-красного раствора.
Б. Другим известным способом определения железа (III) является реакция с гексацианоферратом (II) калия. При этом образуется темно-синий осадок гексацианоферрата (III) железа (II) («берлинская лазурь»):
|
|
(37) |
Ход анализа.К нескольким каплям раствора соли железа (III) добавить по каплям раствор гексацианоферрата (II) калия до образования темно-синего осадка.
2.6. Шестая аналитическая группа катионов
2.6.1. Катион
![]() растворы солей
окрашены в голубой или зеленый цвет.
растворы солей
окрашены в голубой или зеленый цвет.
А. Определяется по реакции комплексобразования в избытке гидроксида аммония с образованием ярко-синего раствора, содержащего комплексный катион тетраамминмеди (II). Реакция протекает в две стадии. Сначала образуется зеленый осадок основной соли меди (например, гидроксосульфата)
|
|
(38) |
который растворяется в избытке гидроксида аммония
|
|
(39) |
Ход анализа.К нескольким каплям раствора соли меди добавить по каплям 2 н. раствор гидроксида аммония, наблюдая сначала образование зеленого осадка, а затем его растворение с образованием ярко-синего раствора.
Б. Более чувствительным, чем реакция с аммиаком, является обнаружение Cu2+с гексацианоферратом (II) калия. При рН7 образуется красно-бурый осадок гексацианоферрата (II) меди:
|
|
(40) |
Осадок не растворим в разбавленных кислотах, но растворяется в аммиаке и разлагается при действии щелочей.
2.6.2. Катион ![]() растворы солей
окрашены в зеленый цвет.
растворы солей
окрашены в зеленый цвет.
Никель определяется по реакции с диметилглиоксимом в аммиачной среде (рН8-10), с которым он образует малиновый осадок внутрикомплексной солидиметилглиоксимата натрия
|
|
(41) |
Диметилглиоксим (реактив Чугаева) является двухдентатным лигандом со структурной формулой:
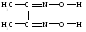
имеющим два донорных атома азота. Реактив
очень чувствителен к иону
![]() ,
с которым он образует очень прочное
внутрикомплексное соединение (хелат),
содержащее пятичленные циклы во
внутренней сфере комплекса:
,
с которым он образует очень прочное
внутрикомплексное соединение (хелат),
содержащее пятичленные циклы во
внутренней сфере комплекса:

Ход анализа.К 2-3 каплям раствора соли никеля добавить 1-2 капли раствора диметилглиоксима и несколько капель разбавленного раствора гидроксида аммония до рН8-10.
2.6.3.Катион
![]() растворы солей
имеют розовый цвет. Определяется по
реакции с тетрароданомеркуратом аммония
при рН=5 с образованием синего
кристаллического осадка тетрароданомеркурата
кобальта (III). Добавление
растворы солей
имеют розовый цвет. Определяется по
реакции с тетрароданомеркуратом аммония
при рН=5 с образованием синего
кристаллического осадка тетрароданомеркурата
кобальта (III). Добавление![]() ускоряет реакцию:
ускоряет реакцию:
|
|
(42) |
Ход анализа.К 2-3 каплям раствора соли кобальта (II) добавить 1-2 капли ацетатного буфера (pH5), избыток тетрароданомеркурата аммония, 1-2 капли раствора сульфата цинка и перемешать.Примечание. Выпадение осадка может происходить через некоторое время после смешивания реактивов.
2.6.4. Катион ![]() в водных растворах
бесцветен.
в водных растворах
бесцветен.
Определяется по реакции с сероводородом при рН=0,5-0,8 с образованием желтого осадка сульфида кадмия, в разбавленных растворах образуется коллоидный раствор также желтого цвета
|
|
(43) |
Ход анализа.К нескольким каплям соли кадмия добавить сероводородную воду до образования желтого осадка или коллоидного раствора того же цвета.
2.6.5. Катион![]() в водных растворах
бесцветен.
в водных растворах
бесцветен.
Способом обнаружения
![]() является восстановление его металлической
медью
является восстановление его металлической
медью
|
|
(44) |
с образованием медно-ртутной амальгамы (светлое пятно).
Ход анализа.Медную пластину предварительно обработать азотной кислотой для удаления пассивирующей пленки оксида меди, промыть водой и протереть фильтровальной бумагой. На подготовленную медную пластину капнуть раствор нитрата ртути (II) и наблюдать образование светлого металлического пятна.