
- •1 Кинетика физико-химических процессов. Химическое равновесие
- •1.1 Значимость изучаемой темы
- •1.2 Требования к исходному уровню знаний и умений
- •1.3 Содержание темы. Основные понятия и определения
- •1.3.1 Скорость химической реакции
- •1.3.2 Необратимые и обратимые реакции. Химическое равновесие
- •1.3.3 Катализ
- •1.4 Примеры решения типовых задач
- •1.5 Контроль усвоения темы
- •1.5.1 Индивидуальные задания
- •1.5.2 Вопросы для тестового контроля знаний
- •2 Растворы электролитов и их основные характеристики
- •2.1 Значимость изучаемой темы
- •2.2 Требования к исходному уровню знаний и умений
- •2.3 Cодержание темы. Основные понятия и определения
- •2.3.1 Растворы электролитов. Основы теории электролитической диссоциации
- •2.3.2 Основные характеристики растворов электролитов
- •2.4 Примеры решения типовых задач
- •2.5 Контроль усвоения темы
- •2.5.1 Индивидуальные задания
- •2.5.2 Вопросы для тестового контроля знаний
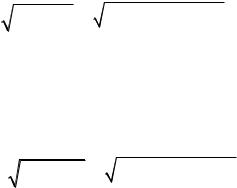
α = |
K |
Д |
/ С |
M |
= 1,8 10−5 |
/ 5 10−3 |
= 6 10−2 ; |
1 |
|
|
|
|
|
C |
OH |
− =α C |
|
=6 10−2 5 10−3 =3 10−4 моль/л; |
||||||
|
|
|
1 |
|
M1 |
|
|
|||
pOH = – lg COH− = – lg 3·10-4 = 3,52. |
Откуда рH =14 –3,52 = 10,48. |
|||||||||
Теперь рассчитаем |
рH |
раствора, |
разбавленного в 10 раз, |
|||||||
CM2 = 0,00005 моль/л: |
|
|
|
|
|
|
|
|
|
|
|
α |
2 |
= |
K |
Д |
/ С |
= 1,8 10−5 /5 10−4 =0,19; |
|||
|
|
|
|
|
M2 |
|
||||
COH− =α2 CM2 =1,9 10−1 5 10−4 =9,5 10−5 моль/л;
pOH = – lg СOH- = – lg 9,5·10-5 = 4,0. Откуда рH =14 – 4,0 = 10. Итак, вслед-
ствие разбавления раствора рH уменьшилось с 10,48 до 10.
2.5 Контроль усвоения темы
Если Вы не сможете решить какую-либо из предлагаемых задач, обратитесь к разделу 2.4 данного методического пособия.
2.5.1 Индивидуальные задания
Вариант 1
1. Вычислите концентрацию ионов водорода в 0,01 М растворах кислоты и основания:
а) HNO3; б) NaOH.
2.ОпределитеpH 0,46%-ногораствора(ρ=1г/ мл) муравьинойкислотыHCOOH.
3.Сколько граммов гидроксида аммония NH4OH содержится в 1л раствора, pH которого равен 10,62?
Вариант 2
1.При какой молярной концентрации раствора CH3COOH недиссоциированными останется: а) 50% молекул кислоты; б) 80%молекул?
2.Вычислите pH 0,01 М KOH и 0,01 М NH4OH . Объясните различие в зна-
чениях pH для этих растворов.
3. Какова степень диссоциации бромноватистой кислоты HOBr в ее 2,425%- ном растворе (ρ =1 г/ мл), если pH раствора равен 2.
Вариант 3
1. Вычислите концентрацию гидрооксид – ионов в 0,01 М растворах кислоты и основания:
а) HOBr; б) NH4OH.
2. Определите pH раствора гидроксида калия KOH , если концентрация ионов K+ в этом растворе составляет 10−4 моль/л.
47
3. Определите, сколько граммов H2SO4 содержится в 1л раствора кислоты, pOH которого равен 12. Запишите уравнение диссоциации H2SO4 , если α =1.
Вариант 4
1.В 100мл раствора содержится 0,745г KCl . Вычислите концентрацию ионов калия и хлорид–ионов в этом растворе.
2.Одинаковы ли значения pH растворов KOH и NH4OH одинаковой кон-
центрации, равной0,01 М? Ответобосноватьуравнениемдиссоциацииирасчетами. 3. Определите молярную концентрацию раствора уксусной кислоты CH3COOH , если pH =5,2 . Запишите уравнение диссоциации кислоты и выра-
жение для константы диссоциации.
Вариант 5
1. Вычислите концентрацию ионов водорода в 0,05 М растворах основания и кислоты:
а) Ba(OH)2 ; б) H2SO4.
2.ОпределитеpH 1,75% - ногораствора(ρ =1 г/ мл) гидроксидааммония NH4OH
3.Сколько граммов уксусной кислоты CH3COOH содержится в 1л раствора,
pH которого равен 2,87? Запишите уравнение диссоциации кислоты и выражение для константы диссоциации.
Вариант 6
1.Определите концентрацию ионов OH− в растворе, если известно, что в 500мл егосодержится0,098гсернойкислоты H2SO4 . Диссоциациюкислотысчитатьполной.
2.Вычислите pH 0,01 М раствора HCl и 0,01 М раствора CH3COOH . Объясните различие в значениях.
3.Какова степень диссоциации гидроксида аммония NH4OH в его 0,175% -
ном растворе (ρ =1 г/ мл), если pOH раствора равен 11.
Вариант 7
1. |
Вычислите концентрацию OH− в 0,001 М растворах основания и кислоты: |
|
а) NH4OH; |
б) HOCl. |
|
2. |
Определите pH раствора гидроксида бария Ba(OH)2 , если концентрация |
|
ионов Ba2+ в этом растворе составляет 0,005 моль/л. |
||
3. |
Определите сколько граммов HNO3 содержится в 1л раствора, pОH кото- |
|
рого равен 10. Запишите уравнение диссоциации HNO3 , если α =1.
Вариант 8
1. При какой молярной концентрации раствора муравьиной кислоты
48
HCOOH недиссоциированными останется: |
а) 50% молекул кислоты; |
б) 90% молекул кислоты? |
|
2.Определите pH раствора, в 500мл которого содержится 0,14г KOH .
3.Чему равны молярные концентрации растворов H2SO4 и Ca(OH)2 , если для первого раствора pH =1, а для второго 13? Запишите уравнения диссоциации, если α =1.
Вариант 9
1. Вычислитеконцентрациюионовводородав0,1 Мрастворахкислотыиоснования:
а) HNO3; |
б)KOH |
|
|
|
2. Определите pH |
0,49%-ного раствора ( |
ρ =1 г/ мл ) |
уксусной |
кислоты |
CH3COOH. |
|
|
|
|
3. Сколько граммов гидроксида аммония |
NH4OH и |
гидроксида |
натрия |
|
NaOH содержится в 1л их растворов, если значения pH у них одинаковы и равны 11,13? Ответподтвердитьуравнениямидиссоциацииисоответствующимирасчетами.
Вариант 10
1. Для приготовления 200мл раствора уксусной кислоты CH3COOH использовали 0,06г кислоты. Определите концентрацию ионов водорода и ацетат–ионов
вполученном растворе.
2.Чему равны значения pH 0,001 М растворов сильных электролитов HCl,
NaOH ?
3. Определите молярную концентрацию раствора азотистой кислоты HNO2 , если pH = 2 . Запишите уравнение диссоциации кислоты и выражение для константы диссоциации.
Вариант 11
1. Вычислите концентрацию OH− в 0,1 М растворах кислоты и основания:
а)CH3COOH; б) NH4OH
2.Определите pOH раствора азотной кислоты HNO3 , если концентрация ионов NO3− в этом растворе составляет 0,001 моль/л.
3.Найдите массу Ba(OH)2 , содержащегося в 250мл водного раствора, если pH этого раствора равен 13.
Вариант 12
1. В 200мл раствора содержится 1,3г хлорида никеля NiCl2 . Вычислите концентрацию ионов никеля и хлорид–ионов в растворе.
2. Запишите уравнения диссоциации HNO2 (КД = 4 10–4) и HNO3 (α = 1) и определите рН и рОН растворов этих кислот одинаковой молярной концентрации,
49
равной 0,01 М.
3. Чему равны молярные концентрации растворов H2SO4 ,Ca(OH)2 , если для первогораствора pH =1, адлявторого13? Запишитеуравнениядиссоциации, если α =1.
Вариант 13
1. Вычислите концентрацию ионов водорода в 0,5 М растворах основания и кислоты:
а) Ca(OH)2 ; б) H2SO4.
2.Определите pH 0,72%-ного раствора ( ρ =1 г/ мл ) иодноватистой кислоты
HOI.
3.Найдите массу H2SO4 , растворенной в 250мл раствора, если pH раствора
равен 1. Запишите уравнения диссоциации H2SO4 , если α =1.
Вариант 14
1. Определите концентрацию ионов OH− в растворе, если известно, что в 250мл его содержится 1,225г серной кислоты H2SO4 . Диссоциацию кислоты
считать полной.
2.Запишите уравнение диссоциации слабого основания и рассчитайте pH раствор, в 500мл которого содержится 0,175г NH4OH .
3.Определите молярную концентрацию раствора метаборной кислоты HBO2 , если pH = 4 . Запишите уравнение диссоциации кислоты и выражение
для константы диссоциации.
Вариант 15
1. Вычислите концентрацию OH− в 0,02 М растворах кислоты и основания:
а) HOI; б) NH4OH.
2.Определите pOH раствора серной кислоты H2SO4 , если концентрация ионов SO42− в этом растворе составляет 0,005 моль/л.
3.Сколько граммов уксусной кислоты CH3COOH содержится в растворе, pH которого равен 5,2? Запишите уравнение диссоциации кислоты и выражение
для константы диссоциации.
Вариант 16
1.В 0,05 М растворе HCN степень диссоциации равна 1,26 10−4 . При какой концентрации раствора она увеличится в 5 раз?
2.Чему равны значения pH 0,5 М растворов сильных электролитов H2SO4 и
Ba(OH)2 ? Как изменятся их значения при разбавлении растворов в 10 раз?
3. Одинаковы ли значения молярной концентрации растворов KOH и NH4OH , если значения pH растворов одинаковы и равны 11,13? Ответ подтвер-
дите уравнениями диссоциации и соответствующими расчетами.
50
