
- •Контрольная работа Вариант 1
- •Контрольная работа Вариант 2
- •Контрольная работа Вариант 3
- •Контрольная работа Вариант 4
- •Контрольная работа Вариант 5
- •Контрольная работа Вариант 6
- •Контрольная работа Вариант 7
- •Контрольная работа Вариант 8
- •Контрольная работа Вариант 9
- •Контрольная работа Вариант 10
- •Контрольная работа Вариант 11
- •Контрольная работа Вариант 12
- •Контрольная работа Вариант 13
- •Контрольная работа Вариант 14
- •Контрольная работа Вариант 15
- •Контрольная работа Вариант 16
- •Контрольная работа Вариант 17
ГОУ ВПО
«СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
Ханты-Мансийского автономного округа – Югры»
Кафедра: химии Утверждено на заседании
Дисциплина: химия кафедры
Факультет: химико-технологический
Направления: УТС, ИТСС, Электроэнергетика
Контрольная работа Вариант 1
На основе энергетических диаграмм молекулярных орбиталей и порядка связи объяснить, почему удаление электрона из молекулы О2 упрочняет, а из молекулы N2 ослабляет химическую связь?
Методом электронного или электронно-ионного баланса подобрать коэффициенты в окислительно-восстановительном уравнении реакции:
![]()
Константа скорости некоторой реакции при 20оС равна 2.10 -2 л/моль·с, а при 40 оС 3,6.10-1. Определить энергию активации.
Вычислить осмотическое давление раствора, содержащего в 1,4л воды 63г глюкозы
 при 0оС.
при 0оС.
Рассчитать стандартную энтальпию процесса образования 100г этилацетата по реакции:
![]() ,
,
если стандартные теплоты сгорания равны Н0сг 298(СН3СООН)=871,6 кДж/моль;
Н0сг 298(С2 Н5ОН)=1374 кДж/моль; Н0сг 298(СН3СООС2Н5)=2256 кДж/моль; теплота образования Н0сг 298(Н2О)=-241,83 кДж/моль.
6. Вычислить константы кислотности муравьиной, уксусной, бензойной, монохлоруксусной, пировиноградной, молочной кислот, записать формулы, расположить соединения в ряд увеличения кислотности, объяснить ряд, если рКк соответственно составляют 3,75; 4,75; 4,30; 2,87; 2,49; 3,87.
7. Вычислите молярную, моляльную, моль-эквивалентную концентрацию 10% раствора серной кислоты с плотностью 1,06 г/мл.
к.х.н., доцент Л.А. Журавлева
ГОУ ВПО
«СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
Ханты-Мансийского автономного округа – Югры»
Кафедра: химии Утверждено на заседании
Дисциплина: химия кафедры
Факультет: химико-технологический
Направления: УТС, ИТСС, Электроэнергетика
Контрольная работа Вариант 2
1. На
основе энергетических диаграмм
молекулярных орбиталей и порядка связи
объяснить, почему удаление электрона
из молекулы
![]() упрочняет, а из молекулы
упрочняет, а из молекулы![]() ослабляет химическую связь.
ослабляет химическую связь.
2. Методом электронного или электронно-ионного баланса подобрать коэффициенты в окислительно-восстановительном уравнении реакции:
![]()
3. Начальная скорость реакции А(г)+В(г) АВ(г) составляет 4.10-6моль/л.с. Начальная концентрация обоих веществ равна 0,02 моль/л. Определить константу скорости реакции и скорость в момент времени, когда концентрации вещества АВ будет равна 0,005 моль/л.
Вычислить на сколько градусов понизится температура замерзания бензола, если в 100г его растворили 2,5г нафталина
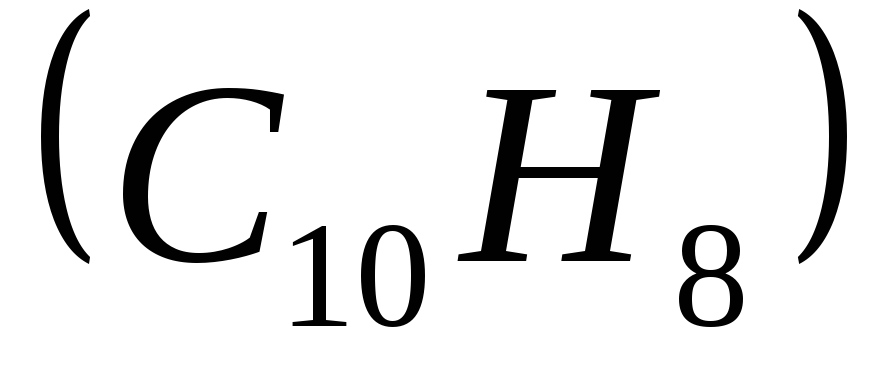 .
. .
.
5. Рассчитать значения энтальпии и теплоты процесса:
2H2S + O2 S+2H2S, если известно, что
Н0обр 298(H2S)= -20,60 кДж/моль; Н0обр.(Н2О)= -285,83 кДж/моль.
6. Вычислить константы кислотности муравьиной, уксусной, бензойной, монохлоруксусной, пировиноградной, молочной кислот, записать формулы, расположить соединения в ряд увеличения кислотности, объяснить ряд, если рКк соответственно составляют 3,75; 4,75; 4,30; 2,87; 2,49; 3,87.
7.Вычислите молярную, моляльную, моль-эквивалентную концентрацию 15% раствора фосфорной кислоты с плотностью 1,085 г/мл.
к.х.н., доцент Л.А. Журавлева
ГОУ ВПО
«СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
Ханты-Мансийского автономного округа – Югры»
Кафедра: химии Утверждено на заседании
Дисциплина: химия кафедры
Факультет: химико-технологический
Направления: УТС, ИТСС, Электроэнергетика
