
- •Глава 6. Водно-минеральный баланс
- •6.1. Роль макро- и микроэлементов
- •Биодоступность элементов (% усвоения)
- •Допустимые уровни содержания некоторых токсичных элементов
- •Расчетные уровни минимальных и максимальных значений макро- и микроэлементов в водно-пищевых рационов жителей зоны эколого-биогеохимического оптимизма
- •Биологическая роль макроэлементов
- •Пищевые продукты – источники магния
- •Основные функции микроэлементов
- •Суточные потребности человека в йоде (мкг/сутки) (воз, 2007)
Основные функции микроэлементов
К ним относят более 30 элементов периодической системы. Остановимся на роли некоторых из них. Многие представители включены в состав гормонов, витаминов, ферментов и других важных соединений.
Железо – (Рис. 3.27) – d-элемент, выполняющий ответственнейшие функции в жизни человека и животных; вследствие того, что это переходный металл, участник окислительно-восстановительных реакций.
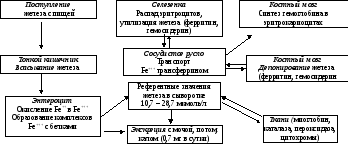
Рис. 3.27. Схема метаболизма железа в организме
С этой целью железо введено в состав порфиринов, в первую очередь – гема, который связываясь с различными белками, дает начало Hb, миоглобину, цитохромам, каталазе, пероксидазе. Их первый представитель, заполняя эритроциты, захватывает в легких О2 и отдает его клеткам других органов. В мышцах, обусловливая их цвет, содержится миоглобин, легко связывающийся с кислородом и служащий его депо. Каталаза и пероксидаза – биокатализаторы, участвуют в восстановлении различных пероксидов, в первую очередь, - Н2О2. В цитохромах используется способность железа менять валентность: данные гемопротеиды – непременные звенья ЭТЦ. С другой стороны, катионы этого металла могут быть донорами электронов, проявляя прооксидантные свойства (участники в образовании АФК). Его катионы включаются в активные центры различных оксидаз, гидролаз, СОД и других энзимов.
Медь – также является переходным металлом, отсюда у него регистрируется определенное сходство с железом по биологическим свойствам. Супероксиддисмутаза (Сu, Zn–содержащая) – один из ключевых ферментов АРЗ, нейтрализующий супероксидные радикалы. Цитохромоксидаза, тоже имеющая в структуре ионы этого металла, - заключительное звено ЭТЦ. Энзимы, включающие Сu, участвуют в синтезе гема, катехоламинов, меланинов, фосфолипидов, железосодержащих протеинов, коллагена; данный биотик обнаруживается в составе некоторых белковых факторов свертывания крови. Как и железо, медь способствует генерации АФК. Основными пищевыми источниками меди служат печень, огурцы, орехи, какао, брусника (до 2,5%), плоды шиповника, грибы, шоколад, но молочные продукты обеднены ею. В плазме крови ионы металла транспортируются в составе гликопротеина церулоплазмина, который не только обеспечивает гомеостаз Сu++, но и является ферроксидазой, белком острой фазы воспаления, АО.
Суточная потребность в цинке в зависимости от биодоступности его пищевых соединений (Табл. 3.5) и физиологического состояния (у беременных и лактирующих женщин до 30–50 мг) колеблется от 5 до 22 мг. Лучше усваиваются катионы этого металла, содержащиеся в продуктах животного происхождения (мясе, рыбе, яйцах), в меньшей степени – в семенах тыквы, зерновом хлебе, чернике, грибах, овсянке, бобовых. Образуя димеры с инсулином, данный микроэлемент способствует его депонированию и бережному использованию. Участвует в созревании репродуктивных органов, играет важную роль в поддержании иммунного статуса за счет способности блокировать синтез оксида азота, цитокинов. Но особенно много Zn++ выступает в качестве активатора различных ферментов аминокислотного, нуклеотидного, липидного, углеводного обменов (более 300 энзимов), является кофактором ЛДГ, ЩФ, ДНК- и РНК- полимераз, карбоангидразы. Zn-энзимы – матриксные металлопротеиназы (коллагеназы, эластазы, протеогликаназы и т.д.) разрушают белки соединительной ткани. В ЦНС ионы металла используются в качестве нейротрансмиттеров и нейромодуляторов, при высоких же концентрациях провоцируют апоптоз или некроз нейронов.
В сравнении с другими микроэлементами жизненно важная роль селена была выявлена относительно недавно. Суточная потребность варьирует в следующих пределах: 50–500 мкг; его концентрация в продуктах питания во многом зависит от географии местности. Обычно основными источниками данного биотика считают кокос, фисташки, чеснок, морскую рыбу и морепродукты (устрицы, креветки), свинину, грибы при условии их происхождения из регионов, богатых Se. В организм он попадает в составе селен-содержащих аминокислот (Se-цистеина, Se-метионина), которые внедряются в различные белки-энзимы (описано более 30): глутатионпероксидазу , отвечающую за разрушение в тканях Н2О2 и органических пероксидов. Отсюда селен экранирует от СРО липиды мембран, а также полинуклеотиды, токоферолы и другие клеточные структуры. Другой Se-содержащий фермент – тиоредоксинредуктаза – восстанавливает монорибонуклеотиды; полученные в этой реакции дезоксирибонуклеотиды служат субстратами в генезе ДНК.
И
радиопротекторный,
антиканцерогенный; предотвращающий
развитие окислительного стресса,
лежащего в основе воспаления, старения,
ишемии и т.д.; антимутагенный,
антитератогенный; ингибирующий
апоптоз; регулирующий
клеточную пролиферацию; антигистаминный,
антиаллергический; подавляющий
депрессию, состояние тревоги, усталости; стимулирующий
репродуктивные функции; облегчающий
адаптацию к неблагоприятным факторам; нормализующий
баланс дистантных (тироидных, СТГ),
тканевых и внутриклеточных (ПГ, ПЦ, ЛТ
и др.) гормонов; служащий
мощным иммуномодулятором; усиливающий
фагоцитарную активность макрофагов; уменьшающий
вредное воздействие токсинов (солей
тяжёлых металлов, нитритов и других
нитропроизводных, микотоксинов,
лекарств, различных ксенобиотиков); обладающий
антиаритмическим влиянием на проводящую
систему сердца, снижающий артериальное
давление.
радиопротекторный,
антиканцерогенный; предотвращающий
развитие окислительного стресса,
лежащего в основе воспаления, старения,
ишемии и т.д.; антимутагенный,
антитератогенный; ингибирующий
апоптоз; регулирующий
клеточную пролиферацию; антигистаминный,
антиаллергический; подавляющий
депрессию, состояние тревоги, усталости; стимулирующий
репродуктивные функции; облегчающий
адаптацию к неблагоприятным факторам; нормализующий
баланс дистантных (тироидных, СТГ),
тканевых и внутриклеточных (ПГ, ПЦ, ЛТ
и др.) гормонов; служащий
мощным иммуномодулятором; усиливающий
фагоцитарную активность макрофагов; уменьшающий
вредное воздействие токсинов (солей
тяжелых металлов, нитритов и других
нитропроизводных, микотоксинов,
лекарств, различных ксенобиотиков); обладающий
антиаритмическим влиянием на проводящую
систему сердца, снижающий артериальной
давление.
В настоящее время трудно найти заболевание, в терапии которого бы не использовались препараты селена.
Суточная потребность марганца колеблется (Табл. 3.7) в зависимости от возраста (у детей 5-7 лет – 0,07-0,1 мг/кг, у подростков – 0,08-0,09 мг/кг), от характера питания. Кишечной абсорбции его соединений препятствуют кальций, железо, фосфаты. Потребление продуктов, имеющих значительное количество таннина (чай) и оксалатов (томаты, шпинат), может также снизить усвоение Mn (Табл. 3.5). Биологическую роль этого биотика трудно переоценить: включаясь в различные биополимеры, он регулирует их функции. Принимает непосредственное участие в формировании спиральных структур нуклеиновых кислот; поддерживает архитектонику некоторых ферментов-мультимеров; входит в активные центры окислительных энзимов; является компонентом Mn-содержащей супероксиддисмутазы, обеспечивая тем самым АРЗ; потенцирует действие инсулина; нормализует обмен коллагена и гликозамингликанов (мукополисахаридов), усиливая рост волос, ногтей, процессы окостенения. Кроме того, активирует пируваткарбоксилазу, аргиназу, фосфатазы, гексокиназу, проявляет липотропное действия.
Кобальт в тканях животных и человека включен в состав витамина В12, который служит коферментом различных трансфераз и изомераз. Представителем последних можно назвать метилмалонил-КоА-мутазу – один из энзимов синтеза гема – простетической группы гемопротеидов (роль которых описана выше). Кроме того, соединения кобальта обладают гипотензивным эффектом, стимулируют продукцию некоторых гормонов (тироидных, катехоламинов). Биокатализаторы, содержащие катионы этого металла, участвуют в образовании фосфолипидов – молекулярных структур биомембран клеток, оболочек нервных волокон. Из компонентов питания наиболее богаты этим МЭ мясо, печень, рыба, молочные продукты, бобовые, чеснок.
Среди вышеперечисленных элементов все имеют положительные валентности, и только представители галогенов отрицательно заряжены. В нашей стране фтор в большинстве пищевых источников регистрируется в десятых долях миллиграмма на 1 кг массы. Количество МЭ в хлебобулочных изделиях зависит от его уровня в применяемой воде. В овощах, фруктах, ягодах значения фтора варьируют от 0,1 до 0,4 мг/кг. В основном он накапливается в зеленых частях растений (петрушки, сельдерея, шпината, киндзы, салата, капусты); зеленые листья чая тоже богаты этим галогеном (до 200 мг/кг). Близкие величины характерны для продуктов животного происхождения: в мясе констатируется не более 0,6 мг/кг, рыбе – меньше того (до 0,4 мг/кг), еще ниже в молоке (до 0,25 мг/л). По выполняемым функциям фтор принадлежит к остеотропным элементам. Его основная масса локализуется в костной ткани, особенно в зубной эмали в виде гидроксиапатита.
Йод - элемент той же группы, что и фтор. Вымываясь из горных пород, аккумулируется в морской воде и морских организмах; легко возгоняется (что и происходит при хранении йодированной соли при теплвой обработке пищи). Для удовлетворения суточной потребности в этом галогене (Табл. 3.9) можно использовать лишь продукты морского происхождения (рыбу, моллюски, водоросли).
Таблица 3.9
