
- •Е. А. Михайлов, н. А. Мухин,
- •150023. Ярославль, Московский пр., 88.
- •150000. Ярославль, ул. Советская, 14а.
- •Введение
- •1. Химические и физические свойства природных вод
- •1.1 Основные физические свойства воды, снега и льда
- •1.1.1 Плотность и удельный объем
- •1.1.2 Удельная теплота парообразования воды и плавления снега и льда
- •1.1.3 Теплоемкость и теплопроводность
- •1.1.4 Молекулярная вязкость. Поверхностное натяжение
- •1.2. Химические свойства воды
- •1.3. Характеристика природных вод
- •1.4 Классификации состава природных вод
- •2. Гидрология рек
- •2.1 Гидрографическая сеть. Речные системы. Главные реки и их притоки.
- •2.2 Исток и устье реки. Основные виды устьев. Устьевые области
- •2.3 Скорости течения воды и распределение их по живому сечению
- •2.4 Средняя скорость в живом сечении. Формула Шези
- •2.5 Поперечные циркуляции
- •2.6 Вихревые движения
- •2.7 Основные закономерности структуры гидрографической сети. Густота речной сети.
- •2.8 Склоновая эрозия
- •2.9 Речной бассейн. Поверхностный и подземный водосборы. Водоразделы. Деление и смешение вод.
- •2.10 Морфометрические характеристики речного бассейна
- •2.11 Речные долины. Элементы долины и поймы.
- •2.12 Характерные речные образования
- •3. Гидрология озер
- •3.1 Происхождение, типы и морфология озерных котловин
- •3.2 Формирование озерного ложа под влиянием волнения и отложения наносов
- •3.3 Зарастание озер
- •3.4 Географическое положение озера. Морфометрические характеристики
- •3.5 Уровневый режим озер
- •3.6 Динамические явления в озерах
- •3.7 Сейши
- •3.8 Изменение температуры воды в озерах в течение года
- •3.9 Ледовые явления
- •3.10 Формирование химического режима
- •3.11 Биологические процессы
- •3.12 Озерные отложения
- •4. Гидрология водохранилищ
- •4.1 Основные особенности гидрологического режима водохранилищ
- •4.2 Режим уровней
- •4.3 Условия водообмена
- •4.4 Формирование берегов
- •4.5 Ледовый режим
- •5. Гидрология ледников.
- •5.1 Фирн. Ледниковый лед, его свойства.
- •5.2 Движение ледников
- •5.3 Таяние ледников
- •5.4 Особенности режима рек с ледниковым питанием
- •6. Гидрология болот
- •6.1 Образование болот и их типы
- •6.2 Болотная гидрографическая сеть
- •6.3 Гидрологический режим болот
- •6.4 Движение воды в торфяном грунте и на болотных массивах
- •6.5 Колебания уровня грунтовых вод на болотных массивах
- •6.6 Сток с болот
- •6.7 Испарение с болотных массивов
- •7. Гидрология подземных вод
- •7.1 Теории и гипотезы происхождения подземных вод
- •7.2 Классификация подземных вод по условиям их происхождения
- •7.3 Виды воды в порах горных пород и почв
- •7.4 Виды воды в порах
- •7.5 Условия залегания подземных вод в земной коре
- •7.6 Вода в почве
- •7.7 Грунтовые и межпластовые безнапорные воды
- •7.8 Напорные воды
- •7.9 Движение подземных вод
- •7.10 Подземные источники
- •7.11 Режим грунтовых вод. Зависимость колебаний уровня от климата
- •7.12 Взаимосвязь речных и подземных вод
- •7.13 Минеральные воды
- •8. Гидрология океанов и морей
- •8.1 Формы морского шельфа
- •8.2 Формы движение морских вод
- •9. Практические задания к главе 1
- •10. Практические задания к главе 2
- •11. Практические задания к главе 3
- •12. Практические задания к главе 4
- •13. Практические задания к главе 5
- •14. Практические задания к главе 6
- •15. Практические задания к главе 7
- •16. Практические задания к главе 8
- •Заключение
- •Список использованных источников
9. Практические задания к главе 1
Понятия и определения.
Вода (Н2О) – слабый электролит, молекула которого состоит из одного водородного (Н+) и одного гидроксильного (ОН--) ионов. Вода является хорошим растворителем химических соединений.
Суммарное содержание в воде растворенных неорганических веществ выражают в виде минерализации (М, мг/л, г/л) либо в виде солености (S, 0/00).
По содержанию солей (минерализации или солености) природные воды подразделяют на 4 группы: пресные – менее 10/00, солоноватые – 1-250/00, соленые (морской солености) – 25-500/00, высокосоленые (рассолы) – более 500/00.
К числу главных ионов солей, находящихся в природных водах, относятся отрицательно заряженные ионы (анионы) – НСО3- - гидрокарбонатный, SO4-2 – сульфатный, Cl- - хлоридный и положительно заряженные ионы (катионы) – кальция Са+2, магния Mg+2, натрия Na+, калия К+.
Вода в природе может находиться в твердом (лед), жидком (собственно вода) и газообразном (водяной пар) агрегатных состояниях. Температура, при которой происходит кристаллизация воды, называется температурой замерзания.
Изменения температуры замерзания воды связаны с влиянием давления и/или солености. Температура, при которой вода имеет максимальную плотность, называется температурой наибольшей плотности. Она составляет 3,980С.
Увеличение солености на каждые 100/00 снижает температуру наибольшей плотности примерно на 20С. Соотношения между температурами наибольшей плотности и замерзания влияют на характер процесса охлаждения воды и вертикальной конвекции.
Задание 1. С помощью круговой диаграммы и прямоугольника Роджерса (рис. 1, А, Б) представить химический состав воды, приведенный в таблице 1.
Таблица 1. - Данные о химическом составе природных вод
|
Вариант |
Катионный состав, %экв. |
Анионный состав, %экв. | ||||
|
Са+2 |
Mg+2 |
Na++K+ |
HCO3- |
SO4-2 |
Cl- | |
|
1 |
80 |
10 |
10 |
60 |
25 |
15 |
|
2 |
66 |
30 |
4 |
57 |
21 |
22 |
|
3 |
12 |
49 |
39 |
22 |
63 |
15 |
|
4 |
4 |
70 |
26 |
30 |
70 |
- |
|
5 |
42 |
42 |
16 |
33 |
42 |
25 |
|
6 |
- |
17 |
83 |
61 |
17 |
22 |
|
7 |
75 |
25 |
- |
44 |
56 |
- |
|
8 |
29 |
42 |
29 |
14 |
72 |
14 |
|
9 |
55 |
- |
45 |
15 |
10 |
75 |
|
10 |
20 |
25 |
55 |
25 |
40 |
35 |
|
“б” |
5 |
90 |
5 |
5 |
5 |
90 |
Методические указания.
Для показа химического состава воды на круговой диаграмме (рис. 1, А) следует разделить окружность на две равные части горизонтальной линией, проходящей через ее центр. В верхней части полукруга показать катионный состав, в нижней – анионный.
Каждое из полукружий разбить на три части пропорционально процентному составу катионов и анионов. Следует помнить, что 100% катионов или анионов на диаграмме соответствуют 1800 или 1% - 1,80.
Выделенные на диаграмме сектора заштриховать согласно самостоятельно разработанной легенде.
При построении прямоугольника Роджерса в первом и третьем столбцах расположить катионы и анионы снизу вверх в последовательности, определяемой относительной реактивной силой (рис. 1, Б).
Во втором столбце прямоугольника Роджерса указать состав солей в воде, выписать их процентное содержание.
Задание 2. С помощью графика Дурова (рис. 1, В) определить химический состав смеси, образующейся при смешивании воды «а» (один из вариантов таблицы 1) с водой «б» (табл. 1) в пропорции 1:1.
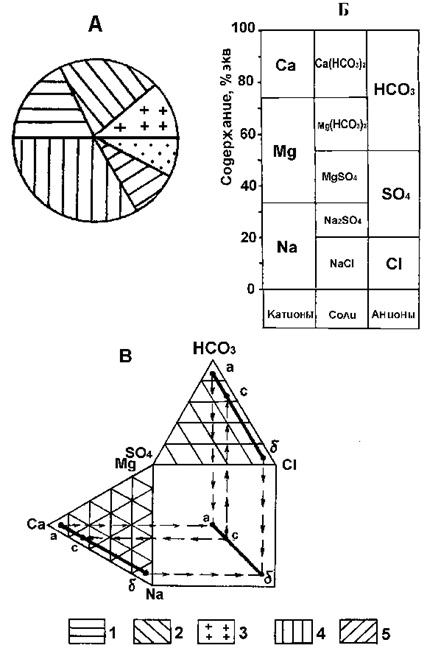
Рис. 1. Графические методы показа химического состава воды
А – круговая диаграмма, Б – прямоугольник Роджерса, В – график Дурова. Катионы: 1 – Са, 2 – Mg, 3 – Na+K. Анионы: 4 – HCO3, 5 – SO4, 6 – Cl
Методические указания.
Построить на миллиметровке макет графика Дурова (рис. 1, В).
На катионном и анионном треугольниках определить местоположение точек «а», соответствующих химическому составу воды выбранного варианта.
Спроецировать положения точек на квадрат путем проведения горизонтального пунктира из катионного и вертикального пунктира из анионного треугольников.
Аналогично определить на квадрате положение точки «б».
Исходя из пропорции смешивания 1:1 найти положение точки «с» (смеси вод «а» и «б»), для чего соединить «а» и «б» отрезком и разделить его пополам.
Из точки «с» провести пунктирные проекции на отрезки «а-б» в катионном и анионном треугольниках и определить химический состав полученной смеси, выписав в тетради процентное содержание основных ионов.
Задание 3. По данным таблицы 3 построить график изменения температуры замерзания и температуры наибольшей плотности воды в зависимости от солености и проанализировать его, объяснив различия в ходе замерзания пресной и соленой воды.
Таблица 3 - Данные для построения графика Хелланд - Хансена
|
Соленость, S, 0/00 |
0 |
5 |
10 |
15 |
20 |
25 |
30 |
35 |
|
Температура замерзания, tз, 0С |
0,00 |
-0,27 |
-0,54 |
-0,81 |
-1,08 |
-1,35 |
-1,62 |
-1,89 |
|
Температура наибольшей плотности, tп, 0С |
3,98 |
2,93 |
1,85 |
0,77 |
-0,30 |
-1,37 |
-2,45 |
-3,53 |
Методические указания.
На оси абсцисс отложить значения солености, на оси ординат – температуры замерзания и наибольшей плотности. Масштабы выбрать самостоятельно.
По данным таблицы 3 отстроить точки и провести через них прямые. Найти координаты точки пересечения прямых.
Показать на графике область распространения пресных, солоноватых и соленых морских вод.
Используя материалы учебника [13, с.25, 28-35] и лекционный материал объяснить различия в ходе замерзания солоноватых и соленых морских вод, изложив их в тетради.
