- •1. Стратегия развития отечественной энергетики.
- •2. Методы определения потребностей промышленных предприятий в теплоте пара и горячей воды.
- •3. Выбор числа и мощности трансформаторов на подстанции. Нагрузочная способность.
- •1. Нормативно-правовая и нормативно-техническая база энергосбережения.
- •2. Системы отопления, вентиляции, горячего водоснабжения и пароснабжения предприятий. Их назначение. Режимы работы. Требуемые параметры тепла.
- •2.5. Паровые системы теплоснабжения
- •3. Выбор электрических аппаратов, изоляторов, электрических проводов по условиям рабочего (нормального) режима.
- •1. Энергетические обследования и энергоаудит объектов теплоэнергетики и теплотехнологий: задачи, виды, нормативная база.
- •2. Суточные и сменные графики теплопотребления. Методика определения максимальных, средних и годовых потребностей в теплоте каждым типом потребителей.
- •3. Выбор электрических аппаратов.
- •1. Двухобмоточные трансформаторы, особенности, схемы замещения.
- •2. Методы регулирования отпуска теплоты из систем централизованного теплоснабжения.
- •3. Энергосбережение в котельных.
- •1. Защита линий электрических сетей от токов коротких замыканий.
- •2. Изоляционные конструкции теплопроводов. Методика их теплового расчета. Определение тепловых потерь участка тепловой сети и падения температур теплоносителя по их длине.
- •3. Сушильные установки: назначение, устройство и принцип работы.
- •1. Защита от атмосферного электричества сельскохозяйственных предприятий.
- •2. Котельные - основной источник генерации теплоты в системах теплоснабжения. Производственные и отопительные котельные. Их назначение и области рационального использования.
- •3. Теплообменные аппараты: назначение, классификация и принцип работы.
- •1. Классификация, свойства и характеристики теплоносителей.
- •2. Классификация и параметры паровых и водогрейных котельных. Принцип выбора основного и вспомогательного оборудования.
- •3. Кабельные линии, конструкции, преимущества.
- •1. Магистральные и радиальные схемы электроснабжения сельскохозяйственных предприятий.
- •Энергетические, экологические и экономические показатели котельных.
- •3. Как проводится консервация котла и выполняется защита от стояночной коррозии?
- •1. Проектирование проводок в производственных и общественных зданиях.
- •2. Назначение и классификация тэц, используемых в системах теплоснабжения. Принципиальные тепловые схемы тэц.
- •3. Виды и краткая характеристика потерь энергии и ресурсов в тепловых сетях.
- •1. Приемники электрической энергии, их основные характеристики.
- •2. Коэффициент теплофикации и определение его оптимального значения. Использование пиковых водогрейных котлов.
- •3. Энергосбережение на тэц промышленных предприятий.
- •1. Закон Фурье; коэффициент теплопроводности. Термическое сопротивление теплопроводности.
- •2. Вторичные энергоресурсы промпредприятий, используемые для генерации теплоты. Их количество, параметры, доля полезного использования в системах теплоснабжения.
- •3. Выбор сечения проводниковой арматуры (проводов, кабелей и шин) в электрических сетях.
- •1. Теплопроводность через плоские, цилиндрические, 1-слойные и многослойные стенки.
- •2. Компрессорные машины. Назначение, область применения.
- •3. Воздушные линии с расщепленными фазами.
- •1. Теплопередача через плоские и цилиндрические стенки. Термическое сопротивление теплопередачи через плоские и цилиндрические стенки. Коэффициент теплопередачи; интенсификация теплопередачи.
- •Цилиндр стенки
- •2. Детандер. Классификация, назначение, схема поршневого детандера.
- •3. Виды электрических сетей.
- •1. Лучистый теплообмен; законы Планка, смещения Вина, Стефана-Больцмана. Степень черноты тела; закон Кирхгофа и следствие из него.
- •2. Рабочий процесс газотурбинных установок (гту).
- •3. Надежность электроснабжения сельских потребителей.
- •1. Теплообменные аппараты. Уравнения теплового баланса и теплопередачи; средняя разность температур между теплоносителями. Расчет прямоточных и противоточных теплообменников.
- •12.5.Конструкторский и поверочный расчёт теплообменных аппаратов
- •2. Классификация газотурбинных установок.
- •3. Холодильные установки: назначение, устройство и принцип работы.
- •1. Режим работы сети электроснабжения с глухозаземленной нейтралью с напряжением до 1000в
- •2. Паровые турбины и их классификация.
- •3. Ректификационные установки: назначение, устройство и принцип работы.
- •1. Свободная и вынужденная конвекции; физические свойства жидкостей. Числа (критерии) подобия конвективного теплообмена.
- •2. Назначение, роль и место тепловых двигателей и нагнетателей.
- •3. Автоматизация и дистанционные управления – как средство повышения безопасности труда.
- •1. Параметры состояния газа. Уравнение состояния идеального газа. Первый закон термодинамики. Основные процессы идеального газа.
- •2. Абсорбционные установки: назначение, устройство и принцип работы.
- •3. Технические средства безопасности, виды и защита работающих.
- •1. Различия между идеальным газом и реальными газами. Фазовые переходы. Основные процессы с водяным паром. Использование водяного пара в технике.
- •2. Выпарные аппараты: назначение, устройство и принцип работы.
- •3. Методы анализа травматизма и заболеваемости. Их показатели и прогнозирование.
- •1. Газовые смеси. Влажный воздух и его параметры. Изображение на h-d диаграмме процессов сушки в конвективной сушилке и кондиционирования воздуха.
- •2. Качество электрической энергии.
- •3. Требования безопасности к конструкции и эксплуатации сосудов, работающих под давлением.
- •1. Мероприятия по снижению потерь мощности и электроэнергии.
- •2. Равновесие капельной жидкости, движущейся прямолинейно и вращающейся вокруг вертикальной оси.
- •3.8. Равномерное вращение сосуда с жидкостью
- •3. Требования безопасности к конструкции и эксплуатации теплотехнического оборудования.
- •1. Построение годового графика активной мощности.
- •2. Теория физического подобия. Три теоремы теории подобия. Критерии гидродинамического подобия.
- •3. Регенеративные аппараты: назначение, устройство и принцип работы.
- •1. Регулирование напряжения в электрических сетях.
- •2. Виды и образование скачков уплотнений. Уравнения скачков уплотнений.
- •3. Рекуперативные аппараты: назначение, устройство и принцип работы.
- •1. Общие принципы энергосбережения в зданиях и сооружениях.
- •1 Бытовое энергосбережение
- •2 Структура расхода тепловой и электрической энергии зданиями
- •3 Тепловая изоляция зданий и сооружений
- •4 Совершенствование теплоснабжения. Тепловая изоляция трубопроводов.
- •5 Изоляционные характеристики остекления и стеклопакеты
- •2. Уравнение Бернулли для элементарной струйки идеальной жидкости. В чем состоит геометрический и энергетический смысл уравнения Бернулли.
- •3. Назовите основные задачи обслуживания паровых и водогрейных котлов.
- •1. Учет энергоресурсов: принципы и требования, предъявляемые к приборам учета тепловой и электрической энергии.
- •2. Поясните основные характеристики газовых потоков: число Маха, коэффициент скорости. Безразмерную скорость.
- •3. Назовите перечень работ выполняемых во время текущего и капитального ремонтов котельных агрегатов.
- •1. Смесительные аппараты: назначение, устройство и принцип работы.
- •2. Потери мощности и электрической энергии в системах электроснабжения.
- •3. Назовите порядок выполнения планового останова котельного агрегата.
1. Параметры состояния газа. Уравнение состояния идеального газа. Первый закон термодинамики. Основные процессы идеального газа.
По роли отдельных тел, входящих в термодинамическую систему, их делят на рабочие тела (РТ), источники теплоты (ИТ) и объекты работы (ОР).
Рабочими телами являются, как правило, газообразные вещества - газы и пары, которые способны значительно изменять свой объём при изменении внешних условий.
В тех состояниях, когда можно пренебречь влиянием сил взаимодействия между молекулами и объёмом самих молекул (сильно нагретый газ при небольших давлениях), газ называют идеальным. В противном случае газ называется реальным.
Рабочее тело в тепловой машине получает или отдаёт теплоту, взаимодействуя с более нагретыми или более холодными внешними телами. Такие тела носят название источников теплоты.
Совокупность физических свойств системы в рассматриваемых условиях называют термодинамическим состоянием системы.
Различают равновесное (стационарное) и неравновесное (нестационарное) состояния термодинамической системы.
Макроскопические величины (т. е. величины, которые характеризуют тело в целом), характеризующие физические свойства тела в данный момент, называются термодинамическими параметрами состояния. Последние разделяются на интенсивные (не зависящие от массы тела) и на экстенсивные (пропорциональные массе тела).
К основным параметрам состояния, поддающимся непосредственному измерению простыми техническими средствами, относятся абсолютное давление , удельный объём и абсолютная температура . Эти три параметра носят название термических параметров состояния.
К параметрам состояния относятся также внутренняя энергия , энтальпия и энтропия , которые носят название калорических параметров состояния.
Равновесным состоянием термодинамической системы называется такое состояние, которое характеризуется при постоянных внешних условиях неизменностью параметров во времени и отсутствием в системе потоков. Состояние термодинамической системы, при котором во всех ее частях температура одинакова, называют термическим равновесным состоянием.
Изолированная термодинамическая система независимо от своего начального состояния с течением времени всегда приходит в состояние равновесия. Необходимо отметить, что никогда самопроизвольно выйти из него система не может (основной постулат термодинамики — нулевое начало).
Состояние термодинамической системы, при котором значения параметров во всех частях ее остаются неизменными во времени благодаря внешнему воздействию потоков вещества, энергии, импульса, заряда и т. п., называется стационарным. Если значения параметров изменяются во времени, то состояние термодинамической системы называется нестационарным.
Любое изменение в термодинамической системе, связанное с изменением хотя бы одного из ее параметров, называется термодинамическим процессом. Если одна система совершает работу над другой системой с помощью механических и электрических сил, то взаимодействие называется механическим. Взаимодействие, которое приводит к изменению энергии и совершается в форме передачи теплоты посредством теплопроводности или тепловой радиации, называется тепловым. Взаимодействие, приводящее к изменению энергии и совершаемое в форме передачи массы, называется массообменным.
Давление — физическая величина, численно равная отношению нормальной составляющей силы к площади, на которую действует эта сила.
Единицей давления в СИ является паскаль — давление, вызываемое силой в 1 Н, равномерно распределенной по поверхности площадью 1 м2 (1Па=1 Н/м2). Часто приходится измерять давление высотой столба какой-либо жидкости (воды, ртути и др.).
Различают атмосферное, или барометрическое, давление Рб, абсолютное давление Ра , манометрическое, или избыточное Ризб, разрежение, или вакуум.
Давление, создаваемое атмосферным воздухом, называется барометрическим, или атмосферным.
Абсолютным давлением называется давление, отсчитываемое от нуля (абсолютного вакуума).
Избыточным, или манометрическим, давлением называется давление сверх атмосферного, то есть избыточное давление — это разность между абсолютным и барометрическим давлениями: .
Разрежением, или вакуумом, называется разность между атмосферным давлением и абсолютным давлением той среды, где измеряется давление. Если абсолютное давление газа или пара в сосуде ниже барометрического, то есть , то разность называется разрежением, или вакуумом.
Вакуум показывает, насколько давление газа (пара) меньше давления окружающей среды. Давление атмосферного воздуха измеряется барометрами, избыточное давление — манометрами, а давление разрежения — вакуумметрами.
В термодинамических уравнениях всегда используют значения абсолютного давления ввиду того, что оно является параметром, характеризующим состояние термодинамической системы.
Атмосферное давление — величина переменная, поэтому в технике применяется нормальное атмосферное давление, Ро=0.10132МПа (760 мм рт. ст.).
Температура тела есть мера его нагретости. Температура определяет направление передачи теплоты. Если два тела А и В имеют соответственно температуру Т1 и Т2 и Т1>Т2, то теплота переходит от тела А к телу В. При этом температура тела А уменьшается, а тела В - увеличивается.
С точки зрения молекулярно-кинетической теории температура есть мера интенсивности теплового движения молекул.
В термодинамике рассматривают температуру как среднестатистическую величину, которая характеризует систему, состоящую из очень большого числа молекул (частиц), находящихся в хаотическом (тепловом) движении. Поэтому к единичным молекулам понятие температуры не применимо. При температуре абсолютного нуля тепловое движение молекул отсутствует. Эта предельная минимальная температура называется абсолютным нулем и является началом для отсчета температур. Понятно, что не может быть Т<0 , то есть абсолютная температура всегда положительна.
Температура, отсчитываемая от абсолютного нуля, называется абсолютной, а шкала температур называется шкалой Кельвина.
Практически измерять кинетическую энергию молекул газа непосредственно невозможно. Поэтому для измерения температуры используют различные косвенные методы. Температура измеряется при помощи различных термодинамических устройств - термометров).
Использование термометров основано на том факте, что два соприкасающихся тела с разными температурами через некоторое время приходят к состоянию теплового равновесия и принимают одинаковую температуру.
Численный отсчет температуры производится по шкале температур. За основную единицу измерения температуры принимают градус, имеющий разную величину в различных температурных шкалах. Шкала температур устанавливается путем деления разности показаний термометра в двух произвольно выбранных постоянных температурных точках, называемых реперными или опорными, на некоторое число равных частей — градусов.
Ввиду того, что выбор постоянных температурных точек и цены деления шкалы является произвольным, имеется ряд различных шкал температуры.
В настоящее время применяются различные температурные шкалы: Цельсия, Фаренгейта, Реомюра, Ранкина.
По шкале Цельсия () приняты следующие постоянные температурные точки: О°C — температура таяния льда, 100°C — температура кипения воды при нормальном атмосферном давлении.
В 1724 г. Фаренгейт предложил термометр, в качестве реперных точек которого приняты: +212°F — температура кипения воды при нормальном атмосферном давлении; +32°F - температура таяния льда. Разность температур кипения воды и таяния льда по шкале Фаренгейта равна 212°— 32° = 180 °F, а по шкале Цельсия — 100°C. Следовательно, 1°F соответствует 5/9 °C, а 1°C — 1,8°F.
Шкала Реомюра () имеет следующие реперные точки: О°R — температура таяния льда, 80°R — температура кипения воды при нормальном атмосферном давлении.
Шкала Ранкина () — это шкала Фаренгейта, отсчитанная от абсолютного нуля. В этой шкале температура таяния льда (T0=273,15 К) соответствует 491,67°Ra, а температура кипения воды при нормальном атмосферном давлении (T0=373,15 К) соответствует 671,67°Ra.
Решением Международного комитета мер и весов приняты две шкалы: термодинамическая температурная шкала, которая принята основной, и Международная практическая температурная шкала (МПТШ-68), выбранная таким образом, чтобы температура, измеренная по этой шкале, была близка к термодинамической. В основу построения термодинамической шкалы положен тот факт, что в циклах Карно, располагающихся между двумя адиабатами, разность температур изотерм считается постоянной, если в механическую работу превращаются одинаковые количества теплоты. Наиболее универсальной шкалой температур является абсолютная термодинамическая шкала температур — шкала Кельвина.
В шкале Кельвина используется единственная экспериментальная реперная точка — тройная точка химически чистой воды (в термодинамическом равновесии находятся три агрегатных состояния; лед, жидкая вода и пар). Этому состоянию соответствует температура 273,15К (0,01°С). Второй постоянной точкой является абсолютный нуль температур (0К). Кельвин — единица измерения температуры по термодинамической температурной шкале, равная 1/273,15 части интервала от абсолютного нуля температуры до температуры тройной точки воды.
Практическим осуществлением термодинамической шкалы температур является Международная практическая температурная шкала. В этой шкале используется одиннадцать реперных точек. В табл. 1.2 приведены значения основных реперных точек.
Удельный объем вещества — это объем, занимаемый единицей массы данного вещества.
Плотность вещества — величина, обратная удельному объему и определяющая количество вещества, заключенное в единице объема.
Единица плотности в СИ — кг/м3, в системе СГС — г/см3. Плотность и удельный объем зависят от температуры и давления, то есть от термодинамического состояния вещества. Обычно в справочниках приводятся их значения при нормальных физических условиях. За нормальные физические условия принимают давление, равное 101,325 кПа (760 мм рт. ст.), и температуру, равную О °С.
Количество вещества. Единицей количества вещества в СИ является моль. Кроме моля применяют кратные и дольные части от моля (кмоль, Ммоль и др.). Количество вещества — это физическая величина, определяемая числом структурных элементов (атомов, молекул, ионов, электронов). Моль равен количеству вещества системы, содержащей столько же структурных элементов, сколько содержится атомов в углероде-12 массой 0,012 кг.
Молярной массой вещества называют отношение массы вещества к его количеству:
![]()
где μ — молярная масса. Если выразить в кг, — в молях, μ — выразится в кг/моль.
Плотность вещества – величина, определяемая отношением массы к объему вещества.
ρ = m / V , [кг/м3] , (1.2) υ = 1 / ρ ; ρ = 1 / υ ; υ • ρ = 1
Законы идеальных газов
Закон Бойля-Мариота
Бойль в 1662 году и Мариот в 1676 году обнаружили, что при Т=const? Pv=const.
Закон Гей-Люссака
Гей-Люссак в 1802 году опытным путём установил, что при p=const v/T=const
Закон Авогадро
В 1811 году Авогадро выдвинул гипотезу: одинаковые объёмы различных газов при одинаковых физических условиях содержат одинаковые количества молекул. Эта гипотеза, став после её доказательства законом, приводит к одному важному следствию, согласно которому при одинаковых физических условиях для любых газов произведение молекулярной массы газа на его удельный объём есть величина постоянная, т. е. .
µν=const
Напомним, что молекулярной массой называется количество вещества в граммах, численно равное его молекулярной массе. Например, молекулярная масса углерода равна 12 граммам, а кислорода - 32 граммам.
Произведение µν
= ![]() представляет собой объём одного моля
газа, который при нормальных физических
условиях равен 22,4 м3.
представляет собой объём одного моля
газа, который при нормальных физических
условиях равен 22,4 м3.
Отметим, что нормальным физическим условиям соответствуют 760 мм рт. ст. и 00С, а нормальным техническим условиям - 735 мм рт. ст. и 100С.
Уравнение состояния
Сопоставление законов Бойля-Мариота и Гей-Люссака приводят к обобщённому закону Бойля-Гей-Люссака: ,
Pν/T=R
где R - характеристическая постоянная идеального газа (при нормальных физических условиях
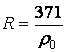
![]() ,
где ρ0
- плотность при нормальных физических
условиях).
,
где ρ0
- плотность при нормальных физических
условиях).
Это уравнение, полученное Клайпероном в 1834 году, называется уравнением состояния идеальных газов или уравнением Клайперона.
Первый закон термодинамики.
Первый закон термодинамики является основой термодинамической теории и имеет огромное прикладное значение при исследовании термодинамических процессов. Этот закон является законом сохранения и превращения энергии: ¦"Энергия не исчезает и не возникает вновь, она лишь переходит ¦из одного вида в другой в различных физических процессах". Для термодинамических процессов закон устанавливает взаимосвязь между теплотой, работой и изменением внутренней энергии т/д системы: ¦"Теплота, подведенная к системе, расходутся на изменение энергии ¦системы и совершение работы". Уравнение первого закона термодинамики имеет следующий вид:
Q = (U2 – U1) + L , (2.1)
где Q - количества теплоты подведенная (отведенная) к системе; L - работа, совершенная системой (над системой); (U2 – U1) - изменение внутренней энергии в данном процессе. Если: Q > 0 – теплота подводится к системе; Q < 0 – теплота отводится от системы; L > 0 –работа совершается системой; L < 0 – работа совершается над системой. Для единицы массы вещества уравнение первого закона термодинамики имеет вид:
q = Q /m = (u2 – u1) + l .
Термодинамические процессы: изохорный, изобарный, изотермический, адиабатный, политропный
Изохорный процесс (v=const)
 Такой
процесс может совершаться рабочим
телом, находящимся в цилиндре при
неподвижном поршне, если к рабочему
телу подводится теплота от источника
теплоты (см. рис. 4.1) или отводится теплота
от рабочего тела к холодильнику. При
изохорном процессе выполняется условие
dv=0 или v=const. Уравнение изохорного процесса
получим из уравнения состояния идеального
газа (см. &1.6) при v=const. В pv-координатах
график процесса представляет собой
прямую линию, параллельную оси p. Изохорный
процесс может протекать с повышением
давления (процесс 1-2) и с понижением
(процесс 1-2’)
Такой
процесс может совершаться рабочим
телом, находящимся в цилиндре при
неподвижном поршне, если к рабочему
телу подводится теплота от источника
теплоты (см. рис. 4.1) или отводится теплота
от рабочего тела к холодильнику. При
изохорном процессе выполняется условие
dv=0 или v=const. Уравнение изохорного процесса
получим из уравнения состояния идеального
газа (см. &1.6) при v=const. В pv-координатах
график процесса представляет собой
прямую линию, параллельную оси p. Изохорный
процесс может протекать с повышением
давления (процесс 1-2) и с понижением
(процесс 1-2’)
Политропный процес
Политропным процессом называется любой произвольный процесс изменения состояния рабочего тела, происходящий при постоянной теплоёмкости сп.
В политропном процессе dq=cп·dT.
Для получения
графика политропного процесса в p-v
координатах будем придерживаться тех
же рассуждений, что и при получении
графика адиабатного процесса. Заменим
в соотношениях, полученных при изучении
адиабатного процесса, обозначение
теплоёмкости с на сп и обнаружим, что
p·vn=const, а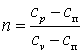
|
|
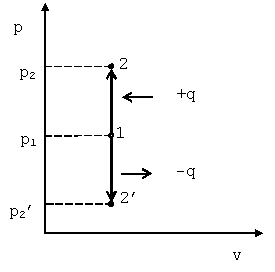
Изотермический процесс (T=const
В p-v координатах график процесса изображается равнобокой гиперболой (рис. 4.3). Изотермический процесс может протекать как с увеличением объёма (процесс 1-2), так и с уменьшением объёма (процесс 1-2’).
|

Адиабатный процесс
Адиабатный процесс – это процесс, при котором рабочее тело не обменивается теплотой с окружающей средой (dq=0). Для получения графика процесса в p-v координатах выполним некоторые преобразования.
В соответствии с первым законом термодинамики dq=cv·dT+p·dv=c·dT, где с – теплоёмкость термодинамического процесса.