
- •119 Общие вопросы аналитической химии раздел 1
- •Глава 1
- •1.1. Предмет аналитической химии
- •1.2. Принцип, метод и методика анализа
- •1.3. Виды анализа
- •1.4. Методы аналитической химии
- •Глава 2
- •Первая аналитическая группа катионов
- •Вторая аналитическая группа катионов
- •Систематический анализ смеси Cl-, Br-, I- - ионов
- •Глава 3
- •3.2. Активность и коэффициент активности
- •Активность (a) -такая концентрация вещества в растворе, при использовании которой свойства данного раствора могут быть описаны теми же уравнениями, что и свойства идеального раствора.
- •0,100 Моль/л
- •0,100 Моль/л
- •3.4. Виды констант химического равновесия, используемые в аналитической химии в аналитической химии используются
- •3.5. Общие принципы расчёта состава равновесных систем
- •Уравнение материального баланса основано на том, что число атомов определённого элемента (или групп атомов определённого вида) в изолированной системе остаётся неизменным.
- •Глава 4
- •4.1. Важнейшие теории кислот и оснований
- •4.3. Влияние растворителя на кислотно-основные свойства растворённого вещества
- •4.4. Нивелирующее и дифференцирующее действие растворителя. Сильные и слабые кислоты и основания
- •Растворы амфолитов
- •4.6. Расчёт состава равновесных смесей протолитов при заданном значении рН
- •4.7. Кислотно-основные буферные растворы
- •Глава 5
- •5.1. Понятие о комплексном соединении
- •5.2. Классификация комплексных соединений
- •5.3. Равновесия в растворах комплексных соединений
- •Природа комплексообразователя и лигандов
- •Концентрация реагентов
- •Ионная сила
- •Температура
- •Побочные реакции
- •Глава 6
- •6.1. Произведение растворимости малорастворимого электролита
- •6.2. Растворимость
- •7,210-4Моль/л
- •6.3. Влияние различных факторов на растворимость Природа растворяемого вещества и растворителя
- •Температура
- •Ионная сила
- •Общий (одноименный) ион
- •Побочные реакции
- •6.4. Общие принципы растворения осадков малорастворимых электролитов
- •Глава 7
- •Электродные потенциалы
- •Уравнение Нернста
- •7.3. Влияние различных факторов на протекание окислительно-восстановительных реакций Температура
- •Посторонние ионы
- •Влияние рН
- •Образование малорастворимых соединений
- •7.4. Расчёт различных констант с использованием электродного потенциала
- •Глава 8
- •8.1. Отбор пробы
- •8.2. Разложение пробы
- •Глава 9
- •9.2. Жидкость - жидкостная экстракция
- •9.2.2. Экстракционные системы и экстрагенты
- •9.2.4. Влияние различных факторов на процесс экстракции
- •Слабые основания
- •Амфолиты
- •Присутствие сильных электролитов
- •Сложение и вычитание
- •Деление и умножение
- •Другие операции
- •10.2. Понятие об аналитическом сигнале
- •10.3. Методы расчёта концентрации вещества по величине аналитического сигнала
- •Метод градуировочного графика
- •Метод стандартов
- •10.4. Неопределённость и погрешности измерений
- •10.5. Некоторые основные положения математической статистики, используемые в аналитической химии
- •10.7. Основные характеристики методики анализа
- •Воспроизводимость
- •Правильность
Присутствие сильных электролитов
При добавлении к водной фазе больших количеств хорошо растворимых сильных электролитов растворимость веществ может уменьшаться (высаливание), иногда растворимость увеличивается (всаливание). При проведении экстракции в системах с высаливанием коэффициент распределения вещества увеличивается, в случае всаливания - уменьшается.
9.2.5 Способы осуществления экстракции
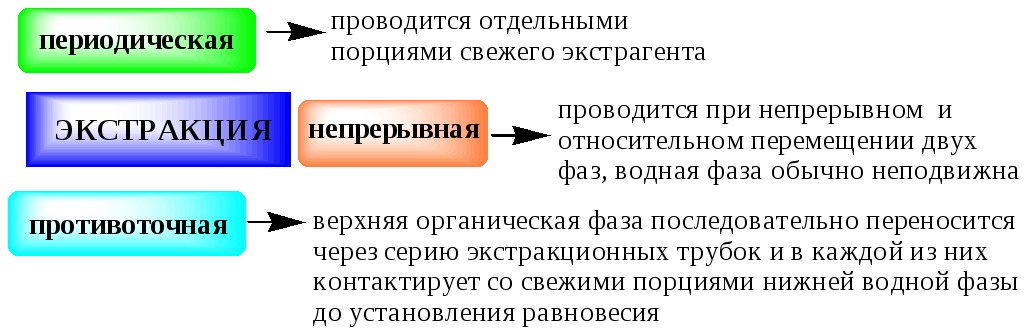
9.2.6. Применение экстракции
![]() разделение
веществ(выделение микрокомпонента,
очистка макрокомпонента);
разделение
веществ(выделение микрокомпонента,
очистка макрокомпонента);
![]() концентрирование;
концентрирование;
![]() в
гибридных методах анализа(экстракционная
фотометрия, экстракционная флуориметрия
и др.)
в
гибридных методах анализа(экстракционная
фотометрия, экстракционная флуориметрия
и др.)
![]() изучение
различных равновесий.
изучение
различных равновесий.
ГЛАВА 10

Хемометрика (хемометрия)-химическая дисциплина, которая занимается применением математических и статистических методов для планирования и выбора оптимальных условий проведения химического эксперимента и аналитического измерения, а также получения максимума информации из химических данных.
Методы хемометрики используются на всех основных этапах химического анализа.
10.1. Приближённые вычисления и значащие цифры
Некоторые из численных величин, полученных экспериментальным путём, могут быть известны абсолютно точно (например, число таблеток, взятых для анализа), другие же (объём раствора, масса навески) всегда известны с некоторой неопределённостью. Простейшим способом описания неопределённости численной величины является понятие «значащие цифры».
Значащими называют все достоверные цифры, входящие в состав численный величины, а также первую, следующую за ними, недостоверную цифру.

При определении числа значащих цифр, входящих в состав численной величины, используют следующие правила:
![]() положение
запятой не влияет на число значащих
цифр
положение
запятой не влияет на число значащих
цифр
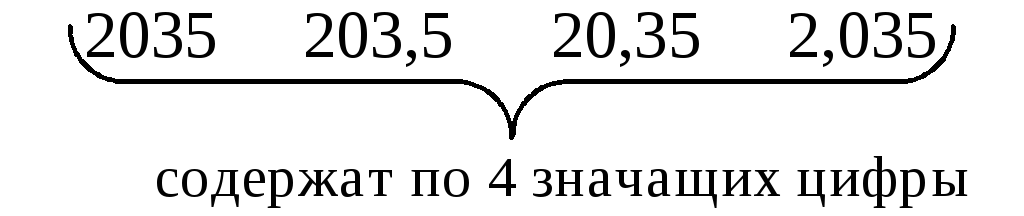
![]() нули,
входящие в состав числа, могут быть как
значимыми, так и незначимыми
нули,
входящие в состав числа, могут быть как
значимыми, так и незначимыми
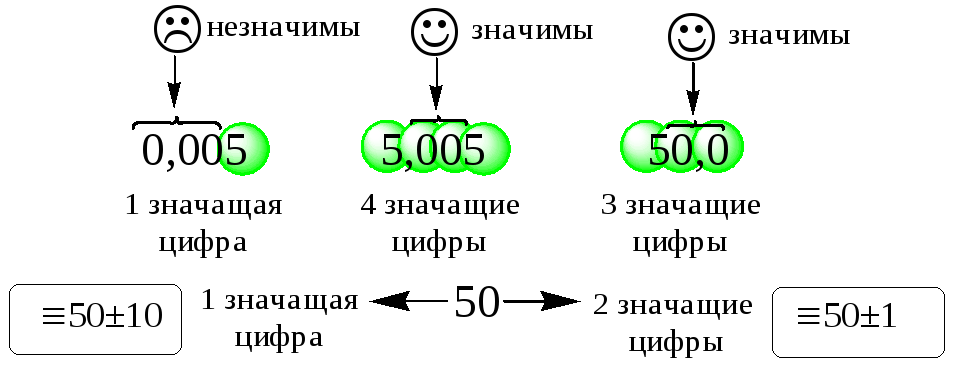
Для того чтобы избежать проблем с определением числа значащих цифр, входящих в состав недостоверно известной величины, рекомендуется используемые численные величины записывать в виде числа, все цифры которого значимы, умноженного на десять в некоторой степени. Например, 0,05 как 510-2; 0,050 как 5,010-2и т.д.
При вычислениях с использованием экспериментально полученных величин следует помнить, что в результате расчётов «точность» не должна искусственно повышаться, так как она определяется тем, с какой погрешностью измерены исходные величины, входящие в расчётную формулу. Существуют определённые правила, которые в большинстве случаев позволяют избежать ошибок при расчётах.
Сложение и вычитание
Перед проведением данных действий необходимо вначале все числа округлить до одинакового числа десятичных знаков - такого же как у числа с минимальным их количеством.
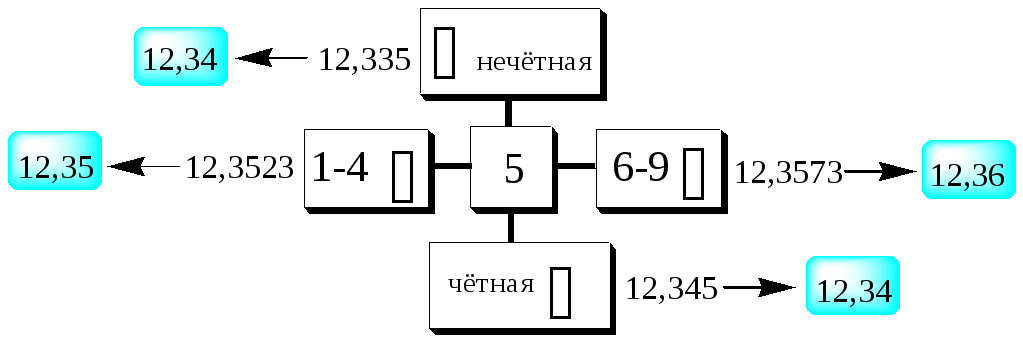
Сумма должна содержать столько же десятичных знаков, сколько этих знаков содержится у числа с наименьшим их количеством.

Возможна и другая последовательность действий: вначале проводят сложение (вычитание) неокруглённых чисел, а затем уже полученный ответ округляют до требуемого числа десятичных знаков.
При сложении или вычитании чисел, записанных в степенной форме, их вначале приводят к числу с наибольшим показателем степени, а затем поступают так же, как и для обычных чисел. Например
1,03102+ 5,2103= 0,103103+ 5,2103= 5,3103
