
22-
.pdf
Жерносек А.К. |
Фармацевтическая химия |
O
OH |
O |
|
|
|
C6H5COCl |
AcO |
|
HO |
|
|
|
|
|
O |
|
O |
OH |
|
|
|
циклогексанон |
|
изопропилат |
HO |
алюминия HO |
Свойства и контроль качества. Тестостерон, его эфиры и метил-
тестостерон являются белыми кристаллическими веществами. Практически нерастворимы в воде, хорошо растворимы в этаноле, хлороформе, метиленхлориде.
Свойства и контроль качества андрогенов аналогичны таковым у гестагенов.
Для идентификации используют ИК- и УФ-спектроскопию, ТСХ, определение физических констант (температура плавления и др.). Например, идентификацию тестостерона пропионата и метилтестостерона методом ТСХ проводят на силикагеле, ПФ – смесь безводной уксусной кислоты, петролейного эфира и бутилацетата (1:30:70), проявляют этанольным раствором серной кислоты (тестостерона пропионат) или насыщенным раствором дихромата калия в растворе серной кислоты (метилтестостерон).
Количественное определение проводят методами УФспектрофотометрии (этанольный раствор, 241 нм), спектрофотометрии с изониазидом, ВЭЖХ.
8
2011/2012
Жерносек А.К. |
Фармацевтическая химия |
ЭСТРОГЕНЫ
Эстрогены – группа стероидных гормонов, регулирующих формирование и функционирование женских половых органов и молочных желез, развитие вторичных половых признаков, некоторые стороны психофизиологического состояния организма млекопитающих, а в комплексе с гестагенами – беременность и лактацию.
По химической структуре эстрогены относятся к производным эстрана.
Me
H эстран
H H
Главными представителями эстрогенов в организме женщины являются эстрон, эстрадиол и эстриол
Вещество |
Формула |
Химическое |
эстрон |
|
название |
|
O |
|
|
|
|
|
|
3-гидроксиэстратриен-1,3,5(10)- |
|
|
-он-17 |
|
HO |
|
эстрадиол |
|
OH |
|
|
|
|
|
эстратриен-1,3,5(10)-диол-3, 17 |
|
HO |
|
эстриол |
|
OH |
|
|
OH эстратриен-1,3,5(10)-триол-3, 16 , 17
HO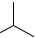
Эстрон синтезируется из дигидроэпиандростерона в яичниках (промежуточным веществом при образовании эстрона является тестостерон). Эстрадиол и эстриол образуются, главным образом, в печени и
9
2011/2012
Жерносек А.К. |
Фармацевтическая химия |
жировой ткани. Эстрогены обладают высокой биологической активностью, их концентрацияя в биологических жидкостях на несколько порядков ниже, чем у других стероидных гормонов. Наиболее активным эстрогеном является эстрадиол.
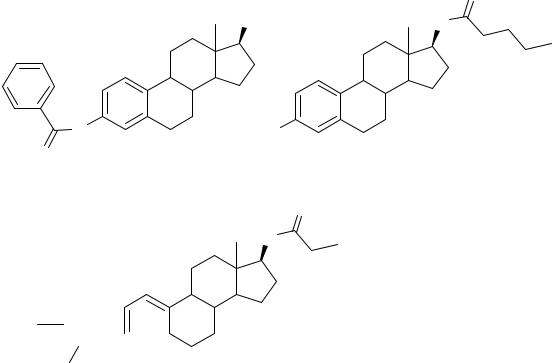
Лекарственные средства группы эстрогенов, могут быть природными и синтетическими. К природным эстрогенам относятся эстрон, эстрадиол, эстриол, которые используются в медицине в свободном виде,
атакже в виде сложных эфиров.
Вобразовании сложных эфиров могут принимать участие фенольный гидроксил или (и) спиртовой гидроксил.
O
|
OH |
O |
O |
HO |
|
O эстрадиола бензоат |
эстрадиола валерат |
|
|
O |
|
|
O |
|
эстрадиола дипропионат
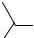 O
O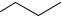

O
Необходимость получения сложных эфиров эстрадиола связана с тем, что данный гормон не может быть применён перорально, так как инактивируется при первом прохождении через печень. Сложные эфиры эстрадиола более устойчивы к действию ферментов и могут применяться перорально. Кроме того, они обладают более продолжительным действием.
Синтетические эстрогены разделяют на две подгруппы:
 соединения стероидной структуры;
соединения стероидной структуры;
 синтетические аналоги эстрогенов нестероидной структуры. К стероидным синтетическим эстрогенам относятся этинилэстра-
синтетические аналоги эстрогенов нестероидной структуры. К стероидным синтетическим эстрогенам относятся этинилэстра-
диол и его метиловый эфир – местранол. Данные соединения применяют перорально.
10
2011/2012
Жерносек А.К. |
Фармацевтическая химия |
OH |
OH |
||
|
|
|
|
|
|
|
|
|
|
|
|
HO |
H3CO |
этинилэстрадиол |
местранол |
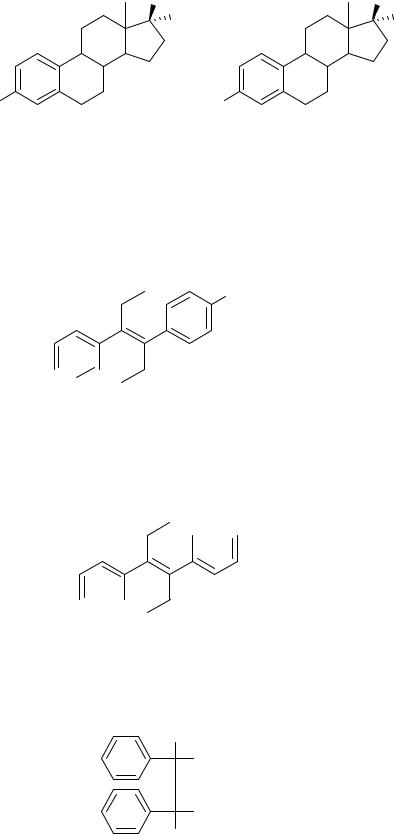
В группу нестероидных синтетических аналогов эстрогенов входят диэтилстильбэстрол, фосфэстрол, синэстрол (гексэстрол) и другие соединения, пространственная структура которых похожа на структуру природных эстрогенных гормонов.
Диэтилстильбэстрол является производным стильбена. Фармакологичекую активность проявляет только Е-изомер.
OH
диэтилстильбэстрол
HO
(E)-3,4-бис-(4-гидроксифенил)-гексен-3, ’-диэтил-(E)-4,4’-стильбендиол
Диэтилстильбэстрол мало растворим в воде и используется в виде масляного раствора. Растворимой формой данного вещества является фосфэстрол-натрий

 OPO3Na2
OPO3Na2
фосфэстрол-натрий
Na2O3PO
Гексэстрол (синэстрол) отличается от диэтилстильбэстрола отсутствием двойной связи. В молекуле данного вещества имеется два центра хиральности. В качестве лекарственного средства используется мезоформа.
C2H5
H
синэстрол
H C2H5
мезо-3,4-бис-(4-гидроксифенил)-гексан
11
2011/2012
Жерносек А.К. |
Фармацевтическая химия |
Способы получения. Эстрогенные гормоны могут быть получены различными способами:
 выделение из мочи жеребцов;
выделение из мочи жеребцов;
 химическая модификация 17-бензоата дигидроэпиандростеро-
химическая модификация 17-бензоата дигидроэпиандростеро-
на;
 сочетание химической и биохимической модификации стероидных соединений, например холестерина.
сочетание химической и биохимической модификации стероидных соединений, например холестерина.
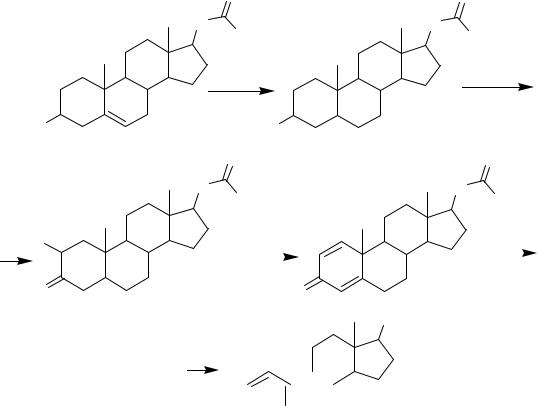
При получении эстрогенов из 17-бензоата дигидроэпиандростерона протекают следующие химические реакции
|
|
O |
|
O |
|
|
O |
C6H5 |
O |
|
C6H5 |
|
|
|
|
||
|
|
H2/Pt |
|
1) CrO3 |
|
|
|
|
|
2) Br2 |
|
HO |
|
HO |
|
|
|
|
|
O |
|
|
O |
|
O |
C6H5 |
|
O |
C6H5 |
|
|
|
|
||
Br |
|
коллидин |
|
|
1) OH- |
|
|
|
|
|
2) |
O |
|
|
O |
|
|
|
|
|
OH |
|
|
HO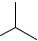
12
2011/2012

|
Жерносек А.К. |
|
|
|
|
|
|
Фармацевтическая химия |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
Вещество |
|
Идентификация |
|
Чистота |
|
|
Количественное |
|||
|
Прогестерон |
|
ИК |
Удельное вращение; СПр – ВЭЖХ; |
СФМ (96% этанол, 241 нм, 535) |
|
|||||
|
|
|
ТСХ |
Потеря в массе при высушивании |
|
|
|
||||
|
Норэтистерон |
|
ИК |
Удельное вращение; СПр – ВЭЖХ; |
алкалиметрия (тетрагидрофуран; |
|
|||||
|
|
|
|
|
Потеря в массе при высушивании |
0,1 М AgNO3; 0,1 M NaOH, потен- |
|
||||
|
|
|
|
|
|
|
|
|
циометрическое обнаружение КТТ) |
|
|
|
Левоноргестрел |
|
ИК |
Удельное вращение; СПр – ТСХ; |
алкалиметрия (тетрагидрофуран; |
|
|||||
|
|
|
удельное вращение |
Потеря в массе при высушивании |
0,1 М AgNO3; 0,1 M NaOH, потен- |
|
|||||
|
|
|
|
|
Сульфатная зола |
|
циометрическое обнаружение КТТ) |
|
|||
|
Медроксипрогестерона ацетат |
ИК |
Удельное вращение; |
|
СФМ (96% этанол, 241 нм, 420) |
|
|||||
|
|
|
|
|
Примесь 4,5- |
|
|
|
|
||
|
|
|
|
|
дигидромедроксипрогестерона ацетата |
|
|
|
|||
|
|
|
|
|
СПр – ВЭЖХ |
|
|
|
|
||
|
|
|
|
|
Потеря в массе при высушивании |
|
|
|
|||
|
Дидрогестерон |
|
ИК |
Поглощение света |
|
СФМ (метанол, 286 нм, 845) |
|
||||
|
|
|
ТСХ |
Температура плавления: 167–171 ºС |
|
|
|
||||
|
|
|
|
|
Удельное вращение |
|
|
|
|
||
|
|
|
|
|
СПр – ГЖХ |
|
|
|
|
||
|
|
|
|
|
Потеря в массе при высушивании |
|
|
|
|||
|
|
|
|
|
Сульфатная зола |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||
|
Вещество |
|
Внешний |
|
|
|
|
Растворимость |
|||
|
|
|
вода |
этанол |
|
метиленхлорид |
|
другие |
|||
|
|
|
вид |
|
|
|
|||||
|
Прогестерон |
|
|
|
|
|
|
|
|
|
|
|
Белый или почти белый кристалличе- |
|
ПрН |
Л |
|
|
|
У в ацетоне и жирных маслах |
|||
|
|
ский порошок или бесцветные кри- |
|
|
|
|
|
|
|
|
|
|
Норэтистерон |
сталлы. Обладает полиморфизмом |
|
|
|
|
|
|
|
|
|
|
Кристаллический порошок от белого |
|
ПрН |
У (безвод- |
|
Р |
|
У в ацетоне |
|||
|
Левоноргестрел |
до желтовато-белого цвета |
|
|
ный) |
|
|
|
|
|
|
|
Белый или почти белый кристалличе- |
|
ПрН |
М |
|
У |
|
|
|
||
|
Медроксипрогестерона |
ский порошок |
|
|
|
|
|
|
|
|
|
|
Белый или почти белый кристалличе- |
|
ПрН |
У |
|
Л |
|
Р в ацетоне |
|||
|
ацетат |
ский порошок |
|
|
|
|
|
|
|
|
|
|
Дидрогестерон |
Белый или почти белый кристалличе- |
|
ПрН |
У |
|
|
|
Р в ацетоне, У в метаноле, М в эфи- |
||
|
|
ский порошок |
|
|
|
|
|
|
ре |
||
2011/2012
Жерносек А.К. |
Фармацевтическая химия |
Внешний вид и растворимость. Лекарственные вещества из группы гестагенов являются белыми либо почти белыми (желтовато-белыми) кристаллическими веществами. Они практически нерастворимы в воде, в той или иной степени растворимы в этаноле, растворимы в неполярных растворителях.
Идентификацию лекарственных веществ из группы гестагенов проводят спектрометрическими (ИК, определение удельного вращения) и хроматографическими (ТСХ) методами.
Применение ТСХ для идентификации и контроля чистоты гестагенов
Вещество |
Тест |
НФ |
ПФ |
Проявитель |
|
|
|
|
|
Прогестерон) |
идентифика- |
СГ F254 |
этилацетат – метилен- |
этанольный раствор |
|
ция |
|
хлорид (33:66) |
H2SO4 |
Левоноргестрел |
сопутствую- |
CГ |
этилацетат – метилен- |
этанольный раствор |
|
щие примеси |
|
хлорид (20:80) |
фосфомолибдено- |
|
|
|
|
вой кислоты |
Медроксипро- |
примесь 4,5- |
CГ |
тетрагидрофуран – 1,1- |
этанольный раствор |
гестерона аце- |
дигидромед- |
|
диметилэтилэтиловый |
толуолсульфоновой |
тат |
роксипроге- |
|
эфир – гептан |
кислоты |
|
стерона ацета- |
|
(10:45:45) |
|
|
та |
|
|
|
Дидрогестерон |
|
Кизельгур, |
циклогексан - петро- |
этанольный раствор |
|
|
импрегниро- |
лейный эфир (1:1) |
H2SO4 |
|
|
ванный сме- |
|
|
|
|
сью пропан- |
|
|
|
|
диола-1,2 и |
|
|
|
|
ацетона (1:9) |
|
|
Чистота. Для большинства кортикостероидов определяют удельное вращение, сопутствующие примеси и потерю в массе при высушивании.
Прогестерон является правовращающим соединением. Среди полусинтетических гестагенов есть как правовращающие, так и левовращающие вещества, причём производные прогестерона в основном вращают плоскость поляризации света вправо, а производные тестостерона и 19нортестостерона – влево. Энантиомеры могут обладать различной биологической активностью. Например, левоноргестрел – левовращающий энантиомер норгестрела более активен, чем правовращающий.
Величины удельного вращения кортикостероидов
Вещество |
Растворитель |
[ ]20D |
|
|
|
(концентрация, г/л) |
|
|
|
Прогестерон |
этанол (10) |
от +186 до |
+194 |
|
Норэтистерон |
ацетон (10) |
от -32 |
до |
-37 |
Левоноргестрел |
хлороформ (20) |
от -30 |
до |
-35 |
Медроксипрогестерона ацетат |
ацетон (10) |
от +47 |
до |
+53 |
Дидрогестерон |
1,4-диоксан |
от -446 |
до |
-464 |
Условия определения сопутствующих примесей (НФ везде С18-СГ) |
|
||
|
|
|
|
Вещество |
ПФ |
|
Детекция, |
|
|
|
нм |
Прогестерон |
вода – ацетонитрил (градиентное элюирование) |
|
241 |
Норэтистерон |
вода – ацетонитрил (градиентное элюирование) |
|
254 и 210 |
Медроксипрогестерона |
тетрагидрофуран – ацетонитрил – вода |
|
254 |
ацетат |
(10:23:65) |
|
|
Медроксипрогестерона |
тетрагидрофуран – ацетонитрил – вода |
|
254 |
ацетат |
(10:23:65) |
|
|
2011/2012

Жерносек А.К. |
Фармацевтическая химия |
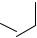
Количественное определение. Производные прогестерона в субстанции определяют методом УФ-спектрофотометрии. В зависимости от способности поглощать электромагнитное излучение ближнего УФ-диапазона гестагены можно разделить не 3 группы. К первой группе относятся гестагены-пролекарства, у которых отсутствует оксогруппа в 3-м положении (например, линестренол). Данные вещества практически не поглощают излучение с длиной волны более 200 нм. Ко второй, наиболее многочисленной группе, относятся гестагены, в молекулах которых содержится фрагмент (1). Такие вещества (прогестерон, норэтистерон, медроксипрогестерона ацетат) имеют максимум поглощения при длине волны около 240 нм. Представители третьей группы (дидрогестерон) содержат в молекуле фрагмент (2) и имеют максимум поглощения при 285 – 290 нм
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
(1) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(2) |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
Поглощение УФ-излучения гестагенами |
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||
Вещество |
макс |
|
1% |
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
A1см |
|
|
||||||||||
Прогестерон |
241 |
|
|
|
|
|
|
535 |
|
|
|
|
16800 |
||||||||||||||||||||||||||||||||||||||||||
Медроксипрогестерона ацетат |
241 |
|
|
|
|
|
|
420 |
|
|
|
|
16200 |
||||||||||||||||||||||||||||||||||||||||||
Дидрогестерон |
286 |
|
|
|
|
|
|
845 |
|
|
|
|
26400 |
||||||||||||||||||||||||||||||||||||||||||
Норэтистерон и левоноргестрел, сордержащие в молекуле этинильную группу, определяют методом алкалиметрического титрования. Навеску испытуемого образца субстанции гестагена растворяют в тетрагидрофуране, вспомогательный реагент – AgNO3, титрант – 0,1 М NaOH. Конечную точку титрования обнаруживают потенциометрически.
R-C CH + AgNO3 R-C C-Ag + HNO3;
HNO3 + NaOH NaNO3 + H2O.
Для количественного определения гестагенов в лекарственных средствах используют УФспектрофотометрию (дидрогестерон); фотометрию, основанную на образовании окрашенного соединения с изониазидом* (прогестерон), ВЭЖХ (норэтистерон, левоноргестрел).
ВЭЖХ – лекформы (НФ везде С18-СГ) |
|
|
|
|
|
ЛС |
ПФ |
Детекция, |
|
|
нм |
Таблетки норэтистерона |
вода – метанол (28:72) |
254 |
Таблетки левоноргестрела |
вода – ацетонитрил (1:1) |
220 |
* При взаимодействии прогестерона с изониазидом (гидразидом изоникотиновой кислоты) образуется продукт жёлтого цвета (λмакс = 380 нм). Реакцию проводят с метанольным раствором изониазида, содержащим HCl.
2011/2012
Жерносек А.К. |
Фармацевтическая химия |
|
|
|
|
|
O |
|
|
|
|
|
N |
NH |
|
O |
CH |
|
O |
|
N |
CH3 |
CH |
|
|
CH3 |
|||
3 |
|
|
|
|
||
3 |
|
|
|
NH2 |
|
|
|
|
|
N |
|
|
|
H C |
+ 2 |
|
H3C |
|
|
|
|
|
|
|
|||
3 |
|
N |
H |
- 2H2O |
|
|
|
|
|
|
|||
O |
|
|
N |
N |
|
|
|
|
|
|
NH |
|
|
|
|
|
|
O |
|
|
2011/2012
