
22-
.pdf
Жерносек А.К.
ТЕМА 22
ГЕСТАГЕНЫ, АНДРОГЕНЫ И ЭСТРОГЕНЫ
Фармацевтическая химия
ПРОГЕСТЕРОН |
|
КРАЙНОН |
(PROGESTERONE) |
|
ПРОЖЕСТИН-КР |
|
|
ПРОЖЕСТОЖЕЛЬ |
O |
CH3 |
СУСТЕН |
CH3 |
УТРОЖЕСТАН |
|
|
|
|
H3C |
|
|
O


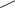
прегнен-4-дион-3,20
Растворы масляные для инъекций 1% (10 мг/мл), 2,5% (25 мг/мл) и 100 мг/мл; гель вагинальный 8%; гель для наружного применения 1%; мягкие желатиновые капсулы по 100 и 200 мг.
НОРЭТИСТЕРОН НОРКОЛУТ
(NORETISTERONE)
CH CH3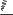 OH
OH
O


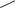
17-гидрокси-19-нор-17 -прегнен-4-ин-20-он-3
Таблетки по 5 мг.
ЛЕВОНОРГЕСТРЕЛ
(LEVONORGESTREL)
CH
H3C



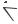 OH
OH
17 -гидрокси-18,19-динор-13 -
O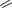

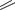

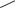 этил-17 -прегнен-4-ин-20-он-3
этил-17 -прегнен-4-ин-20-он-3
Таблетки по 0,75 мг (ПОСТИНОР) и 1,50 мг (ЭСКАПЕЛ); КЛИМОНОРМ (драже 0,15 мг + 2,0 мг эстрадиола валерата); РИГЕВИДОН (таблетки ПО 0,15 мг + 0,03 мг этинилэстрадиола); ТРИКВИЛАР (драже), ТРИ-РЕГОЛ (таблетки ПО) с ЭЭ 0,05/0,03; 0,075/0,04; 0,125/0,03.
МЕДРОКСИПРОГЕСТЕРОНА АЦЕТАТ |
ДИДРОГЕСТЕРОН |
|
|||
(MEDROXYPROGESTERONE ACETATE) |
(DYDROGESTERONE) |
ДЮФАСТОН |
|||
O |
|
|
|
||
CH3 |
ПРОВЕРА |
O |
|
||
CH3 |
CH3 |
||||
O |
ДЕПО-ПРОВЕРА |
CH3 |
|||
H3C |
CH3 |
|
H3C |
|
|
|
O |
|
|
||
O |
|
|
O |
|
|
CH3 |
|
|
|
||
|
|
9 ,10 -прегнадиен-4,6-дион-3,20 |
|||
|
|
|
|||
6 -метил-3,20-диоксопрегнен-4-ил-17 ацетат |
Таблетки ПО по 10 мг; ФЕМОСТОН |
||||
Таблетки по 500 мг; суспензия для в/м |
|||||
(таблетки 10 мг + 2 мг эстрадиола либо |
|||||
введения 150 мг/мл и 500 мг/3,3 мл. |
|||||
5 мг/1 мг, 10 мг/1 мг). |
|||||
|
|
|
|||
|
|
2011/2012 |
|
||
1
Жерносек А.К.
ТЕСТОСТЕРОН
(TESTOSTERONE)
CH3OH
H3C
O


 17 -гидроксиандростен-4-он-3
17 -гидроксиандростен-4-он-3
Тестостерон: гель 1% для наружного применения (АНДРОГЕЛЬ).
Тестостерона ундеканоат: капсулы по 40 мг (АНДРИОЛ ТК); раствор для в/м введения 250 мг/мл (НЕБИДО, ОМНАДРЕН 250 – смесь эфиров).
Фармацевтическая химия
МЕТИЛТЕСТОСТЕРОН
(METHYLTESTOSTERONE)
CH3OHCH3
H3C
O



17 -гидрокси-17 -метиландростен-4-он-3
Таблетки по 5 и 10 мг.
МЕТАНДИЕНОН
(METANDIENONE)
OH МЕТАНДРОСТЕНОЛОН CH3 CH3 НЕРОБОЛ
H3C 


 ДИАНАБОЛ
ДИАНАБОЛ
O



17 -гидрокси-17 - метиландростадиен-4-он-3
Таблетки по 1 и 5 мг.
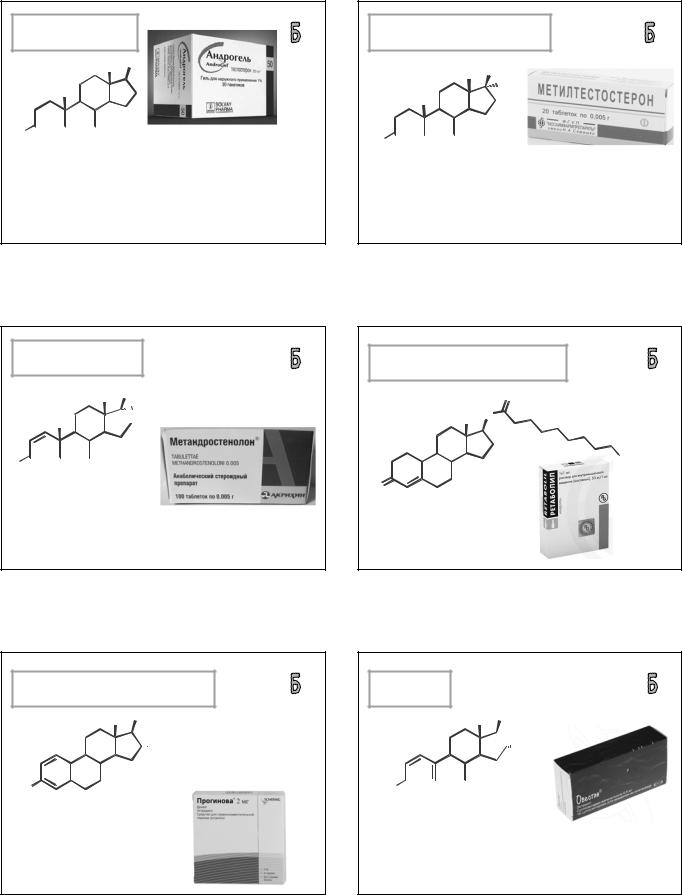
НАНДРОЛОНА ДЕКАНОАТ |
|
|
(NANDROLONE DECANOATE) |
|
|
O |
РЕТАБОЛИЛ |
|
CH3O |
||
|
||
|
CH3 |
|
O |
|
|
3-оксоэстрен-4-ил-17 -деканоат |
|
|
Масляный раствор для |
|
|
инъекций 50 мг/мл. |
|
ЭСТРАДИОЛА ГЕМИГИДРАТ
(ESTRADIOL HEMIHYDRATE)
|
|
|
|
|
CH |
OH |
|
|||
|
|
3 |
|
ЭСТРОЖЕЛЬ |
||||||
|
|
|||||||||
|
|
|
|
|
|
|
|
0,5H2O |
ПРОГИНОВА |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
Эстрадиола валерат |
||
|
|
|
|
|
|
|
|
Эстрадиола бензоат |
||
HO |
||||||||||
|
|
|||||||||
эстратриен-1,3,5(10)-диол-3,17 |
|
|||||||||
Гель трансдермальный |
|
|||||||||
0,6 мг/г; драже по 2 мг. |
|
|||||||||
ЭСТРИОЛ
(ESTRIOL)
CH3OH ОВЕСТИН




 OH
OH
HO


эстратриен-1,3,5(10)-триол-3,16 ,17
Суппозитории вагинальные по 0,5 мг; крем для интравагинального применения 1 мг/г; таблетки по 0,2 мг.
2011/2012
2

Жерносек А.К.
ЭТИНИЛЭСТРАДИОЛ
(ETHYNILESTRADIOL)
CH3 OH








 CH
CH
HO


19-нор-17 -прегнатриен-1,3,5(10)-ин-20-диол-3,17
Входит в состав комбинированных ЛС с гестагенами (ТРИ-РЕГОЛ, ТРИКВИЛАР, ЯРИНА, ЛОГЕСТ, ДЖЕС и др.)
Фармацевтическая химия
ГЕКСЭСТРОЛ
(HEXESTROL)
СИНЭСТРОЛ
H3C
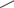

 OH
OH
HO


 CH3
CH3
мезо-3,4-бис-(4-гидроксифенил)гексан
Масляный раствор для инъекций 0,1% и 2%.
2011/2012
3
Жерносек А.К. |
Фармацевтическая химия |
ГЕСТАГЕНЫ
Гестагенами, или прогестагенами (gesto – ношу, gennao – рож-
даю) называют гормоны, регулирующие беременность у плацентарных животных. Данные вещества подготавливают слизистую матки к имплантации зародыша и сохраняют его во время беременности.
Природным гестагенным гормоном является прогестерон. По химическому строению это вещество относится к производным прегнана.
O
CH3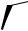 CH3
CH3
H3C
прогестерон
O
Прогестерон был открыт в 1928 году В.М. Алленом (США). Его строение было установлено в 1934 году А.Бутенандтом.
Прогестерон образуется как в женском, так и в мужском организмах: в яичниках, яичках и надпочечниках. Веществом, из которого синтезируется данный гормон, является прегненолон, представляющий собой производное холестерина. Процесс превращения прегненолона в прогестерон состоит из двух стадий: окисление 3-OH группы до оксогруппы и перемещение двойной связи из пятого в четвёртое положение.
O |
CH |
O |
CH3 |
|
|
||
CH3 |
3 |
CH3 |
|
|
|
||
H3C |
|
H3C |
|
HO |
O |
|
|
прегненолон |
|
|
|
Сам прогестерон является исходным веществом для получения других гормонов: альдостерона, кортизола, андростендиона.
В клетках-мишенях прогестерон активирует прогестероновые рецепторы, расположенные в цитоплазме. Комплексы прогестерона с рецепторами затем проникают в ядро, где связываются с рецепторной последовательностью нуклеотидов ДНК. Взаимодействие прогестерона с рецептором происходит за счёт фрагмента молекулы, содержащего оксогруппу, сопряжённую с двойной связью (такую же группировку атомов имеют и кортикостероиды, однако конформация этой группы отли-
1
2011/2012

Жерносек А.К. |
Фармацевтическая химия |
чается и связывания данных веществ с прогестероновыми рецепторами не происходит).
В печени прогестерон подвергается интенсивному метаболизму. Время полужизни данного гормона в плазме составляет всего 5 минут. Метаболическим превращениям подвергаются, главным образом, заместители, находящиеся в кольцах A и D. Вначале происходит восстановление оксогруппы в 20-м положении, затем двойной связи и оксогруппы в 3-м положении, гестагенная активность при этом утрачивается.
фрагмент молекулы, необходимый для взаимодействия с рецептором
H3C
 O
O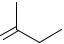

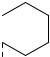
O |
CH |
HO |
CH3 |
|
CH |
CH3 |
|||
3 |
|
|||
3 |
|
|
|
|
|
|
H3C |
|
|
|
HO |
нективный метаболит |
||
|
OH |
|
||
|
|
|
||
Лекарственными формами прогестерона являются масляный раствор для инъекций, капсулы (принимают интравагинально и внутрь) и гель. Данное вещество используется при аменорее, дисменорее, бесплодии, невынашивании беременности, при заместительной гормонотерапии в период менопаузы, эндометриозе, раке матки и молочной железы и т.д.
Полусинтетические гестагены (прогестины). Первый прогестин
– этистерон (прегнин) – был открыт случайно в 1938 году. Оказалось, что вещество, полученное при введении в 17-е положение молекулы тестостерона этинильной группы, обладало гестагенной активностью и в отличие от прогестерона сохраняло эту активность при пероральном применении.
CH3OH

 C
C CH
CH
H3C
этистерон
O
Этистерон стал прототипом для других полусинтетических гестагенов. При получении прогестинов проводилась такая модификация структуры прогестерона (защита оксогруппы при С21 и кольца А), чтобы при сохранении (или даже повышении) гестагенной активности вещество было бы устойчивым к метаболическим превращениям и могло бы применяться перорально.
Защита оксогруппы, находящейся в боковой цепи молекулы прогестерона, может быть проведена следующими способами:
2
2011/2012
Жерносек А.К. |
Фармацевтическая химия |
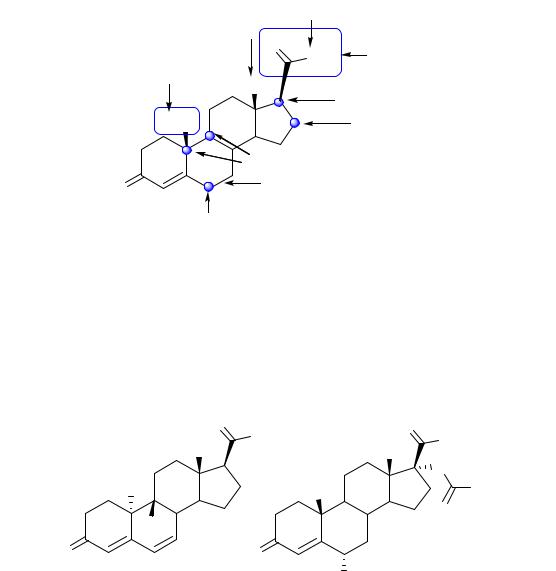
 введение заместителей в кольцо D: ацил, алкил или атом галогена – в 17-е положение либо алкил или циклоалкил – в 16-е положение;
введение заместителей в кольцо D: ацил, алкил или атом галогена – в 17-е положение либо алкил или циклоалкил – в 16-е положение;  введение OH-группы, атома галогена или алкильного радикала
введение OH-группы, атома галогена или алкильного радикала
в 21-е положение;
 замена 17 -ацетильной группы на комбинацию 17 - этинильной и 17 -гидроксильной групп.
замена 17 -ацетильной группы на комбинацию 17 - этинильной и 17 -гидроксильной групп.
Для защиты кольца А и увеличения гестагенной активности могут быть проведены следующие модификации структуры прогестерона:
 введение CH3-группы или атома галогена в 6-е положение;
введение CH3-группы или атома галогена в 6-е положение;
 введение дополнительной двойной связи в 6-е положение;
введение дополнительной двойной связи в 6-е положение;
 инверсия конфигурации атомов C9 и C10 (ретростероиды);
инверсия конфигурации атомов C9 и C10 (ретростероиды);  удаление С19 (19-норстероиды), при этом метильная группа С18
удаление С19 (19-норстероиды), при этом метильная группа С18
может замещаться этильной.
|
замена метильной |
|
атом галогена или алкил |
|||
|
группы этильной |
O |
21 |
замена ацетильной группы |
||
|
|
|
|
|||
|
|
|
|
на комбинацию этинильной |
||
|
|
|
|
|
CH3 |
|
удаление метильной группы |
18 |
CH |
|
и гидроксильной |
||
|
|
|
|
|||
|
|
|
|
3 |
|
ацил, алкил, атом галогена |
|
19 |
|
|
17 |
|
|
|
|
|
|
алкил или циклоалкил |
||
|
H3C |
|
|
16 |
|
|
|
|
9 |
изменение конфигурации |
|||
|
10 |
6 |
||||
O |
|
|
дополнительная |
|||
|
|
|
||||
|
|
|
двойная связь |
|||
|
|
метил |
|
|||
|
|
|
|
|
|
|
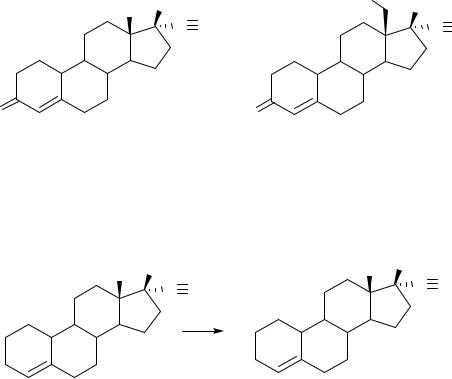
В нестоящее время в медицинской практике используется более 20 различных прогестинов. Обычно их разделяют на две группы: производные прегнана (содержат, как и прогестерон, в 17-м положении ацетильный радикал) и производные тестостерона и 19-нортестостерона (содержат в 17-м положении этинильную и гидроксильную либо сложноэфирную группы). Формулы некоторых полусинтетических гестагенов приведены ниже
 производные прогестерона
производные прогестерона
O |
CH3 |
O |
CH |
|
CH3 |
CH |
|||
|
3 |
|||
|
|
3 |
O |
|
H3C |
|
|
||
|
H C |
CH3 |
||
|
|
3 |
O |
|
H |
|
|
||
|
|
|
||
O |
O |
|
|
|
Дидрогестерон |
|
CH3 |
|
|
|
Медроксипрогестерона ацетат |
|||
3
2011/2012
Жерносек А.К. |
Фармацевтическая химия |
 производные тестостерона и 19-нортестостерона (см. также этистерон)
производные тестостерона и 19-нортестостерона (см. также этистерон)
CH OH |
HO |
OH |
|
|
|||
3 |
C CH |
|
C CH |
|
|
||
O |
|
O |
|
Норэтистерон |
|
Левоноргестрел |
|
|
|
|
|
Кроме активных форм прогестинов в медицинской практике используются их пролекарства, например, линестренол. В молекуле данного вещества отсутствует оксогруппа в 3-м положении. В печени линестренол окисляется с образованием норэтистерона.
CH3 |
OH |
CH OH |
|
C CH |
3 |
C CH |
|
|
|
||
O
линестренол норэтистерон
Классификация АТХ
G03 Половые гормоны и модуляторы половой системы G03D Прогестагены
G03DA Производные прегнена-4
 G03DA02 Медроксипрогестерон
G03DA02 Медроксипрогестерон
 G03DA04 Прогестерон
G03DA04 Прогестерон
G03DB Производные прегнадиена
 G03DB01 Дидрогестерон G03DС Производные эстрена
G03DB01 Дидрогестерон G03DС Производные эстрена
 G03DС02 Норэтистерон
G03DС02 Норэтистерон
Полусинтетические гестагены применяют по тем же показаниям, что и прогестерон. Кроме того, данные вещества индивидуально либо вместе с эстрогенами входят в состав пероральных контрацептивов. Основной лекарственной формой для прогестинов являются таблетки.
Способы получения. Прогестерон выделяют из природных источников (яичники свиней), а также получают полусинтетическим путём из холестерина, диосгенина, соласодина и других стероидов. Например, получение прогестерона из соласодина включает в себя следующие стадии.
4
2011/2012
Жерносек А.К. |
Фармацевтическая химия |
Вначале гидроксильную группу в молекуле соласодина этерифицируют уксусным ангидридом и окисляют образовавшийся сложный эфир дихроматом натрия.
H3C |
H |
|
O |
|
N |
|
CH3 |
||
CH3 |
|
|
CH3 |
|
|
|
|
||
H3C |
O |
1) Ac2O |
H3C |
|
|
2) Na2Cr2O7 |
|
||
|
|
O |
|
|
HO |
|
H3C |
O |
|
соласодин |
|
|
|
|
Полученный сложный эфир гидролизуют и гидрируют одну двойную связь водородом в присутствии никеля.
|
|
O |
CH3 |
O |
CH3 |
|
|
CH3 |
|||
|
|
CH3 |
|||
|
|
1) H2O |
|
||
|
H3C |
|
H3C |
|
|
|
|
2) H2/Ni |
|
||
O |
|
|
|
||
|
|
|
|
|
|
H3C O |
|
|
HO |
|
|
|
|
|
|
прегненолон |
|
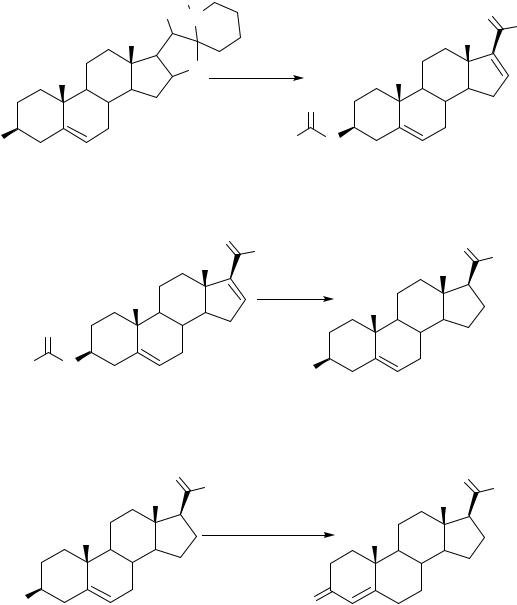
На последней стадии прегненолон окисляют до прогестерона по реакции Оппенауэра.
O |
CH3 |
O |
CH3 |
CH3 |
CH |
||
|
циклогексанон |
3 |
|
H3C |
H3C |
|
|
изопропилат |
|
||
|
алюминия |
|
|
HO |
O |
|
|
|
|
прогестерон |
|
5
2011/2012

Жерносек А.К. |
Фармацевтическая химия |
АНДРОГЕНЫ
Андрогены – гормоны, стимулирующие развитие и функционирование мужской генитальной системы, развитие вторичных половых признаков, регулирующие рост и некоторые стороны поведения человека и животных.
Природным андрогеном является тестостерон
OH
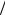 17
17
O 3 4
17 -гидроксиандростен-4-он-3
В качестве лекарственных веществ используют различные сложные эфиры прогестерона: пропионат, энантат, деканоат, изокапронат.
Полусинтетическим андрогеном является метилтестостерон.
OH 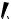

 CH3
CH3
O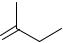

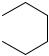
Тестостерон неактивен при приёме внутрь и используется только парентерально, причём эфиры тестостерона обладают пролонгированным действием. Метилтестостерон применяется перорально в виде таблеток.
Анаболики. Анаболическими веществами называют синтетические лекарственные вещества, стимулирующие синтез белка в организме и кальцификацию костной ткани. Одним из эффектов действия данных веществ является увеличение массы скелетной мускулатуры.
Различают нестероидные (оротат калия, рибоксин) и стероидные анаболические вещества. Анаболики стероидной структуры можно разделить на
 производные андростана;
производные андростана;
6
2011/2012

Жерносек А.К. |
Фармацевтическая химия |
OHCH |
OHCH3 |
|
3 |
O |
HO |
метандростенолон |
метиландростендиол |
 производные эстрана (19-норстероиды).
производные эстрана (19-норстероиды).
O
O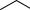 R
R
O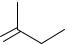

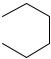
эфиры нандролона
Фенилпропаноат нандролона называется феноболином, деканоат – ретаболилом и т.д.
OHCH3 |
|
OHCH3 |
|
HO |
N |
|
|
O |
N |
|
|
H |
станозолол |
||
оксиметолон |
|||
|
Способы получения. Тестостерон получают полусинтетическим путём. Например, вначале из холестерина в несколько стадий (Ac2O, Br2, CrO3, Zn, NH2CONHNH2, HCHO) получают ацетат дигидроэпиандростерона. Затем данное вещество гидрируют и после защиты OHгруппы в 17-м положении окисляют по реакции Оппенауэра.
O OH
|
H2/Ni |
AcO |
AcO |
|
7
2011/2012
